¿Cuál es el uso del extracto de Ginseng ginsenósido?
Los ginsenósidos son los principales ingredientes farmacológicamente activos extraídos de las raícesPanax ginseng en la familia de las Araliaceae. Tienen los efectos de impulsar el body's promover el metabolismo de los materiales, combatir los tumores, combatir la fatiga y combatir el envejecimiento. En los últimos años, la investigación en los ingredientes activos individuales de los ginsenósidos ha hecho buen progreso en el tratamiento de enfermedades. El siguiente es un resumen del progreso de la investigación en los últimos dos años.
1. Mejorar el sistema inmunológico
Zhang Caixun et al. encontraron que despuésGinseng saponin Rhl [20, 40, 80 mg/(kg·d)]Se administró a ratones con baja función inmune, los índices de bazo y timo, función fagocím − y proliferación de linfot de los ratones en cada grupo de dosis mejoraron significativamente.
Pan Weihua et al. utilizaron el método MTT y la prueba de red neutra para determinar los efectos de cada componente de saponina ginseng en la proliferación de linfocitos esplénicos y la función fagocíde macrófagos. Los resultados mostraron queGinseng saponin components (en inglés)Los resultados obtenidos con diferentes concentraciones de etanol tuvieron diferentes grados de promoción de la proliferación de linfocitos esplénicos de ratón y de la función fagocíde macrófagos dentro del rango de ensayo. Entre ellos, la fracción de ginsenósido elutada con etanol al 70% tuvo el efecto promotor más fuerte, lo que sugiere que la fracción de ginsenósido obtenida elutando ginsenósidos con etanol al 70% tiene un buen efecto inmunopotenciador.
Zhou Yingwu et al. utilizaron la tecnología biochip para detectar el efecto deGinsenósido RglEn la expresión de genes relacionados con la regulación funcional de las células dendríticas de ratón (Dc), y encontró que el ginsenósido Rg3 afecta Dc mediante la regulación de la expresión de múltiples genes, que controlan y afectan a la función, la diferenciación y la maduración de Dc, proporcionando pistas para la identificación de nuevas dianas del fármaco.
Lo anterior sugiere que los componentes ginsenoside pueden ser desarrollados y utilizados como potenciadores inmuneficaces.
2 efectos antitumorales
Fang et al. estudiaron el efecto de Rg3 en la densidad microvascular (MVD) de un modelo de trasplante de hepatoma de ratón desnudo. Los resultados mostraron que el grupo Rg3 de ratones desnudos no experimentó toxicidad obvia del medicamento, y la calidad de vida fue la mejor. El peso tumoral promedio en el grupo Rg3 fue menor que en el grupo control, y la diferencia fue significativa (P < 0. 05). El MVD en el grupo Rg3 fue significativamente menor que en el grupo control (P < 0. 001). El estudio también encontró que el Rg3 combinado con trióxido de arsétuvo el efecto más fuerte en los tumores de cáncer de hígado humano trasplantados en ratones, inhibiendo significativamente la proliferación de células cancerosas de hígado trasplantadas. Sugerencia: Rg3 puede reducir la expresión de MVD en el tejido tumoral e inhibir la neovascularización del cáncer de hígado. La aplicación combinada también tiene un mejor efecto sinérgico.
Liao Danqiong et al. usaron el método MTT y el método de inmunofluorescbrdu para detectar el efecto del ginsenósido Rg3 en la proliferación de células madre de tumor de glioma C6. El estudio encontró queEl ginsenósido Rg3 tiene un efecto inhibitsignificativoSobre la proliferación de células madre tumorales de glioma.
Liao Yilin et al. usaron MTT, agar blando tasa de formación clonogénica, morfoe inmunofluorescde proteína ácida fibrilar glial (GFAP) para identificar el grado de inducde la diferenciación de saponde ginseng en células de glioma C6 de rata. Los resultados mostraron que10ug/mL de saponinas de ginsengPuede inducir significativamente la diferenciación de las líneas celulares de glioma C6 de rata, que se manifiesta como la supresión de la proliferación, la pérdida de la capacidad clonogé, el crecimiento de protuberancias celulares, y el aumento de la expresión de glial fibrillary acid protein (GFAP). Esto indica que los ginsenósidos a una cierta dosis puede inducir la diferenciación de las células de glioma de rata para lograr un efecto antitumoral.
Zhao Ying et al. encontraron esoGinsenósicombinado con saponinas de clematisMostraron un efecto inhibitmuy significativo en los tumores trasplantados de sarcoma de ratón 180 (S180), ascide hepatoma (HepA) y ascileucémico (P388) todos los tumores trasplantados mostraron un efecto inhibitmuy significativo, con tasas de inhibide 52,41%, 53,57% y 54,15%, respectivamente, y un efecto significativo en la prolongación de la vida de los ratones. Esto sugiere que el uso combinado de hierbas medicinales chinas individuales también puede tener un mejor efecto antitumoral.
Un estudio realizado por Cong Zhongyi lo demostróGinsenósido Rg3 puede inhibir la proliferación de humanosCélulas de cáncer de colon SW480 in vitro, lo que indica que los ginsenósidos pueden usarse como fármacos adyuven el tratamiento clínico del cáncer de colon para reducir los efectos secundarios de los fármacos quimioterapéuticos.
Usando un modelo tumoral de trasplante de ratón, Xiaojie Gong y otros encontraron que el estestarato M1 de ginsenósido puede inhibir significativamente el crecimiento de células cancerosas de hígado y células cancerosas de estómago en ratones después de un período de acción, y tiene efectos antitumsignificativos sin efectos secundarios tóxicos.
Jiang Xin et al. usaron células de melanoma B16 para establecer un modelo de metástasis pulmonar espontánea y un modelo de tumor sólido en ratones por inoculación subcutánea, y observaron el número de metástasis de tumores pulmonares después de la inyección intraperitoneal de diferentes dosis de Rg3 (al grupo control se le administró una solución de clorsódico al 0,9%), y detectaron la expresión de la proteína de la metaloproteinasa de matriz 9 (MMP-9) en los tumores sólidos. El ensayo de invasión de la cámara de Boyden y la tininmunohistoquímica se utilizaron para detectar el efecto de Rg3 en la capacidad de invasión de las células tumorales y la expresión de MMP-9. Los resultados mostraron que tras el tratamiento con diferentes dosis de Rg3 (0. 3, 1. 0 y 3. 0 mg/kg), el número de metástasis pulmonares en ratones fue menor y el nivel de expresión de MMP-9 en tejido tumoral se redujo, lo que fue estadísticamente significativo (P < 0. 05) comparado con el grupo control. In vitro, el número de células B16 que invadieron a través de la membrana basal artificial en los grupos de tratamiento con Rg3 de 2,5 y 5,0 μg/mL fue significativamente menor que en el grupo control (P < 0,01), y 5,0 μg/mL Rg3 pudo inhibir la expresión de MMP-9 en las células tumorales. Esto indica que el Rg3 puede inhibir la metástasis pulmonar de células de melanoma de ratón, y su efecto de metástasis antitumoral puede lograrse mediante la reducción del nivel de expresión de MMP-9 en las células tumorales y la capacidad de invasión de las células.
El estudio también encontró esoGinsenósido Rg3A ciertas concentraciones pueden mejorar la expresión génica de las células de cáncer de mama humano MCF-7 Cx26 y restaurar la función de comunicación juncional intercelular de 0 huecos (GJIC) de las células MCF-7. Este puede ser uno de los mecanismos por los cuales el ginsenósido Rg3 inhila la proliferación celular MCF-7 y ejerce un efecto antitumoral.
Wang Yan et al. encontraron que en pacientes con cáncer de pulmón de células no pequeñas en estadio III B que es inoperable, después de dos ciclos de quimioterapia y oralAdministración de ginsenósido Rg3El factor de crecimiento endotelial vascular sérico (VEGF) y los niveles de CEA disminuyeron significativamente en promedio, la puntuación KPS de calidad de vida mejoró significativamente y la incidencia de efectos secundarios tóxicos se redujo significativamente.
Huang Jingzi et al. encontraron esoEl ginsenósido Rg3 inhiel el crecimiento de células no pequeñasEl cáncer de pulmón, inducido la apoptosis de las células tumorales, y aumentó significativamente la sensibilidad a la radioterapia a través de estudios experimentales sobre el efecto radiosensibilizante de ginsenoside Rg3 en el cáncer de pulmón de células no pequeñas.
En resumen:Rg3 ginsenoside puede inhibir la angiogénesis tumoral,Inducir la diferenciación de células tumorales, y reducir la invasión de células tumorales, proporcionando una base fiable para el desarrollo de fármacos antitumorales.
3 efecto anti-envejecimiento
Zhou Liping et al. estudiaron laEfecto antienvejecimiento de ginsenósido Rg1. El ginsenósido Rg1 se administró por inyección intraperitoneal a un modelo de ratón de Alzheimer#39; enfermedad s (da) causada por la proteína beta-amiloide 25-35 (A ≥ 25-35), y la prueba de laberinto acuático de Morris se utilizó para probar el aprendizaje de intervalo estrecho y la capacidad de memoria de los ratones, y la tecnología RT-PCR se utilizó para detectar la expresión del gen bcl-2 en el hipocampo. Los resultados mostraron que Rg1 puede reducir la latencia y la distancia total de los ratones con AD (q=5.478, 6.097, P < 0.05), aumentar el número de veces que cruzan la plataforma (g=6.023, P < 0.05), invirtiendo la disminución en la expresión génica de bcl-2 causada por A ≥ 25-35 (q=9.661, P < 0.05). Esto indica que Rg1 puede reducir el daño causado por A − 25-35 A las neurondel hipocampo en ratones, y el mecanismo puede estar relacionado con la activación de la vía del receptor de estrógeno.
Ginsenósido Rg1 puede inhibir el proceso de envejecimientoMediante la regulación de la expresión de P16 INK4a y P21 Cip/WaflmRNA y proteína en ratas de envejecimiento indupor d-galactosa, lo que impide que las células en el tejido cerebral de entrar en el proceso de envejecimiento. Zhou Yue et al. encontraron que el ginsenósido Rgl puede retrasar el envejecimiento de las células madre hematopoyéticas (HSC) y sus mecanismos relacionados a través dela investigación: Rgl tiene el efecto de retrasar y tratar el envejecimiento de Sca-1+HSC, y el p16INK4a_Rb y p19Arf_Mdm2-p53-p2-P21 cip1/ WMFL vías de señalización puede desempeñar un papel importante.
Li Xi et al. estudió el efecto deGinsenósido Rg1 en la fosforilación de la proteína tauEn rebanadas de cerebro de rata causadas por ácido okadaico (OA), y encontró que el ginsenósido Rg1 puede upreregular la expresión de la proteína fosfatasa 2A (PP2A) en un modelo de rebande de cerebro de rata de la fosforilación de la proteína tau similar a ad, promoviendo así la desfosforilación de la proteína tau fosforilada (P-tau) en el hipocampo, y por lo tanto inhibila fosforilación de la proteína tau. Esto sugiere que el GSR tiene un cierto efecto preventivo y terapéutico sobre la AD. 4 efectos antiinflamatorios y antioxidantes PP2A), promoviendo así la desfosforilación de la proteína tau fosforilada (P-tau) en el hipocampo, y de esta manera inhibila fosforilación de la proteína tau. Se sugiere que Rgl tiene un cierto efecto preventivo y terapéutico sobre AD.

4 efectos antiinflamatorios y antioxidantes
Zhao Baosheng et al. encontraron esoGinsenósido Rgl en el altoLos grupos de dosis media y baja inhibieron significativamente el grado de inflamación del oído en ratones causado por xileno (P < 0. 05 o P < 0. 01). También se encontró que las dosis altas de Rgl ginsenósido mostraron un cierto efecto inhibitorio sobre la proliferación de tejido granular inflamsubagudo (P < 0. 01).
Lu Zhenchao et al. aseptically retirpiezas de cartílago de espesor total de las articulaciones de la rodilla de conejos blancos de nueva Zelanda y cultivlas células de cartílago externamente. Después de cultivar con éxito las células de cartílago, establecieron un grupo conGinsenósidos Rg1 y Rb1 y un grupo control. La IL-1 se utilizó para inducir apoptosis en las células del cartílago, y se utilizó un citómetro de flujo para detectar el número y la proporción de células apoptóticas. Se utilizó un microscopio electrónico de transmisión para observar la estructura morfológica y submicroscópica de las células apoptóticas. Los resultados mostraron que los ginsenósidos Rg1 y Rb1 pueden inhibir significativamente la apoptosis excesiva de los condrocitos, inhibir la aparición y el desarrollo de la osteoartritis de rodilla, y no hay diferencia significativa entre los dos en el proceso de proliferación y apoptosis. El mecanismo es principalmente para eliminar los radicales libres producidos durante el metabolismo celular y reducir la producción de peróxidos lipícelulares, creando un ambiente favorable para prevenir el envejecimiento celular y reparar células, y proporcionando una base teórica para futuros experimentos in vivo.
Zhang Dailei et al. usaron cultivos in vitro de células espermatogoniales de ratón, y añadi.Ginsenoside GS (0,1 a 10 mg/L)Hipoxantina/xantina oxid(HX/XO) sola o en combinación. El oxígeno activo producido por el sistema (HX/XO) puede causar una disminución en la actividad de las células germinativas, un aumento en la cantidad de MDA producida, y una disminución en la actividad de SOD y los niveles de GSH. La adición de ginsenósido (0. 1-10mg/L) puede restaurar la actividad de las células reproductivas, la actividad de SOD y los niveles de GSH causados por (HX/XO), así como el aumento en la producción de MDA. Esto indica que el ginsenósido GS puede proteger a las células germinales del daño oxidativo causado por especies reactivas de oxígeno al inhibila peroxidlipíy eliminar los radicales libres en las células germinales a través de su efecto antioxidante, manteniendo así un sistema antioxidante normal.
Li Zhenbin et al. establecieron un modelo de rata de artritis adyuvpor inyección intradérmica de Freund& completo#39;s adyuv, y estudió los efectos de tigogenina TG de Thunder God vine enCombinación con ginsenoside GSSobre TNF- -, IL-1 - y MIF en ratas con artritis adyuvante. Los resultados mostraron que tanto la TG como la GS inhibieron significativamente el índice de artritis AI en ratas con artritis adyuv, redujeron los niveles de las citocinas inflamatorias séritnf - -, IL-1 - y los niveles de MIF, y pueden tener un efecto beneficioso sobre la patología articular. La combinación de TG y GS mostró un cierto efecto sinérgico, y el mecanismo de acción puede estar relacionado con su inhibición de la expresión de las citocinas inflamatorias TNF- -, IL-1 - y MIF. Se especula que la combinación de ingredientes efectivos de la medicina China puede ser una manera importante de mejorar aún más la eficacia clínica de la artritis reumatoide (AR), y es digno de investigación en profundidad.
Lo anterior muestra que los ginsenósidos pueden ejercer efectos anti-inflamatorios y antioxidantes por la eliminación de los radicales libres en el cuerpo y la inhibición del daño oxidativo.
Inhibición de la apoptosis de células endotelivasculares 5
He Guoyang et al. Se cultivaron células endotelide vena umbilical humana (HU VECs) in vitro y se observó el efecto del ginsenósido Rg 1 sobre la apoptosis de HUVECs indupor angiotensina II (Ang −). La apoptosis se detectó mediante electroforeen gel de agarosa y tintinmediada por deoxnucleotidil transferasa terminal. Se constató que40 μg/mL ginsenósido Rg1Puede hasta cierto punto revertir la apoptosis de HUVECs indupor Ang Ⅱ, lo que sugiere que el ginsenósido Rg1 tiene un cierto efecto protector y terapéutico sobre el daño endotelial vascular. El mecanismo molecular de ginsenósido Rg1 en la inversión de Ang II inducida apoptosis de células endotelivasculares requiere una mayor investigación. Ginsenósido Rg1 también se ha encontrado que inhila la apoptosis indupor homocisteína (Hcy) de las células endotelide la vena umbilical humana, y este efecto puede estar relacionado con la upregulación de los niveles de eNOS en las células endotelivasculares.
6 efecto Antiviral
Chu Xiuling et al. usaron un modelo de pollos infectados artificialmente con Marek's virus de la enfermedad (MDV) yGinsenósido Rg3 administrado por vía oral. El efecto protector del fármaco en el organismo se evaluó utilizando indicadores como incidencia, tasa de protección y edad media de supervivencia. Los resultados mostraron que el ginsenósido Rg3 puede reducir significativamente la incidencia y la tasa de detección de tumores de pollos experimentales, proteger los órganos inmunde pollos infectados, mejorar la inmunidad de pollos infectados, y tiene efectos antivirales. El estudio también encontró que el ginsenósido y el derivado modificado 7 pueden reducir el grado de daño a los fibroblade embrión de pollo (MD V) infectados. Lo anterior sugiere que los ginsenósidos pueden ser utilizados como un buen antiviral medicina tradicional China, proporcionando una base para el desarrollo de nuevos medicamentos antivirales.
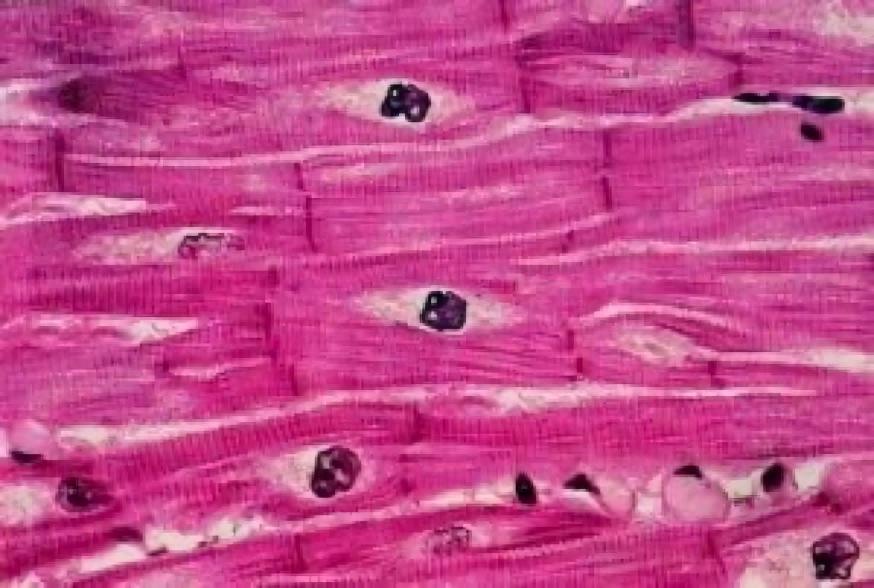
7 efecto protector sobre los cardiomiocitos
Ma Yongjie et al. utilizaron cultivos primarios de cardiomiocitos para causar daño celular utilizando un modelo de hipoxia-reoxigen. El efecto protector fue evaluado midiendo la viabilidad celular y la filtración de la lactato deshidrogenasa (LDH), y el estado antioxidante intracfue evaluado midiendo la actividad de la superóxido dismutasa (SOD). Los resultados mostraron queGinsenósido Rg1 (120 μmol/L)Los monómeros tanshinone II A (4 μmol/L) y tanshinone II A (4 mol/L), así como la combinación de ginsenósido Rg1 y tanshinone II A, pueden aumentar significativamente la viabilidad de los cardiomiocileados hipooxigenreoxigen. El efecto combinado es mejor que la monoterapia. La combinación de ginsenósido Rg1 (160 μmol/L) y tanshinone IIA (2 μmol/L) tiene el mejor efecto. La combinación de los dos monómeros también puede reducir el escape de LDH y aumentar la actividad de SOD en la hipoxi-reoxigenindupor lesión miocárdica. Esto muestra que la combinación de los dos monómeros, ginsenósido Rg1 y tanshinone IIA, tiene un efecto protector significativo sobre las células del miocardio dañadas por la hipoxia y la reoxigen. El mecanismo de su daño anti-oxidativo puede lograrse parcialmente mediante el aumento de la actividad de la enzima SOD. Zhao Yingjun et al. también encontraron que Gs-Rb1 puede inhibir la apoptosis indupor hipóxia de las células del miocardio mediante el aumento de la expresión de la supervivencia.
Wen Fei et al. observaron elEfecto protector del ginsenósido Rb1 sobre los cardiomiociindupor peróxido de hidrógenoApoptosis y encontró que el ginsenósido Rb1 puede reducir significativamente el daño a los cardiomiocicausado por el peróxido de hidrógeno, mejorando la viabilidad celular (P < 0. 01); Reducción de la fuga de LDH (P < 0. 01); Inhibir una disminución del potencial de la membrana mitocondrial (P < 0. 01); Y reduciendo significativamente el nivel de apoptosis (P < 0. 01). Se puede ver que el ginsenósido Rb1 puede reducir el daño celular causado por el peróxido de hidrógeno hasta cierto punto, estabilizar la estructura y la función de las mitocondrias celulares, e inhibir la apoptosis de las células del miocardio inducido por peróxido de hidrógeno.
Li Xuefeng et al. estudiaron el efecto del ginsenoside ER en la hipoxia de las células del miocardio en ratas y encontraron que el ginsenoside ER pretratamiento puede reducir la liberación de lactato deshidrogenasa (LD H) de las células del miocardio de rata hipóxica, mejorar significativamente la comunicación intercelular, y tiene un efecto protector significativo en las células del miocardio hipóxico. La dosis es especialmente adecuada para 20g/L.
Lo anterior sugiere que ginsenoside Rg1 tiene un buen efecto preventivo y terapéutico sobre la enfermedad coronaria, angina de pecho, insuficiencia cardíaca, etc.
8 Efectos cosméticos
Zhao Ziran et al. crearon un modelo de cicatriz hipertrófica de oreja de con, con el grupo experimentalInyeccon GS-Rg3 ginsenósido(concentración 6mg/mL) y al grupo control se le inyectó un volumen igual de solución salina al 0,9%. Después de 2, 4 y 6 semanas de administración, el tejido cicatricial fue removido y comparado con el grupo control usando el proceso de operación de etiquetado terminal in situ (TUNE L), observación histológica y otros métodos. En comparación con el grupo control, la piel en el grupo de tratamiento se volvió más delgada después de 6 semanas de administración, la disposición del colágeno fue más ordenada, el número de fibroblay vasos sanguíneos disminuyó; Y el número de fibroblasometidos a apoptosis aumentó significativamente con la administración prolongada. La observación macromostró que alrededor de 60 días después de la aplicación del medicamento, la cicatriz comenzó gradualmente a suavi, encode de tamaño y tiende a aplanarse. El grupo de control, sin embargo, continuó proliferando. Esto indica que el ginsenósido Rg3 puede inducir apoptosis de fibrobla, inhibiendo la formación de cicatrices patológicas, proporcionando una base teórica importante para futuras aplicaciones clínicas.

Song Wengang et al. estudiaron el efecto deGinsenósido Rb1En la tirosinasa de hongo in vitro mediante la detección de la actividad de la tirosinasa de hongo y se estudió el efecto del ginsenósido Rb1 en la proliferación de células de melanoma B16 mediante la medición de la tasa de proliferación celular. En los resultados se observó que el efecto del ginsenósido Rb1 en la proliferación de células de melanoma B16 cambia con la concentración. Cuando la concentración másica de Rb1 es < 125 μg/mL, promueve la proliferación de células de melanoma B16; Cuando es > 125 μg/mL inhila la proliferación de células de melanoma B16. Se sugiere que el ginsenósido Rb1 tiene un cierto efecto blanqueador.
En resumen,Ginsenósidos puede ser ampliamente utilizado para la protección y el tratamiento de la cardiovascularSistemas nervioso, inmunológico y endocrino. En la actualidad, los ginsenósidos se utilizan en las siguientes cuatro maneras principales: en primer lugar, los componentes individuales de los ginsenósidos se utilizan por separado, con objetivos claros y resultados inmediatos; Segundo, el uso combinado de componentes individuales de los ginsenósidos tratando múltiples objetivos simultáneamente; Tercero, el uso combinado de diferentes ingredientes monoméricos efectivos de la medicina tradicional China basados en la idea de la diferenciación del síndrome y el tratamiento en la medicina tradicional China. Creo que esta es la tendencia de desarrollo de las prescripciones de compuestos; Cuarto, el uso combinado de saponinas de ginseng y drogas químicas puede mejorar la eficacia mientras reduce eficazmente los efectos secundarios tóxicos de las drogas químicas. Esta es también la tendencia de desarrollo de la combinación de la medicina tradicional China con la medicina occidental.
referencias
[1] Peng Bin, Chen Maoshan, Pu Ying, et al. Estudio preliminar sobre el efecto y mecanismo del ginsenósido Rg1 en retrasar el envejecimiento cerebral en ratas inducidas por d-galactosa [J]. Journal of Chongqing Medical University, 2011, 36 (4): 419-422.
[2] Lv Zhenchao, Guo Yanxing, Cao Xiangyang, et al. Efectos de ginsenósirgl y Rbl sobre la apoptosis de células de cartílago de rodilla cultivadas in vitro [J]. World Journal of Integrative Medicine, 2010, 5 (1): 32-34.
[3] Zhou Liping, Ge Keli, Chen Wanfang, et al. Efecto protector de ginsenoside Rgl en un daño inducido por un ≥ 25-35 A las neurondel hipocampo en ratones [J]. Journal of Qingdao University Medical College, 2011, 47 (3): 189-191.
[4] Yang Haidong, Lin Bilian. El efecto de Rgl ginsenósido antagoniel aumento de hierro en la sustancia negra inducido por MPTP en ratones [J]. Journal of Shanxi Medical University, 2011, 42 (1): 10-14.
[5] Huang Jingzi, Jin Xiangshun, Dong Mingxin, et al. Estudio Experimental sobre el efecto radiosensibilizador del ginsenósido Rg3 en el cáncer de pulmón de células no pequeñas [J]. Journal of Practical Oncology, 2010, 24 (3): 264-267.
[6] Zhang Qingqin, Tian Xiaojun, Li Shujun, et al. Efectos y mecanismos del ginsenósido Rg3 en la supervivencia a largo plazo después de una cirugía de cáncer de pulmón de células no pequeñas [J]. China Medical Frontier, 2010, 5 (21): 10-11.
[7] Chu Xiuling, Su Jianqing, Wei Xubin. The effect of ginsenosides and their derivatives against Marek& (en inglés)#Virus de la enfermedad 39;s detectado por método de observación de lesiones celulares [J]. Chinese Journal of Animal Science and Veterinary Medicine, 2010, 37 (3): 179-182.
[8] Zhao Yingjun, Kong Hongliang, Li Zhanquan, et al. El ginsenósido Rb1 mejora la apoptosis indupor hipóxia de cardiomiocide ratón a través de la supervivencia [J]. Guangdong Medicine, 2010, 31 (21): 2760-2762.
[9] Wen Fei, Zhang Fan, Leng Qin. Efecto protector del ginsenósido Rb1 sobre la apoptosis de cardiomiociindupor peróxido de hidrógeno [J]. Hubei Journal of Traditional Chinese Medicine, 2010, 32 (7): 5-7.
[10] Zhou Yingwu, Peng Guiying, Gu Ligang, et al. Utilizando la tecnología biochip para detectar el efecto de ginsenósido Rgl en la expresión de genes relacionados con la regulación de la función de las células dendríticas en ratones [J]. Chinese Journal of Immunology, 2010, 26 (7): 1086-1090.
[11] Wang Yan, Liu Jinglei, Zhao Hongli, et al. Observación de la eficacia de las cápsulas de ginseng saponin Rg3 combinadas con quimioterapia en el tratamiento del cáncer de pulmón de células no pequeñas avanzado [J]. Journal of Practical Oncology, 2011, 25 (1): 33-35
[12] He Guoyang, Li Yongzhen, Li Xinqiang, et al. Investigación sobre el efecto y mecanismo de ginsenósido Rg1 en la inhibición de la apoptosis indupor homocisteína de las células endotelide la vena umbilical humana [J]. Chongqing Medical Journal, 2011, 40 (14): 1376-1378
[13] Song Zhiying, Fu Kui, Hu Liyan, et al. Efectos del ginsenósido Rg3 sobre la expresión de los genes ID-1 y NRP-1 en tejidos de endometriosis [J]. Chinese Journal of Traditional Chinese Medicine and Clinical, 2011, 11 (7): 768-771
[14] Li D, Li Y, Han B, et al. Un estudio de toxicidad A largo plazo de la inyección de emulsión de C-K de saponina ginseng en conejos de nueva Zelanda [J]. Medicina China moderna educación a distancia, 2011, 9(3): 188-189.
[16] Yan Yuxian, Song Yueying, Wang Xiaoping, et al. Efectos del ginsenósido Rg1 sobre la acción crónica de la morfina y la retirada indupor naloxona en las células SK-N-SH y su mecanismo de acción [J]. Chinese Journal of Pharmacology, 2010, 26 (8): 1074-1078.
[17] Li Xuefeng, Shi Xiaohua, Luo Qizhi. El efecto del ginsenósido Re sobre la hipoxia en cardiomiocide rata [J]. Chinese Journal of Burns, 2011, 27 (3): 169-172.
[18] Liu Hesong, Zhao Ziran, Lan Shanshan, et al. Estudio Experimental sobre el efecto de ginsenósido Rg3 en la proliferación y apoptosis de fibroblahumanos [J]. Chinese Journal of Experimental Diagnostics, 2010, 14 (11): 1697-1700.
[19] Ma Yanmei, Wen Wenbin, Liu Jiwei. Efectos del ginsenósido Rg3 sobre la expresión del gen Cx26 y la función de comunicación intercelular de las células de cáncer de mama humano [J]. Tumor Research and Clinical Oncology, 2011, 23 (2): 91-93.
[20] Jiang Xin, Xin Ying, Xu Tianmin, et al. Efectos del ginsenósido Rg3 sobre la invasión, la metástasis y la expresión de MMP-9 en células de melanoma B16 en ratones [J]. Cáncer, 2011, 31(2): 117-121.
[21] Zhang Li, Xia Zhongyuan. Efecto protector del pretratamiento ginsenósido Rb1 sobre la lesión por isquemia y repermiocárdica en ratas diabéticas [J]. China Medical Guide, 2010, 12 (3): 446-449.
[22] Yan Yuxian, Song Yueying, Wang Xiaoping, et al. Efectos del ginsenósido Rb1 sobre la proliferación celular SK-N-SH crónica indupor la morfina y [Ca2+]i [J]. Chinese Journal of Drug Dependence, 2010, 19 (6): 468-471.
[23] Liao Danqiong, Zhang Jianping, Fu Yingen, et al. Efectos del ginsenósido Rg3 sobre la proliferación de células madre de glioma de rata [J]. Journal of Henan Medical College for Workers, 2011, 23 (2): 131-133.
[24] Dai Qun, Liu Pei. Efecto inhibitdel ginsenósido Rh2 sobre el crecimiento de las líneas celulares humanas de cáncer de colon SW620 y LOVO [J]. Zhejiang Journal of Integrated Traditional and Western Medicine, 2010, 20 (8): 466-467.
[25] Mao Yimin, Sun Yuxia, Wang Xueting, et al. Efecto de la intervención del ginsenósido en tallo y hoja sobre el contenido de TNF- - y expresión de IL-8 en tejido pulmonar de ratas con lesión pulmonar aguda [J]. Shizhen Traditional Chinese Medicine, 2010, 21 (5): 1107-1108.
[26] Zhao Ying, Liu Dan. Efecto inhibitdel ginsenósido Rg3 sobre el crecimiento de células epiteliales del cristalhumano [J]. International Journal of Ophthalmology, 2011, 11(1): 25-27.
[27] Wang Hua, Zhou Bin, Guo Xing, et al. Efectos del ginsenósido Rh2 sobre la proliferación celular y el citoesqueleto de células SMMC-7721 [J]. Chinese Journal of pathophysiology, 2011, 27 (6): 1226-1229.
[28] Li Zhenbin, Ma Hua, Xu Zheng, et al. Efectos del compuesto de TCM que contiene polisacáridos de TCM y ginsenósidos sobre TNF- -, IL-1 - y MIF en ratas con artritis adyuv[J]. Chinese Journal of PLA Medicine, 2011, 23(2): 9-11.
[29] Li Xi, Liu Ying, Yuan Haifeng, et al. Efectos del ginsenósido Rg1 sobre la fosforilación de la proteína tau en cortes de cerebro de rata causados por ácido okadaico [J]. Journal of Integrated Traditional and Western Medicine, 2010, 8 (10): 955-959.
[30] Liu Guoliang. Una breve discusión sobre el progreso de la investigación de ginsenoside Re [J]. Jilin agricultura, 2011 (3): 253.
[31] Gong Xiaojie, Chen Lirong. Investigación sobre la actividad antitumoral del estearato M1 ginsenósido [J]. Ginseng Research, 2010 (2): 9-11.
[32] Zhao Qingxia, Xu Yan, Yan Wenhai, et al. Observación del efecto inhibidor del ginsenósido Rb1 sobre la apoptosis indupor un ≥ 25-35 de las células nervide las ratas [J]. Shandong Medicine, 2010, 50 (30): 29-30.
[33] Liu Hongying, Ge Junbo, Ma Xiaojuan, et al. Chinese Journal of Integrated Traditional and Western Medicine, 2011, 31 (3): 350-354.
[34] Song Wengang, Sun Liwei, Li Yu. Estudio preliminar sobre el efecto blanqueador del ginsenósido Rb1 [J]. Journal of Jilin Agricultural University, 2010, 32 (5): 498-499, 504.
[35] Chu Shifeng, Zhang Juntian. Análisis de acción y mecanismo multiobjetivo de ginsenósido Rg1 [J]. Journal of Medical Research, 2010, 39 (5): 11-15.
[36] Li Qian, Zhang Yanmin, Guan Ming, et al. Efectos de ginsenoside Rg1 sobre la isquemia intestinal/lesión de reperfusión en ratas [J]. Chinese Journal of Pharmacology, 2010, 26 (3): 358-361.
[37] Fang Qing, Lu Weihua, Zhao Zhigang. Efecto protector del ginsenósido Rg1 sobre las células ganglionde la retina de rata [J]. Journal of Practical Medicine, 2011, 27 (9): 1548-1550.
[38] Ma Lanqing, Dong Xiangqian, Liang Bing, et al. Efectos del ginsenósido Rg1 sobre la ultraestructura de hepatocien hígados fibróticos y su expresión de inhibititide metaloproteinasas-1 [J]. Chinese Journal of Hepatology, 2010, 18 (4): 304-306.
[39] Ma Yongjie, Zhu Dan, Zhong Zhi, et al. Efecto protector de la compatibilidad de ginsenósido Rg1 y tanshinona 1I A en cardiomiocilehipooxigenreoxigen[J]. Journal of the Academy of Military Medical Sciences, 2010, 34 (3): 243-246.
[40] Zhao Baosheng, Gui Haishui, Xu Tunhai. Estudio Experimental sobre el efecto antiinflamatorio del ginsenósido Rg1 [J]. Ginseng Research, 2010 (4): 2-4.
[41] Chu Xiuling, Su Jianqing, Wei Xubin, et al. In vivo anti-Marek& (en inglés)#Efecto del virus 39;s del ginsenósido Rg3 [J]. Hubei Agricultural Science, 2010, 49 (1): 143-146.
[42] Zhao Ziran, Liu Hesong, Zhang Kejia, et al. Ensayo túnel del efecto de ginsenósido Rg3 (GS-Rg3) en la apoptosis de células fibroblásticas de conejo [J]. Chinese Journal of Experimental Diagnostics, 2010, 14 (10): 1551-1553.
[43] Wang Zhenhua, Zhao Weiping, Liu Qing, et al. Efecto protector del ginsenósido Rh2 sobre el daño por radiación de rayos x en ratones [J]. Chinese Journal of Radiation Medicine and Protection, 2010, 30 (2): 143-146.
[44] Cheng C, He Z, Wang H. avance de la investigación sobre los efectos de las células antitumorales del ginsenósido Rh2 [J]. Traffic Medicine, 2010, 24 (1): 23-28.
[45] Zhang D, Yang B, Wu L, et al. Investigación sobre la protección de los ginsenósidos contra el daño oxidativo en células espermatogoniales de ratón [J]. Chinese Pharmacology Bulletin, 2010, 26 (8): 1014-1016.
[46] Zhang Fengpu. Investigación sobre el mecanismo de acción de los ginsenósidos [J]. Clinical Rational Drug Use, 2010, 3 (21): 158.
[47] Meng Fanli, Su Xiaotian, Liu Fugui, et al. The inhibiteffect of ginsenoside on aldose reductase [J]. Chinese Pharmacology Bulletin, 2011, 27 (6): 827-830.
[48] Zuo Rui, Luo Chunmei. El mecanismo de los ginsenósidos en anti-depresión [J]. Chinese Medicine Information, 2010, 2 (17): 156.
[49] Zhang Yixuan, Chen Xiaoying, Zhao Wenqian. Progreso de la investigación en la biotransformación de los ginsenósidos [J]. Journal of Shenyang Pharmaceutical University, 2008, 25 (5): 420-421.
[50] Zhao Ying, Yu Fulai, Zhang Guiying, et al. Efectos antitumorales de los ginsenósido Rb1 y clematoside [J]. Journal of Jilin Agricultural University, 2010, 32 (6): 654-656, 660.
[51] Liao Yilin, Zhang Jianping, Sun Xinming. Las saponinas Ginseng inducla diferenciación de las células de glioma C6 de rata [J]. Journal of Anatomy, 2010, 33 (2): 207-209.
[52] Liu Hanqing, Chen Fangfang, Miao Ningshu, et al. Estudio sobre la toxicidad aguda del ginsenósido C-K y su papel en causar edema pulmonar [J]. Journal of Yantai University, 2011, 24 (1): 59-63.
[53] Zhou M, Yang B, Jiang R, et al. Ginsenósido Rg1 retrasla senescencia de células madre hematopoyéticas y su mecanismo relacionado [J]. Chinese Medical Journal, 2010, 90(48): 3421-3425.
[54] Liu Xia, Bao Cuifen, Wei Jia, et al. Efecto protector y mecanismo de ginsenósido Rg1 sobre neuronen la región CA1 del hipocampo de ratas con isquemia cerebral y reperfusión [J]. Progress in Anatomy Sciences, 2010, 16(2): 177-180.
[55] Du Lijuan, Yao Yuhong, Fu Kui. Efectos del ginsenósido Rg3 sobre la expresión del gen ID-1 en tejidos de endometriosis [J]. Chinese Medicine and Clinical, 2010, 10 (6): 655-656.


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés