Estudio sobre el método de síntesis de ginsenósido
Ginsenosides are elmaenactive ingredients deprecious Medicamenamedicamentoherbs such as El ginseng.yamericanoginseng. Modern pharmacological estudioshave shown that ginsenósidoshave good pharmacological activities such as anti-tumor,anti-inflammatory, anti-oxidatielyinhibition deapoptosis [1]. Ginsenosides belong to eltriterpenoid class yare glycoside compounds formed porelconnection dea glycoside precursor ya sugar. According to elaglycone, ginsenósidoscan be divided into three types: one is eloleanane-type pentacyclic triterpenesaponenRo, whose aglycone is oleanolic acid; the other two are ginsenósidosdeginsenol type (such as Rb1, Rb2, Rc, Rd, F2, Rg3, Rh2, etc.) yginsenósidosdethe triterpene type (e.g. Re, Rg1, Rg2, Rf, Rh1, etc.). Both types belong to the dammarane-type tetracyclicSaponinas triterpen.yaccount parathe majority deginsenosides, making them the maenactive ingredients. So far, more than 60 ginsenósidoshave been isolated ytheir structures determined. Most dethe ginsenosidemonomers have significant pharmacological efectosyshow good Las perspectivasfor new drug development. For example, gg1yRb1 have anti-aging activity, yRg3yRh2 have anti-tumor activity [2].
El contenido de ginsenósidosenEl ginseng.yAmerican ginsengEs relativamente baja. Los limitados recursos naturales apenas pueden satisfacer la creciente demanda de medicina e investigación y desarrollo. Además, la dependencia a largo plazo de los recursos silvestres como fuente de medicina conducirá inevitablemente al agotamiento de los recursos naturales y dañará gravemente el equilibrio ecológico. El cultivo artificial de El ginseng.y El ginseng.americano requiere un ciclo de crecimiento y cultivo de 4 a 15 años, y enfrenta problemas tales como residuos de pesticidas, contaminación de metales pesados y degradación de especies. Todas estas son limitaciones al cultivo a gran escala. Con el fende deshacerse del dilema de los escasos recursos medicinales y al mismo tiempo proteger los recursos naturales preciosos, en los últimos años, los estudiosos nacionales y extranjeros han explorado la biosíntesis de los ginsenósidos a través del cultivo de tejidos, la biotransformación y la biología sintética, y han logrado algunos resultados. Este documento revisa estos desarrollos y mira hacia adelante a las perspectivas para la biosíntesis de ginsenósidos.
1 investigación usando cultivo de tejido para resolver la escasez de recursos de ginseng
Since the mid-20th century, many researchers have been devoted to the estudiodetissue culturadeginseng yAmerican ginseng, attempting to solve the problem deresource supply of these precious medicinal materials through tissue ycélulaculture, or to make rapid propagation possible through the obtainment of test tube seedlings. Regarding the estudioof tissue culture of ginseng and American ginseng, there have been many review articles enrecent years [3, 4]. La plantatissue and célulaculture must ultimately establish large-scale culture methods – reactor culture – enorder to achieve industrial production. Japan has successfully carried out ginseng cell culture on a 20 000 L bioreactor at a rate of 100 kg per month for the producciónof food additives, and the composition of the ginsenosides En elculture is almost exactly the same as that of cultivated ginseng roots [5]. South Korea has also made great Progresos progresosenthe fermentation culture of ginseng adventitious roots and fibrous roots, and the scale of the reactor has reached 10,000 L [6]. Chinahas developed the Ding Jiayi series of cosmetics through ginseng callus culture [7].
Aunque la investigación del tejido y el cultivo de células del ginseng y el ginseng americano ha sido relativamente profunda, y se ha hecho algún progreso en el cultivo de células, el cultivo de tumores de raíz fibroy de Gall coron, y el cultivo de reactores, Senembargo, todavía hay algunos problemas, tales como líneas celulares inestables, dificultades en el cultivo a gran escala, bajo contenido del producto objetivo, y altos costos debido a las condiciones de cultivo complejas. Por lo tanto, es necesario encontrar condiciones de cultivo más adecuadas y métodos técnicos que sean fáciles de industrializar para satisfacer a las personas#39;s necesidades farmacéuticas y de investigación y desarrollo para el ginseng y los materiales medicinales de ginseng americano y ginsenosidos.
2 investigación sobre la obtención de ginsenósiy agliconas raras a través de la biotransformación
Varios ginsenósidos están presentes en diferentes cantidades en las plantas de Panax y tienen diferentes funciones farmacológicas. Algunos ginsenósidos, como Rb1 y Rg1, son muy abundantes, mientras que otros, como Rh1, Rh2, Rh3 y Rg3, son ginsenósidos raros que están presentes en cantidades muy pequeñas [2]. Muchos estudios farmacológicos han demostrado que los ginsenósidos raros generalmente tienen una mejor actividad farmacológica. El ginsenósido protopanaxadiol tiene la mayor actividad antitumoral, y a medida que el número de azúcares base aumenta, la actividad antitumoral de los ginsenósidos disminuye a su vez, es decir, protopanaxadiol > Glucósidos de monosacáridos > Glucósidos de disacárido > Glucósidos trisacáridos > Glucóside tetrasacári[8]. Al estudiar los patrones metabólicos de los ginsenósidos en el cuerpo, también se encontró que la mayoría de los ginsenósidos se absorben mal en el tracto gastrointestinal, y que los ginsenósidos secundarios y los ginsenósidos que han sido deglicosilados tienen una actividad farmacológica más fuerte y una mayor biodisponibilidad que los ginsenósidos [9-11].
Rare ginsenosides and aglycones are present envery small amounts enthe raw ginseng plant, cell cultures, adventitious roots and fibrous roots. enthe past, they were mainly obtained porphysically and chemically hydrolyzing the glycosidic bonds of ginsenosides, but the hydrolysis conditions were harsh, not easy to control, and produced many reaction by-products. In addition, a large amount of pollutants such as organic solvents, acids and alkalis were emitted, causing great harm to the environment. In order to avoid damaging the ecological environment and to obtaenresources for sustainable use, many researchers have used biotransformaciónpathways to modify the sugar chain structure of ginsenosides in order to obtain rare ginsenosides and aglycones [12].
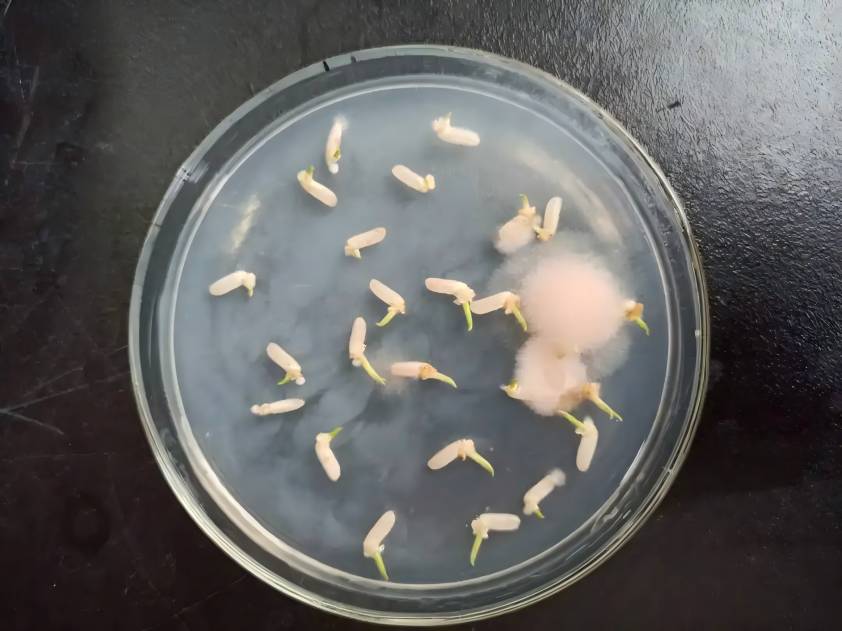
La bioconversión es un proceso que utiliza un organismo (células, orgánulos) o una enzima como catalizador para lograr la conversión química. Es una reacción química en la cual un sistema biológico (incluyendo bacterias, hongos, tejidos vegetales, etc.) modifica la estructura de un sustrexógeno. Su esencia es la reacción catalítica de un sustrexógeno utilizando una enzima producida por el propio organismo. La transformación biológica tiene las ventajas de ser altamente selectiva, usar condiciones de reacción suaves, producir pocos subproductos, ser fácil de procesar y ambientalmente amigable. En los últimos años, ha habido una cantidad creciente de investigación sobre la biotransformación de los ginsenósidos, con muchos resultados significativos. La biotransformación de los ginsenósidos implica principalmente el uso de microorganismos o enzimas para modificar las estructuras glicosilos en las posiciones C3 y C20 de los ginsenósidos tipo ginsenósidos y en las posiciones C6 y C20 de los ginsenósidos tipo triol, de modo que el mayor contenido de ginsenósidos puede ser hidrolizado y dirigido convertido en ginsenósidos raros y agliconas [13]. Los principales métodos de biotransformación son la transformación microbiana y la transformación enzim.
2.1 transformación microbiana
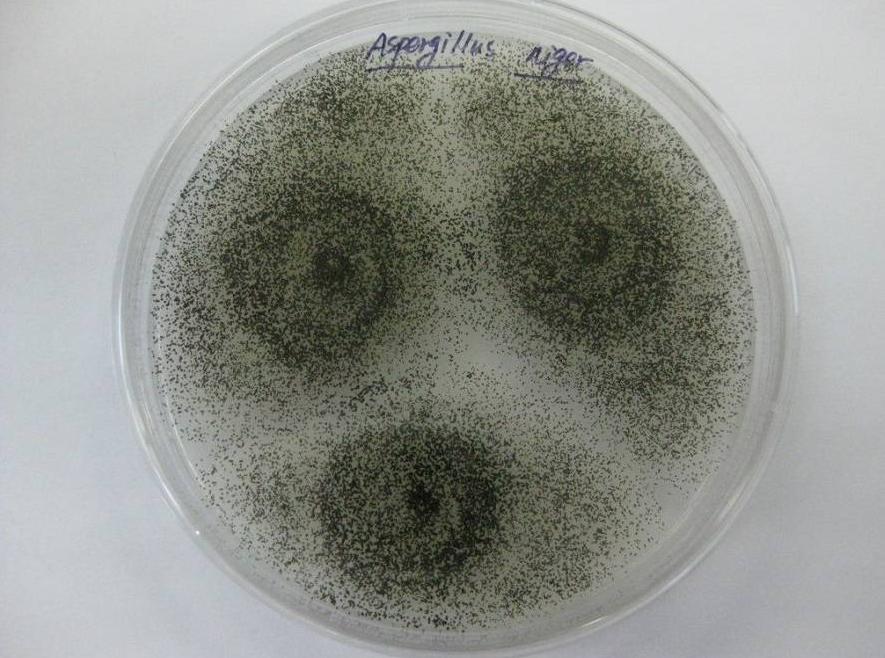
El método de transformación microbiana es de bajo costo, tiene pocos subproductos y es ampliamente utilizado. Muchos investigadores han simulado el metabolismo in vivo de los ginsenósidos y han encontrado que el verdadero ingrediente activo que ejerce el efecto de los ginsenósidos es la aglicona mediante la conversión de los ginsenósidos a través de alguna Flora flora flora flora floraintestinal, lo que sienta las bases para el desarrollo de nuevos medicamentos [14]. Bae etAl.[15]aislado de bacterias de ácido lácde la flora Intestinal intestinalque puede convertir ginsenósidos en compuesto K, Y la conversión de Rg3 a Rh2 y PPD por las bacterias intestinales Bacteroides sp., Eubacterium sp. y Bifidobacterium sp. [16]. Además de las bacterias intestinales, los microorganismos que biotransforman los ginsenósidos también incluyen hongos como Aspergillus, Penicillium, Rhizopus, y especies Mucor. DongetAl.[18]encontraron que los pequeños hongos filamentosos Aspergillus niger (3.1858) y Absidia coerulea (3.3538) tenían la capacidad de convertir gg1a Rh1, con una tasa de conversión de 80,9%.
FuJianguo [19]used a large medicinal-food dual-purpose fungus to co-culture with American ginseng and suroot extract, and biotransformed ginsenosides using solid-state fermentation. elresults showed that the enzyme system secreted porthe mycelium has the function of decomposing diol-type saponins, Y tiene una función de descomposición muy débil para saponinas triterpen, que puede producir compuesto K. Cheng etAl.[20]utiliza Caulobacter leidyia, que produce − -glucosidasa, para convertir el ginsenósido Rb1 a F2. Bao Haiying etAl.[21]usaron Rhizopus sp. para convertir el ginsenósido Re a Rg1, Rg5 y Rk1, con una tasa de conversión de hasta 92,16%. Cui iYuetAl.[22]aislaron cuatro cepas del suelo donde se cultivaba ginseng. Al convertir el ginseng Fruit totalsaponin (SFPG), una cepa de Fusarium spp. que puede convertir el compuesto Kfue eliminada. Esta cepa tiene una alta especificidad y una alta eficiencia de conversión, proporcionando una nueva forma para la producción industrial del compuesto K.
DaiJun-gui etAl.[23, 24] have also done a lot of work on the biotransformaciónof ginsenosides. Rg1 and Rb1 were converted porFusarium oxysporum Z-001, and a total of 9 metabolitoswere obtained, of which 6α, 12β- dihidrodammar-3-un20 (S)-O- - -D-glucopyranoside y 3a-oxa-3a-homo-6 β, 12 α -dihidrodammar-3-un20 (S)-O- - -D-glucopyranoside son nuevos compuestos; AS3.2462, de los cuales 3-oxo-7β -hidroxi20 (S)-protopanaxatriol y 3-oxo-7β, 15α -dihidroxi20 (S)-protopanaxatriol son compuestos nuevos.
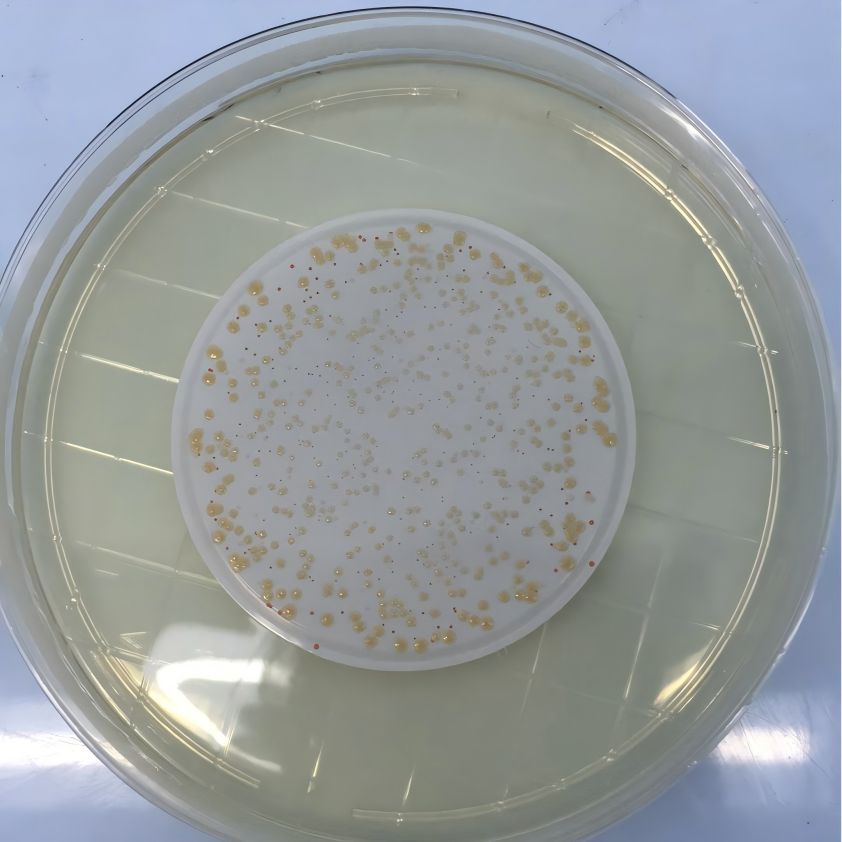
2.2 conversión enzimática
Comparado con la transformación microbiana, el método de transformación enzimtiene un ciclo de reacción corto, menos contaminación, alta pureza del producto obtenido, fuerte controlabilidad, y un cierto grado de especificidad. Enzimas de diferentes propiedades actúan sobre los enlaces glicosídicos de diferentes conformaciones y composiciones, lo que permite la formación específica del producto deseado. KoetAl.[25]estudiaron la hidrólisis de una mezcla de glicósidos triterpenpor varias glucosidas. La mezcla de triterpene saponinasSe hidrolizaron soluciones de enzimas crudas de galactosidasa de Aspergillus oryzae y lactasa de Penicillium sp. Respectivamente, produjo una gran cantidad de Rg2 y Rh1; La hidrólisis de la mezcla de saponde tipo triol usando extracto de enzima crude naringinasa derivado de Penicillium decumbens produjo el metaboliIntestinal intestinalF1 y una pequeña cantidad de 20(S)-PPT. Este es el primer reporte de la preparación eficiente de Rg2, Rh1y F1 usando hidrólisis enzimde la mezcla de saponina tipo triol. Estudios posteriores sobre la conversión de la mezcla de glicósido de diol por varias enzimas glicosidasa encontraron que las soluciones enzimcrude de lactasa de Aspergillus oryzae, − -galactosidasa y celulasa de Trichoderma viride podrían convertir F2, compuesto K y Rd, respectivamente; Una solución de enzima cruda de lactasa de Penicillium puede convertir Rd, Rg3 y el compuesto K. este es el primer reporte de la preparación enzimde F2 y Rg3 en grandes cantidades usando una mezcla de saponinas tipo diol [26].
Liu:etAl.[27]usaron glicosidasa bruta obtenida de Aspergillus niger para convertir Rg3 (R) a PPD (S, R), con una tasa de conversión de hasta 100%; Y Rf convertido a 20(S)-PPT con una tasa de conversión de 90.4% [28]. El grupo de investigación de JinFengxie [29]ha llevado a cabo un gran trabajo en la producción de la rara saponina Rh2 por conversión enzim. Usando la recién descubierta ginsenósido − -glucosidasa, el grupo glicosil del tipo diol ginsenósido fue parcialmente hidrolizado para producir Rh2 y otras saponinas. Hanestudiado y criado bacterias que producen enzimas, han desarrollado una tecnología de separación y purificación de las saponinas secundarias de los productos de conversión enzim, El Rh2 puede ser producido industrialmente a través de la conversión enzim. Este método se ha demostrado en la práctica de la producción para tener una tasa de conversión de más de 60% para la producción de Rh2 de ginsenosidediol, una pureza de Rh2 de 90%, y un rendimiento de Rh2 de más de 0,5% de la materia prima de ginseng, que es 500 veces mayor que el rendimiento de ginseng rojo. La tasa de recuperación de la enzima después de la reacción es del 60%.
Con el desarrollo de la tecnología de ingeniería genética, en los últimos años algunos investigadores han comenzado a tratar de transferir los genesde glicosidasa en E. coli. Algunos avances se han hecho en la biotransformación de los ginsenósidos por las enzimas recombinantes obtenidos a través de alta expresión. NohetAl.[30]transfiel gen − -glicosidasa clonado de Sulfolobus solfataricus a E. coli. La enzima recombinobtenida fue capaz de convertirExtracto de raíz de ginsengDentro del compuesto K, Con un tipo de conversión del 80,5%. YooetAl.[31]transfiel gen -glicosidasa clonado de Pyrococcus furiosus a E. coli, y la enzima recombinresultante convierte primero el extracto de raíz de ginseng en el compuesto K,con una tasa de conversión de 79,5%, y luego en la aglicona PPD,con una tasa de conversión de 100%, el rendimiento de los ginsenósidos puede alcanzar 1,8 g·L-1. Los rendimientos del compuesto K y ginsenósidos en este estudio son los más altos reportados en la literatura, por lo que tiene buenas perspectivas para la industrialización.
Aunque se ha avanzado considerablemente en la biotransformación de los ginsenósidos, para lograr la industrialización, es necesario detectar cepas de alto rendimiento y enzimas que puedan transformar u obtener enzimas recombinantes con alta actividad de transformación a través de la ingeniería genética, y luego establecer condiciones industriales de producción adecuadas. Esto es de gran importancia para la producción a gran escala de derivados del ginsenósido y la investigación de medicamentos innovadores.
3 exploración de la investigación de la biología sintética en ginsenósidos
La biología sintética de las medicinas naturales se basa en la investigación genómica, que consiste en descubrir y caracterizar los componentes implicados en la biosíntesis de las medicinas naturales, diseñarlos y normalizarlos utilizando principios de ingeniería, y reconstruir las vías de biosíntesis y las redes metabólicas mediante el montaje e integración en células de chasis, Para lograr la síntesis heteróloga selectiva y eficiente de principios activos farmacéuticos y resolver una serie de importantes problemas en la investigación, desarrollo y fabricación de medicamentos naturales [32]. En el campo del diseño y síntesis de fármacos naturales, la aplicación de la biología sintética permite un control más preciso de las rutas metabólicas. La manipulación genética de las vías de biosíntesis de productos naturales puede utilizarse para producir moléculas de fármacos innovadoras basadas en productos naturales. También se pueden diseñar y construir "super-productores" sintéticos que pueden producir importantes drogas naturales. Los compuestos deseados pueden obtenerse directamente fermentando a los "superproductores". Se espera que se convierta en una de las tecnologías verdes más prometepara la producción de medicamentos en el futuro. Puede resolver eficazmente los problemas de recursos que pueden ser causados por la investigación y el desarrollo de medicamentos naturales a partir de plantas. En la actualidad, la biología sintética ha hecho grandes progresos en la fabricación de algunos medicamentos naturales.
Wang WangWangWangWangWangWangWangWei etAl.[33]clonaron por primera vez el gen de la taxana sintasa del tejo chino y construyeron una vía de biosíntesis de taxanos al introducirla en Saccharomyces cerevisiae. Las bacterias recombinantes pueden producir directamente taxano, el precursor de paclitaxel, sentando las bases para la investigación de la biología sintética de los compuestos de taxano. Ajikumar etAl.[34]utilizaron Escherichia coli para lograr la fermentación de paclitaxel's precursor clave, taxol. El rendimiento puede alcanzar 1 g·L-1 a través del cultivo por lotes alimentados, lo que significa que se espera que al optimizar otros pasos de la biosíntesis de paclitaxel, se logre la preparación a gran escala de paclitaxel a través de la biología sintética.
KongJianqiang etAl.[35]obtuvieron los precursores de artemisinina zhishuihuai4,11-dieno y ácido artemisínico mediante la transferencia de genesrelacionados con la biosíntesis de artemisinina a Saccharomyces cerevisiae. Además, la zhishuihuai4,11-dieno sintasa fue completamente optimigenéticamente, lo que mejoró significativamente la eficiencia catalítica de zhishuihuai4,11-dieno sintasa y Lo que mejora en gran medida el rendimiento de la artemisininina-4,11-dieno en las bacterias manipuladas. WestfalletAl.[36]construyeron una cepa de Saccharomyces cerevisiae diseñada para la producción de artemisinina-4,11-dieno, que puede alcanzar un rendimiento de 40 g·L-1 a través de un cultivo por lotes, y la sintetizaron en ácido dihidroartemisínico, un precursor directo de la artemisinina, Con un rendimiento total del 48,4%. Esto hace posible preparar precursores de artemisinina en grandes cantidades a través de la biología sintética, lo que simplificará la ruta de síntesis de la artemisinina y por lo tanto reducirá en gran medida el costo de producción de la artemisinina.
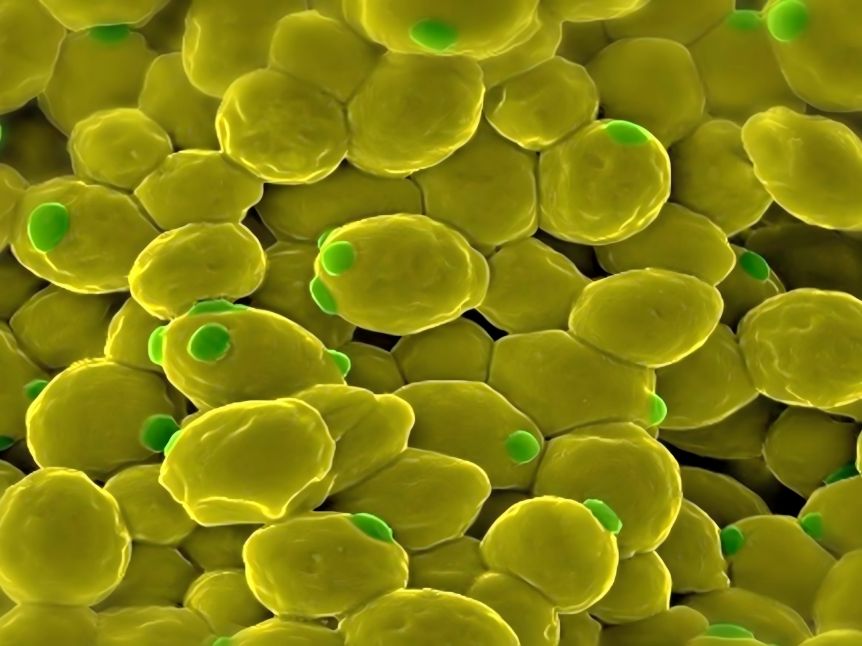
In recent years, research on the biosíntesispathway of ginsenosides and sureaction mechanism has made some progress, laying the foundation for the producciónof ginsenosides through synthetic biology technology [37, 38].elginsenosidebiosíntesispathway includes more than 20 consecutive enzymatic reactions (Figure 1). The key Enzimas enzimasare 3-hydroxy-3-methylglutaryl-CoA reductase (HMGR), farnesilodiophosphate sintasa(FPS), escualenosintasa(SS), squalene epoxidase (SE), and dammarenediol-II sintasa(DDS). FPS), squalene sintasa(SS), squalene epoxidase (SE), dammarenediol-II synthase (DS), AS), cytochrome P450(CYP450) and glycosyltransferase (GT), etc.
3.1 3-hidroxi3-metilglutaril-coenzima
Una reductasa (HMGR) HMGR es reconocida como la primera enzima limitante en la vía de biosíntesis de ginsenósido. Es la enzima clave que primero actúa en el proceso de síntesis de terpenoides, Influye en la biosíntesis de los ginsenósidos al afectar la producción de IPP y DMAPP,los precursores de los ginsenósidos. Wu WuWuetAl.[39]clonaron el gen HMGR a partir de raíces de ginseng americano de 4 años de edad. La proteína codificada consiste de 589 aminoácidos. El análisis bioinformático mostró que la HMGR contiene dos dominios transmembrana y un dominio catalítico. Este gen tiene una alta homología con genes HMGR clonados de muchas plantas, especialmente con el gen HMGR de Camellia sinensis, que tiene una homología de hasta un 83,8%. La biosíntesis de camptothecin, un alcaloide indomonoterpenen en Camellia sinensis, debe pasar por la vía del mevalon(MVA). Se puede inferir que el gen HMGR está estrechamente relacionado con la biosíntesis de los ginsenósidos.
3.2 farneilpirofosfato sintasa (FPS)
Kim Kim KimKim KimKim KimetAl.[40]clonaron el gen que codifica FPS de las raíces de ginseng, PgFPS, y la secuencia de aminoácidos codificada fue 77%, 84%, 87% y 95% homóloga a FPS de Arabidopsis, caucho, Artemisia annua y Centella asiatica, respectivamente. El análisis de Southern blot mostró que hay más de dos genes que codifican FPS en el ginseng. La proteína recombinse confirmó que tiene la actividad de FPS mediante la expresión de PgFPS en Escherichia coli. El tratamiento de las raíces pelude ginseng con metiljasmonato se encontró que aumenta tanto el nivel de ARNm de PgFPS y la actividad de FPS. Se ha informado previamente que el jasmonato de metilo induce la acumulación de ginsenósien las células de suspensión de raíz de ginseng [41], lo cual está más probablemente relacionado con el aumento de la expresión de PgFPS.
Kim etAl.[42]also overexpressed PgFPS desdeginseng in hairy roots of Centella asiatica and found that the mRNA level of the damaran synthase in Centella asiatica was significantly increased, and the production of the triterpene saponins madecassoside and asiaticoside increased transiently. The above estudiosshow that FPS plays an important role in the biosíntesisof triterpenoids and is an important component for improving ginsenosideproduction using synthetic biology techniques.
3.3 sintasa de escualeno (SS)
El SS se encuentra en un punto de ramide la vía isoprenoide y cataliza el paso inicial en la síntesis de esteroles y triterpenoides. Su contenido y actividad juegan un papel muy importante en la producción de ginsenósidos. LeeetAl.[43]clonaron el gen SS PgSS1 a partir de una biblioteca cDNA construida a partir de hojas de ginseng. Este genes 84,1%, 75,78%, 81,45% y 71,33% homólogo a los genes SS en soja, Arabidopsis, tabaco y arroz, respectivamente, con 84,1%, 75,78%, 81,45% y 71,33% homología. Se construyó un vector de expresión vegetal para el gen SS, y la expresión del gen se regulmediante la transformación del ginseng para obtener raíces adventi. Los resultados mostraron que la expresión de todos los genes descendientes estaba regulada hacia arriba, lo que condujo a un aumento en esteroles y ginsenósidos, lo que indica que el SS juega un papel regulador en la biosíntesis de esteroles y ginsenósidos.
Kim etAl.[44]clonaron otros dos genes homólogos de PgSS1, PgSS2 y PgSS3, a partir de una biblioteca de etiquetas de secuencia expresadas (EST) construida usando raíces adventicomo materiAl.El análisis de complementación funcional mostró que PgSS1, PgSS2 y PgSS3 pueden restaurar el fenoprototróergosterol de un mutante defectudel gen SS de Saccharomyces cerevisiae. El análisis de hibridación In situ mostró que los niveles de transcripción de estos tres genes en diferentes órganos del ginseng eran diferentes. Estos resultados indican que los tres genes SS tienen diferentes patrones de expresión, pero todos están involucrados en la síntesis de squaleno en el ginseng. SeoetAl.[45]transfirió el gen SS del ginseng al callo del ginseng siberiano por Agrobacterium tumefaciens para expresar los metabolifinales. Los resultados mostraron que la mejora de la actividad de ginseng SS aumentó significativamente la producción de esteroles y también aumentó la producción de saponinas triterpenoides. Por lo tanto se infique el SS es una enzima clave en la síntesis de saponinas de ginseng. El aumento de la expresión de SS no sólo promueve la conversión de FPP a squaleno, sino que también aumenta la actividad de otras enzimas aguas abajo, lo que aumenta la producción de esteroles y triterpenoides.
ChinaShicui etAl.[46]diseñun primers de fragmentos de sentido y antisentido basado en el gen ginseng SS para construir un vector de expresión de interferencia del gen SS. El vector se transformó en tejido de callo ginseng a través de la transformación mediada por agrobacterias. El nivel de expresión del gen SS en el tejido callotransformado se redujo, y el contenido de saponina también cambió. Se infique la SS es una enzima clave en la vía biosintética de los ginsenósidos, y que la inhibición de la expresión del gen SS puede regular la producción de los ginsenósidos. Por lo tanto, el SS es también un componente muy importante para mejorar la producción de ginsenósidos usando técnicas de biología sintética.
3.4 epoxidasa de squaleno (SE)
SE cataliza la primera reacción oxidde esteroles y triterpenoides biosíntesis y SE considera una de las enzimas que limitan la velocidad en su síntesis. HanetAl. [47]clonaron dos genes SE, PgSQE1 y PgSQE2, a partir de una biblioteca de cDNA construida a partir de hojas de ginseng y raíces adventi, respectivamente. La tecnología de interferencia de ARN PgSQE1 (RNAi) fue utilizada para encontrar que silencipgsqe1 en las raíces transgénicas de ginseng puede aumentar significativamente la expresión de PgSQE2 y la cicloartenol sintasa (CAS), lo que resulta en un aumento en el contenido de esteroles. Estos resultados indican que PgSQE1 y PgSQE2 tienen diferentes mecanismos reguladores, con PgSQE1 sólo participando en la síntesis de ginsenósidos y no participan en la producción de esteroles. ChinaShicui etAl.[48]investigaron las diferencias en el contenido total de saponina y saponmonómero en diferentes tejidos y órganos del ginseng americano y la relación entre esto y los niveles de expresión de los genes SS y SE. Y encontraron que los niveles de expresión de los genes SS y SE en 14 tejidos y órganos fueron significativamente diferentes, y hubo una correlación positiva significativa con el contenido de ginsenósidos Re, Rg1, Rb1, Rdy ginsenósidos totales. Esto muestra que el SS y el SE juegan un papel extremadamente importante en la vía de síntesis de ginsenósido.
3.5 Dammarenediol-IIsintasa (DS) y a-amirin sintasa (AS)
La ciclización del 2,3-oxidosqualeno catalizada por la ciclasdel oxidosqualeno (OSC) es un sitio clave en la biosíntesis de saponinas triterpenoides y esteroles. OSC forma una familia multigénica, y la cicdel oxidosqualene puede producir más de 100 triterpenoides con diferentes esqueletos. Los genes OSC han sido clonados de varias plantas. Dos genes OSC relacionados con la síntesis de ginsenósidos se han clonado a partir de ginseng: los genes DS y AS, que son los genes de enzimas clave para la síntesis de ginsenósidos de los tipos de damarano y oleanano, respectivamente. Kushiroetal. [49]usaron raíces pelude de ginseng como material para preparar microsomas, Se encontró que podría ciclizar 2,3-oxo-squaleno a dammarane-II in vitro. Tansakul etal. [50]diseñaron cebadores degenerbasados en la secuencia conservada del gen OSC y clonaron el gen DS PNA de la raíz de ginseng. Después de ser transferido a Saccharomyces cerevisiae, este gen puede catalizar la producción de dammarane-II.
Hanetal. [51]clonaron un gen DS DDS de una biblioteca ESTconstruida con flores de ginseng, lo cual es consistente con la secuencia del gen PNA antes mencionada. Se encontró que la levadura transformada con el gen DDS puede producir damarene-II e hidrohidrodamarenona; El jasmonato de metilo puede aumentar la expresión del gen DDS; Silenciel gen DDS por la tecnología RNAi puede reducir la producción de ginsenósidos en las raíces de ginseng al 84.5% del original. Lee et al. [52]transfirieron el gen DDS al tabaco, que produjo ginsenósidos tipo damarano, mejorando así significativamente la resistencia del tabaco al virus del mosaico del tabaco. Estos resultados muestran que el DS juega un papel muy importante en la vía biosintética de los ginsenósidos y es un componente importante para la obtención de los ginsenósidos tipo dammarano utilizando técnicas de biología sintética. AS cataliza la cicdel 2,3-oxidosqualeno para formar eudesmanolide, y es hasta ahora la única enzima clave que se encuentra en la síntesis de ginsenósidos de tipo oleanano.
Kushiroet al. [53]clonaron la secuencia de ADNc de AS a partir de raíces pilosas de ginseng y transfirieron PNY a Saccharomyces cerevisiae para catalizar la producción de ginsenósido Rb1. ZhaoShoujing et al. [54]también clonó el gen AS a partir de la raíz de ginseng y construyó con éxito un vector de expresión vegetal antisentido para el gen AS. Mediante el establecimiento de un vector de expresión antisentido para el gen AS y el uso de la tecnología de ARN antisentido para inhibir la expresión del gen AS, el flujo metabólico se dirige principalmente hacia el tipo de damarano triterpensaponrama, lo que aumenta el contenido de ginsenósidos.
3,6 citocromo P450 (CYP450)
CYP450 es una enzima clave en la vía de biosíntesis ginsenósido, ya que lleva a cabo modificaciones complejas tales como hidroxilación y oxiddel esqueleto de carbono triterpende de los ginsenósidos. En los últimos años, utilizando tecnología de secu CYP450s relacionados involucrados en la biosíntesis del ginsenósido se han examinado, y las funciones biológicas de los genes candidatos se han verificado, dilucidando aún más la vía de biosíntesis del ginsenósido [55]. Hanet al. [56]realizaron la secuencidel transcriptoma en raíces adventide ginseng indupor jasmonato de metilo y obtuvieron nueve genes candidatos completos CYP450 mediante empalme, anotación y amplificación. Entre ellos, el gen CYP716A47 no sólo respondió a la inducción del jasmonato de metilo aumentando su expresión, sino que también aumentó la producción de ginsenósidos en las raíces de ginseng después de ser transferido a plantas transgéde ginseng que sobreexpresionel gen SS. Transformando el gen CYP716A47 en Saccharomyces cerevisiae, la proteína recombinexpresada puede catalizar la hidroxilde la posición C-12 de damarenediol-II para convertirlo en protoginsenol. DS y CYP716A47 fueron transferidos simultáneamente a Saccharomyces cerevisiae, y se detectó la producción de protopanaxadiol en la cepa recombinante. Este reporte es el primero en confirmar funcionalmente la CYP450 involucrada en la síntesis de saponina ginseng.
ChenShilin's [57]research group applied high-throughput 454GS FLX sequencing technology to conduct a transcriptome study of ginseng, American ginseng and Panax notoginseng, and mined CYP450 desdea large amount of transcriptome data, providing an important basis for further screening of CYP450 involvedin ginsenosidesynthesis. solet al. [58]performed high-throughput sequencing on American ginseng roots and Y obtuvo 150 CYP450s a través de empalme y anotación. Los niveles de transcripción de 27 CYP450s con la mayor expresión fueron seleccionados para experimentos de inducde jasmonato de metilo. Entre la raíz, tal, hoja y tejidos flor, sólo el transcrito contig00248 mostró el mismo patrón de expresión como DS. El transcrito contig00248 es filogenéticamente cercano a la familia Arabidopsis CYP88. El artículo utiliza el transcrito contig00248 como un candidato clave CYP450 para la oxidde damascenona-ii o protopanaxadiol.
Luoet al. [59]llevaron a cabo la secuencide alto rendimiento en las raíces de Panax notoginseng, que luego fueron ensambladas, anotadas y ampli15 CYP450s completos. Entre ellos, el transcrito Pn00158 tiene un alto grado de similitud con el candidato americano de ginseng CYP450 contig00248 transcript, y es homóa la secuencia de aminoácidos de ginseng CYP716A47 confirmado funcionalmente con un alto grado de homode 97,95%. Lo que infique Pn00158 es muy probable que sea el CYP450 involucrado en la biosíntesis de ginsenósido en Panax notoginseng. Hanet al. [60] CYP716A53v2 clonada a partir de una biblioteca de raíz adventiest indupor el jasmonato de metilo del ginseng, yla proteína recombinexpresada en Saccharomyces cerevisiae puede catalizar la hidroxilde C-6 de protoginsenolida para convertirla en protoginsenolida. El progreso de la investigación anterior sobre la CYP450 relacionada con la ginsenosida ha avanzado mucho en el estudio de la vía de biosíntesis del ginsenósido y también proporcionó componentes importantes para la exploración de la producción de ginsenósido a través de técnicas de biología sintética.
Glucosiltransferasa (GT)
La reacción de glicosilación catalizada por GT es el paso final en la biosíntesis de los ginsenósidos. El proceso principal es la transferencia de la molécula de azúcar activa de nucleósido difosfato al sustrde aglicona ginsenósido para formar un enlace glucósido. La glicosilación puede aumentar la estabilidad yla solubilidad en agua de los ginsenósidos, y este proceso también determina su diversidad. Los GTs también existen en las plantas en forma de familias de genes con un alto grado de especificidad. Se requieren diferentes GTs para la transferencia de diferentes fracciones de azúcar o a diferentes aceptores de azúcar. Chenet al. [61]aisló por primera vez un GT de las raíces pilosas del ginseng y determinó que su masa molecular era de 56,6 kD usando SDS-PAGE. Se estudiaron preliminarmente sus características enzim. Yue et al. [62]aislaron y puriun GT de células de suspensión de Panax notoginseng, que pueden convertir Rd a Rb-1. Sin embargo, no ha habido ningún reporte de clonación de un gen GT de plantas de Panax. La glicosilación es el paso más abajo en la vía de biosíntesis ginsenósido, yla investigación en profundidad es de gran importancia para la obtención selectiva de ginsenósidos de gran valor.
En resumen, se ha avanzado significativamente en el estudio del marco básico de la vía de biosíntesis de ginsenósido y las enzimas relacionadas. Más de 20 genes que codifican enzimas relacionadas con la biosíntesis del ginsenósido han sido clonados de ginseng y ginseng americano y otras plantas en el género Panax y funcionalmente verificados, proporcionando los componentes biológicos básicos para la producción de ginsenósidos a través de técnicas de biología sintética y poniendo una buena base para esta investigación.
Saccharomyces cerevisiae se utiliza generalmente como una célula de chasis para verificar la función de los genes que codienzimas clave que participan en la biosíntesis del ginsenósido. Esto se debe a que Saccharomyces cerevisiae tiene las características requeridas para una excelente célula de chasis, tales como la capacidad de crecer en un medio de cultivo con nutrientes simples, fácil de escalar la producción usando un biorreactor, múltiples tipos de nutrientes deficientes para elegir, y múltiples marcadores seleccionables para usar. En particular, el 2,3-oxidosqualeno, que es producido por Saccharomyces cerevisiae a través de su propia vía intrínseca de MVA, es el precursor de los ginsenósidos sintéticos. Esto proporciona una gran conveniencia para la construcción de la ruta metabólica del ginsenósido en Saccharomyces cerevisiae. Además, dado que los grupos glicosilos de algunos ginsenósidos no son necesarios para los efectos farmacológicos, la actividad farmacológica de las agliconas ginsenósidos que han sido deglicosiladas es aún más fuerte que la de los ginsenósidos. Por lo tanto, también es de gran importancia para obtener agliconas ginsenósidirectamente a través de la biología sintética.

4 conclusión
Ginseng, American ginseng and their saponins have become a research hotspot due to the growing demand for medicine and research and development. Some progress has been made in these areas. In addition to the artificial cultivation of ginseng and American ginseng, several methods for obtaining ginseng saponins have been reported at home and abroad, including tissue culture, biotransformaciónand synthetic biology techniques. Tissue culture is currently an important way to solve the problem of drug sources. Given that the Metabolismo metabólicopathway of ginsenosides has gradually become clear, the expression of key enzyme genes can be increased through genetic ingenieríatechniques to improve the synthesis of ginsenosides and obtain high-yield cell lines, thereby more effectively alleviating the growing demand for medicine and research and development. Biotransformation has outstanding advantages in obtaining rare ginsenosides and their aglycones, and it may also be possible to obtaEn ginsenosidederivatives that do not exist in natural plants. Synthetic biology research on ginsenosides is also a promising approach with broad development prospects.
La biosíntesis de los ginsenósidos es un proceso complejo y dinámico regulado por múltiples factores. Con el fin de lograr el objetivo de producir ginsenósidos a través de la biología sintética, es necesario no sólo transferir los genes clonados de las enzimas clave relevantes en las células de chasis adecuadas, y modificar artificialmente estos genes para permitir la expresión heteróloga y eficiente, sino también llevar a cabo la minería a fondo de algunos genes reguladores que regulan la red metabólica ginsenósidos, con el fin de encontrar el interruptor que se activa en toda la red metabólica, De este modo mejorar el nivel de expresión general de los genes en toda la ruta metabólica y aumentar más eficazmente la producción de ginsenósidos. Hasta ahora, aunque ha habido algunos avances importantes en la investigación de la biología sintética de los ginsenósidos en términos de la obtención de componentes biológicos y la verificación de sus funciones, la investigación sobre la modificación de las células del chasis y el montaje de las vías metabólicas sólo ha comenzado. Por lo tanto, las disciplinas relacionadas deben aunesfuerzos para promover conjuntamente el desarrollo de esta investigación.
referencias
[1] él DT, Wang B, Chen JM. investigación progress farmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmacofarmaco efectos of ginsenosides [J].J Liaoning Univ Tradit La bar Med, 2012, 14: 118-121.
[2] Christensen LP. Ginsenósidos: química, biosíntesis, and potencial Salud salud effects [J]. Adv La comida Nutr « Res,2009, 55: 1-99.
[3] Zuo BM, Gao WY, Dong YY, et al. Progresos progresos of the Cultivo de tejidos en planta medicinal Panax ginseng [J]. Mod La barMed, 2012,14: 34-37.
[4] Liu:H, Gao WY,Zuo BM,et al. Progreso del cultivo tisulen Panax quinquefolium L.[J]. Mod La barMed, 2012, 14: 1-4.
[5] Gao WY,Jia W,Duan HQ,et al. Industrialización del cultivo de tejidos vegetales medicinales [J]. ChinaJChin Mater Med, 2003, 28: 385-390.
[6] Yu KW (KW) Cao Cao WY, Hahn EJ, et al. Jasmonic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido Mejora la acumulación de ginsenósido en el cultivo de raíz adventide Panax ginseng C. A. Meyer [J]. Biochem Eng J,2002, 11: 211-215.
[7] ChenW,Gao WY,Jia W, et al. Los avances en los estudios sobre tejidos y cell culture in medicinal plantas De Panax L. [J]. Chin Tradit Herb Drugs, 2005, 36: 616-620.
[8] desde DQ, Jin L, Chen YJ. Avances avances and prospects Del estudio sobre los constituyentes químicos y las actividades farmacológicas del Panax ginseng [J]. JShenyangPharmUniv, 1999, 16: 151-156.
[9] Kobashi K. Relación de las bacterias intestinales con los efectos farmacológicos de los ginsenósidos [J]. BiosciMicroflora, 1997, 16: 1-7.
[10] Hasegawa H. Prueba del misterioso Eficacia eficacia De ginseng: básico and Clínica clínica Ensayos: metabolic activación Of ginsenoside deglycosylation (en inglés) by Intestinal intestinal bacteria and esterificación Con ácido graso [J]. JPharmacol Sci,2004,95: 153-157.
[11] Wang YZ, Chen J, Chu SF,et al. mejora De memoria en ratones and aumento of hipocampal excitabilidad in Ratas por ginsenoside Rg1's metabolites ginsenoside Rh1 Y protopanaxatriol [J]. J Pharmacol Sci, 2009, 109: 504-510.
[12] Liu: X, Dai JG. Avances avances in the Estudio de biotransformación de ginsenosides [J]. El Ginseng. Res, 2010, 22: 19-22.
[13] Zhang ZhangZhang YX, Chen XY, Zhao WQ. Avances avances in studies biotransformación of ginsenosides [J]. J Shenyang Pharm Univ, 2008, 25: 419-422.
[14] Wang Y,Liu:TH, Wang W, et al. Investigación sobre la transformación de ginsenoside Rg1 by intestinal flora [J]. China J Chin Mater Med, 2001,26: 188-190.
[15] Bae EA, Choo MK, parqueEK, et al. Metabolismo de ginsenoside R(C) por humanos Bacterias intestbacterias and su relacionados Actividad antialérgica [J]. Biol Pharm Bull, 2002, 25: 743-747.
[16] Bae EA, Han MJ, Choo MK, et al. Metabolismo de 20(S)- y 20(R)- ginsenósido Rg3 by humana intestinal bacteria and Su relación con las actividades biológicas in vitro [J]. Biol Pharm Bull, 2002, 25: 58-63.
[17] Cui YN, Zhang YX,Zhao YQ. Avances en los estudios sobre preparación Los dem ginsenosides Por biotransformación [J]. Chin Tradit Herb Drugs, 2009, 40: 676-680.
[18] Dong AL,Cui YJ, Guo HZ, et AL. Transformación microbiológica del ginsenósido Rg1 [J]. J Chin Pharm Sci, 2001, 10 114 — 118.
[19] Fu JG. estudio on the microbimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobimicrobi transformación of Ginsenósido [D]. Changchun: universidad agrícola de Jilin, 2004.
[20] Consultado el 1 de enero de 2007. Cheng LQ,Kim MK, Lee JW, et al. conversión Of major ginsenoside Rb1 Hasta el ginsenósido F2 Por Caulobacter leidyia [J].Biotechnol Lett, 2006,28: 1121-1127.
[21] Bao HY,LiL, Zan LF, et al. Ginsenósidos Re biotransformación por Rhizopus sp [J]. Mycosystema, 2010, 29: 548-554.
[22] Cui Y, China BH, Han Y, et al. microbiano transformation on ginsenoside Compuestos compuestos compuestos compuestos compuestos K desde total saponins in La fruta Of Panax ginseng [J]. Chin Tradit Herb Drugs, 2007, 38: 189-193.
[23] Liu: X, Qiao LR, Xie D, et al. microbiano Deglycosylation and ketonization (en inglés) Ginsenósidos Rg1 and Rb1 por Fusarium oxysporum [J]. J Asian Nat Prod Res, 2011,13: 652-658.
[24] Liu X, Qiao LR, Xie D, et al. microbiano transformation Absidia coerulea y la reversión de la actividad de los metabolihacia las células tumorales resisitantes multifármacos [J].Fitoterapia, 2011, 82: 1313-1317.
[25] Ko SR, ChoiKJ, SuzukiK, et al. Preparación enzimática De los ginsenósidos Rg2, Rh1 y F1 [J]. Chem Pharm Bull, 2003, 51: 404-408.
[26] Ko SR, Suzuki Y, Suzuki K, et al. marcado production De los ginsenósidos Rd, F2, Rg3, y el compuesto K por vía enzim. Chem Pharm Bull, 2007, 55: 1522-1527.
[27] Liu L, Zhu XM,Wang QJ, et al. enzimenzimenzim Preparación preparación De 20(S, R)-protopanaxadiol by transformation De 20(S, (a) (b) (b) desde negro ginseng [J]. Fitoquímica, 2010, 71: 1514- 1520.
[28] Liu L, Gu LJ, Zhang DL, et al. Conversión microbiana de raro ginsenósido Rf a 20(S)-protopanaxatriol por Aspergillus niger [J]. Biosci Biotechno1 Biochem, 2010,74: 96-100.
[29] Kim DS, Cue YS,Yu HS,et al. Ginsenoside Rh2 preparado a partir de la reacción enzim[J]. J Dalian Inst Light Ind, 2002, 21: 112-115.
[30] Noh KH, hijo JW, Kim HJ, et al. Ginsenoside Producción de K compuesto a partir de extracto de raíz de ginseng mediante una be- ta-glicosidtermoestable desde Sulfolobus solfataricus [J]. Biosci Bio- techno1 Biochem, 2009, 73: 316-321.
[31] Yoo MH, Yeom SJ, Park CS, et al. producción De aglicon protopanaxadiol vía compuesto K por un termoestable − -glicosida de Pyrococcus furiosus [J]. Appl Microbiol Biotechnol, 2011, 89: 1019-1028.
[32] Chen SL, Zhu XX, Li CF, et al. genógenómica and Biología sintética de la medicina tradicional China [J]. Acta Pharm Sin, 2012, 47: 1070-1078.
[33] Wang W, Meng C, Zhu P, et al. Preliminary study Sobre el metabolismo engineering of levadura for producing taxadieno [J].China Biotechnol, 2005, 25: 103-108.
[34] Ajikumar PK, Xiao WH, Tyo KE, et al. Optimización de la vía isoprenoide para la sobreproducción de precursores de taxol en Escherichia coli [J]. Science, 2010, 330: 70-74.
[35] Kong JQ, Wang W, Wang En, et al. The mejora Producción de amorfa-4,11-dieno por una variante conforma levadura [J].JAppl Microb, 2009, 106: 941-951.
[36] Westfall PJ, Pitera DJ, Lenihan JR, et al. producción Amorfadieno en levaduras, y su conversión a ácido dihidroartemisínico, precursor del agente antimaláriartemisinina [J]. Proc Natl Acad Sci USA, 2012, 109: E111-118.
[37] Wu Q, Zhou YQ, sol C, et al. Progresos progresos in Ginsenósidos biosíntesis y prospecde ingeniería metabólica secundaria para the production of ginsenosides [J]. China Biotechnol, 2009, 29: 102-108.
[38] Ming QL, Han T, Huang F, et al. Avances avances in studies En ginsenoside biosíntesis and its relacionados enzymes [J]. Chin Tradit Herb Drugs, 2010, 41: 1913-1917.
[39] Wu Q, Sun C, Chen SL. Identificación identificación and Análisis de expresión de un gen de la 3-hidroxi3-metilglutaril coenzima a reductasa from American ginseng [J]. La planta Los fondos estructurales J, 2012, 5: 414-420.
[40] Kim OT,Bang KH, Jung SJ, et al. Caracterización Molecular del gen ginseng farnesil difosfato sintasa y su up- reg- ulation by methyl jasmonate[J]. Biol Plant, 2010, 54: 47-53.
[41] Ali Ali MB, Yu KW (KW) Hahn EJ, et A1. Methyl jasmonate Y salicílico Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido elicitaion induce ginsenosides Acumulación, and No enzimático antioxidante in Cultura de suspensión Panax ginseng roots (en inglés) in bioreactores [J]. La planta célulaRep, 2006, 25: 613-620.
[42] Kim OT,Kim SH, Ohyama K, et al. Upregulation of phytosterol and triterpene biosynthesis in Centella asiatica hairy Raíces sobreexpresadas ginseng farnesyl difosfato synthase [J]. La plantacélulaRep, 2010, 29: 403-411.
[43] Lee MH, Jeong JH, Seo JW, et al. mejorado Biosíntesis de triterpeny fitoesteren Panax ginseng sobrexxpressing squalene synthase gen [J]. La planta Cell Fisiol, 2004, 45: 976-984.
[44] Kim TD, Han JY,Huh GH, et al. Expresión y caracterización funcional De tres squalene synthase genes Asociado con Biosíntesis de saponina In Panax ginseng [J]. Plant Cell Fisiol,2011, 52: 125-137.
[45] Seo JW, Jeong JH, Shin CG, et A1. La sobreexpresión de la squa- lene sintasa en Eleutherococcus senticosus aumenta la acumulación de phytos- terol y triterpen. [J]. Phytochemistry, 2005, 66: 869-877.
[46] Jiang SC, Zhang MZ, Wang Y, et al. interferencia Construcción vectorial del gen SQS de Panax ginseng y callo de transformación [J]. J Jilin Univisidad, 2011, 49: 1136-1140.
[47] Han JY, In JG, Kwon YS, et al. reglamento Of ginsenoside and phytosterol biosynthesis by RNA interferences of squalene epoxidase gene in Panax ginseng [J]. Phytochemistry, 2010, 71: 36-46.
[48] Jiang SC, Liu WC, Wang Y, et al. Correlación correlación Entre la acumulación de ginsenósido y la expresión génica de SQS y SQE en diferentes Órganos órganos Panax quinquefolius [J]. Chin Tradit Herb Drugs, 2011, 42: 579-584.
[49] Kushiro T, Ohno Y, Shibuya M, et A1. Conversión In vitro de 2,3-oxidosqualeno en dammarenediol por Panax ginseng microsomes [J]. Biol Pharm Bull, 1997, 20: 292-294.
[50] Tansakul P, ShibuyaM, Kushiro T, et al. Dammarenediol-II Sintasa, la primera enzima dedicada a la biosíntesis de ginsenósido, en Panax ginseng [J].FEBS Lett, 2006, 580: 5143-5149.
[51] Han JY, Kwon YS, Yang DC, et al. Expresión expresión and Silenciamiento indupor interferencia de ARN del gen dammarenediol sintasa in Panax ginseng [J]. La planta Cell Physiol, 2006, 47: 1653-1662
[52] Lee MH, Han JY,Kim HJ,et al. La producción de Dammarenediol-II confiere tolerancia TMV en tabaco transgéexpresando Panax ginseng Dammarenediol-II synthase [J]. Plant cell Physiol, 2011, 53: 173-182.
[53] Kushiro T, Shibuya M, Ebizuka Y. − -amirin Clonación de sintasa de la clase oxidosqualene que cataliza la formación del triterpenmás popular entre las plantas superiores [J]. Eur J Biochem, 1998, 256: 238-244.
[54] Zhao SJ, Hou CX, Liang YL, et al. Clonación de ginseng − como gen and the construcción of its antisentido La planta Vector de expresión [J]. China Biotechnol , 2008, 28: 74-77.
[55] Niu YY, Luo HM, Huang LF. Avances avances in the study De CYP450 implica en la biosíntesis ginsenósidos [J]. Ciencia mundial Tradit Chin Med Mater Med, 2012, 14: 1177-1183.
[56] Han JY, Kim HJ, Kwon YS, et al. The Cyt P450 La enzima CYP716A47 cataliza la formación de protopanaxadiol a partir de dammarenediol-II durante ginsenoside biosynthesis in Panax ginseng [J]. Plant Cell Physiol, 2011, 52: 2062-2073.
[57] Chen SL, Luo HM, Li Y, et Al. 454 EST análisis Detecta genes implicados en la biosíntesis del ginsenósido en Panax ginseng [J]. Plant Cell Rep, 2011, 30: 1593-1601.
[58] Sun C, Li Y, Wu Q, et al. De novo Secuenciy análisis del transcriptode raíz de ginseng americano usando un GS FLX Titanium Plataforma plataforma to descubrir Un supuesto genes involved in ginsenoside biosynthesis [J]. BMCGenomics, 2010, 11:
262-273.
[59] Luo HM, Sun C, Sun YZ, et al. El análisis del transcriptoma de la raíz de Panax notoginseng descubre un supuesto triterpensapon- genes biosintéticos y marcadores genéticos [J]. BMC Genomics, 2011, 12: S5.
Han JY, Hwang HS, Choi SW, et al. citocromo P450 CYP716A53v2 catcat the formation of Protopanaxatriol de protopanaxadiol durante Ginsenoside biosynthesis In Pa- nax ginseng [J]. Plant Cell Physiol, 2012, 53: 1535-1545.
[61] Chen X, Xue Y, Liu JH, et al. Purificación y caracterización de glucosiltransferasa de cultivos de raíz pilosa de Panax Ginseng [J]. Pharm Biotechnol, 2009, 16: 50-54.
[62] Yue CJ, Zhong JJ. Purificación y caracterización de UDPG: ginsenoside Rd glucosiltransferasa from suspensión Células células of Panax notoginseng [J]. Proc Biochemistry, 2005, 40: 3742-
3748.
-
anterior
Estudio sobre el extracto de Ginseng bueno para antibacteriano
-
siguiente
Estudio sobre la síntesis de ginsenósido


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




