Stduy on Ginsenoside Rg1 Rb1 Rg3
La farmacocinética es el estudio de los procesos de absorción, distribución, metabolismo y excreción de fármacos en el organismo. Es la clave para estudiar la forma y el mecanismo de acción de las drogas. Sólo conociendo la farmacocinética de un fármaco podemos explorar a fondo el mecanismo molecular de su acción farmacológica.
ginsenósidosSon los principales ingredientes activos en la preciosa hierba medicinal China ginseng. Tienen las funciones de mejorar la memoria [1], aumentar la inmunidad [2-3], mejorar los vasos sanguíneos [4], regular la secreción endocr[5], retrasar el envejecimiento [6] y combatir los tumores [7]. En los últimos años, la investigación farmacocinética de los ginsenósidos se ha convertido en un tema candente de preocupación en el país y el extranjero. Ahora se da una revisión sobre la farmacocinética de los ginsenósidos en el cuerpo y los factores que los afectan.
1 farmacocinética de varios monómeros ginsenósidos
Aunque el ginseng, como medicina tradicional China, se ha demostrado durante mucho tiempo que tiene efectos farmacológicos, la investigación sobre su situación enVivo vivoestá todavía en su infancia, y la mayor parte de la investigación actual se centra en la farmacocinética deGinsenósido monómeros.
1.1 farmacocinética del ginsenósido Rg1
GinseGas naturalsaponenRg1Puede pasar fácilmente a través de la barrera intestinal y se absorbe de manera dependiente del tiempo en todo el intestino delgado [8]. Feng Liang et al. [9] estudiaron la farmacocinética y los metabolide El ginseng.saponrg1 en ratas después de la inyección intravenosa y la administración oral. Después de la administración oral a ratas, la cantidad de metabolide gg1 de ginsenósido en el cuerpo excede la del fármaco original. Cuatro sustancias, ginsenósido Rg1, Rh1, F1 y protopanaxatriol, fueron detectadas en el plasma, y sus tmáx fueron 0.92, 3.64, 5.17 y 7.30 h, respectivamente. Ylos MRT fueron 2,68, 5,06, 6,65 y 5,33 h, respectivamente, y los valores de AUC0-t fueron 2363,5, 4185,5, 3774,3 y 396,2 ng·h·mL-1, respectivamente. Después de la administración intravenosa, el gg1 ginsenósido estaba principalmente en su forma original en el cuerpo de la rata, con sólo una pequeña cantidad de metaboli. Tres sustancias, ginsenósido Rg1, Rh1 y F1, fueron detectadas en su plasma, con t1/2β de 3.12, 5.87 y 6.87 h, respectivamente, y MRT de 1.92, 5.99 y 7.13 h, respectivamente, AUC0-t fueron 1454.7, 597.5 y 805.6 ng·h·mL-1, respectivamente. Lee et al. [10] investigaron las características farmacocinéticas del compuesto K del metabolidel ginsenósido gg1en humanos. Los resultados mostraron que el compuesto K fue absorbido en la sangre dentro de las 24 hdespués de la administración oral de ginseng, y su tmax, − max y AUC fueron (10.76 − 2.07) h, (27.89 − 24.46) ng·mL−1 y (221.98 − 221.42) − g·h·mL−1, respectivamente. La absorción del compuesto K por el cuerpo humano no se ve afectada por la flora intestinal, pero sus parámetros farmacocinéticos están relacionados con la tasa de conversión de la flora intestinal en cada sujeto y existen diferencias individuales.
1. 2 farmacocinética de ginsenósido Rg2
Ginsenósido Rg2, junto con ginsenósido Rg1, es un triterpenginsenósidoY un fármaco candidato para el tratamiento de enfermedades cardiovasculares y cerebrovasculares. Tiene dos isómeros, R y S. el AUC de los diferentes isómeros de ginsenósido Rg2 en ratas es proporcional a la dosis (inyección intravenosa: 10, 20, 50 mg·kg-1) y es consistente con un modelo abierto de un solo compartimento. Los valores de los parámetros farmacocinéticos Ke, t1/2Ke, Ve y CLs no se vieron afectados por la dosis administrada; Senembargo, hubo diferencias significativas en Ke, t1/2Ke y CLs entre S-ginsenoside-Rg2 y R-ginsenoside-Rg2 (P < 0.05) [11]. Gui et al. [12] administraron 25 mg·kg-1 de 20(R, S) ginsenósido Rg2 [incluyendo 2 mg·kg −1 de 20(R) -ginsenoside-Rg2 y 23 mg·kg −1 de 20(S) -ginsenoside-Rg2] a ratas mediante inyección en la vena de la cola. Se encontró que 20(R) -ginsenósido Rg2 y 20 (S) -ginsenósido Rg2 podrían ser detectados en la sangre 1. 5 h después de la inyección. Y sus principales parámetros farmacocinéticos t1/2α, t1/2β, K12, AUC y CLs fueron (4.024 6 ± 0.008 7) y (3.724 2 ± 0.045 9) min, (71.1999 ± 3.1586) y (38.4414 ± 1.1134) min, (0.0997 ± 0.157) y (0.0942 ± 0.0358) min-1, (197.7176 ± 5.1766) y (1092.5109 ± 83.0747) ± g·min·mL-1, (0. 126 4 ± 0. 3 000) y (0. 023 2 ± 0. 001 3) min−1, y los parámetros farmacocinéticos del ginsenósido Rg2, que contiene isómeros, se ajustan a un modelo de dos compartimientos.
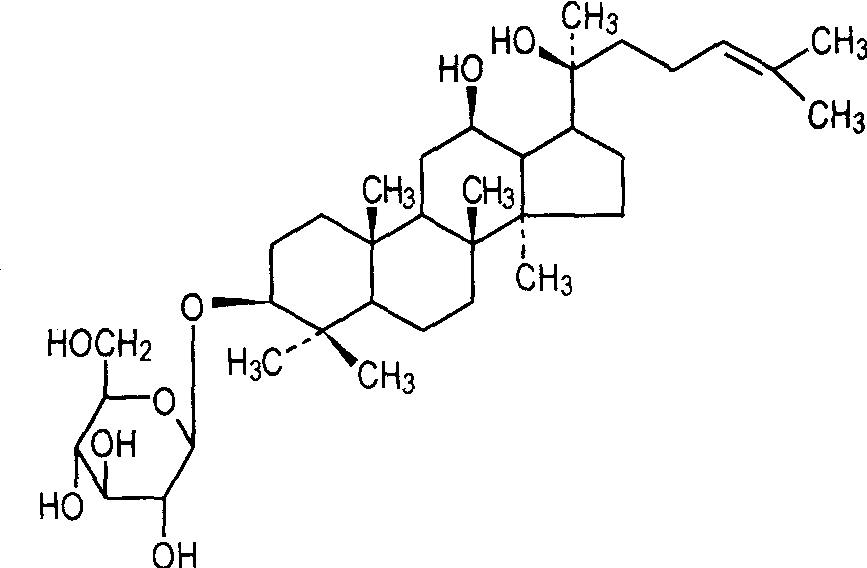
1. 3 farmacocinética de ginsenósido Rg3
Después de que el ginsenósido Rg3fue inyectado intramuscularmente1. 5 mg·kg-1), la distribución del contenido en cada órgano de la rata fue en orden descendente: El bazo > Corazón > Riñón > Hígado [13]. Cai et al. [14] usaron LC-ESI-MS para estudiar la farmacocinética del ginsenósido Rg3 en Plasma plasmade rata y sus metabolienvitro. El ginsenósido Rg3 no se detectó en orina de rata, ni se administró por vía oral (50 mg·kg-1) ni por vía intravenosa (5 mg·kg-1). Senembargo, Rg3 puede ser detectado en la sangre dentro de 1,5 h después de la inyección intravenosa, y se metabolirápidamente (vida media metabólica 14 min). Otros estudios sobre el metabolismo del ginsenósido Rg3 se llevaron a cabo enVitro vitrosimulando el ambiente gastrointestinal. Se encontró que el principal metabolito era el protopanaxadiol, que contiene un grupo hidroxilo, mientras que no se detectaron Rh2 y protopanaxatriol, que son metabolireconocidos. Al mismo tiempo, se encontró que el ginsenósido Rg3 sufre principalmente reacciones oxiden el hígado. Después de 16 horas, el hígado de rata microsomal S9 oxida el ginsenósido Rg3 a la aglicona, que luego se oxida por el citocromo P450 a los 24,25-epoxides.
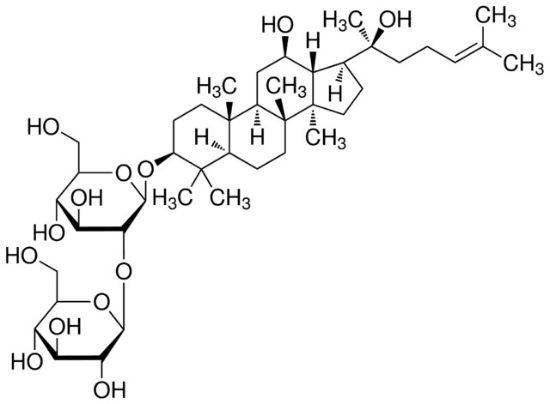
1. 4 farmacocinética del ginsenósido Re
Liu et al. [15] estudiaron laFarmacocinética del ginsenósido Reen humanos. Después de la administración oral a una dosis de 200 mg·kg-1, el tmáx y t1/2 del ginsenósido Re fueron (1.19 ± 0.44) y (1.82 ± 0.75) h, AUC0-t y AUC0- ± fueron (2. 476 ± 2. 281) y (2. 699 ± 2. 284) − g ·h ·L-1, respectivamente, − max fue (0. 939 ± 0. 549) − g · L-1, CL/F era (124 054 − 84 725) L· H-1. Los metabolidel ginsenósido Re en orina se estudiaron más a continuación, y se infirieron tres rutas metabólicas del ginsenósido Re: − Re − Rg1 − F1 − PPT, − Re − Rg2 − Rh1 − PPT, y − Re − Rg1 − Rh1 − PPT. Además, Joo et al. [16] encontraron que el extracto de ginsenósido puede promover la absorción del ginsenósido Re. El ginsenósido Re se administró por vía oral a dosis de 10 mg·kg-1 y 50 mg·kg-1, la biodisponibilidad absoluta del ginsenósido Re en el extracto de saponina de ginseng en ratas (0,33% y 0,75%) fue mayor que la de su monómero administrado por vía oral (0,28% y 0,19%).
1.5 farmacocinética de ginsenósido Rb1
El ginsenósido Rb1 es el principal protopanaxadiol saponin.Qian et al. [17] estudiaron los metabolidel ginsenósido Rb1 en la sangre, las heces y la orina de ratas. La administración intravenosa (5 mg·kg-1) de Rb1 ginsenósido se metaboliza principalmente en el cuerpo de la rata por oxid; Mientras que después de la administración oral (100 mg·kg-1) de ginsenósido Rb1, metabolitales como Rd, Rg3, F2, Rh2, y C-K fueron detectados en las heces de rata. Y se especula que la vía metabólica del Rb1 en el intestino de la rata es: Rb1 − Rd − Rg3 o F2 − Rh2 o C-K − PPD. Los metabolien la orina de las ratas son similares a los de las heces. La diferencia entre los metabolide la administración oral y la administración intravenosa es que el ginsenósido Rb1 se metaboliza principalmente mediante la eliminación del grupo de azúcar en el tracto gastrointestinal.
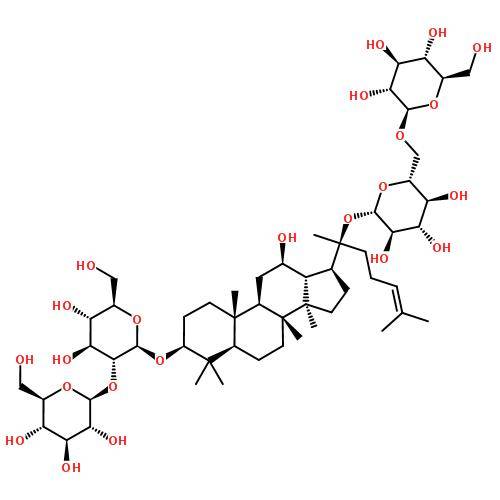
1. 6 farmacocinética de ginsenósido Rh2
Gu et al. [18] investigaron elDistribución de ginsenósido Rh2 en ratas. Después de una única administración oral de ginsenósido Rh2 (3 mg·kg-1), la concentración más alta se encontró en el hígado, mientras que las concentraciones en el corazón, bazo, estómago y riñón fueron similares a la concentración en sangre. Una pequeña cantidad se distribuyó en los ovarios, las glándulas suprarreny la grasa, mientras que el Rh2 no se detectó en el cerebro, la piel, los músculos y los testículos.
1. Farmacocinética de la Rd con ginsenósido 7
Rd Ginsenoside (10 mg·kg-1)Se administró por vía intravenosa en el cuerpo humano, y el valor máximo se alcanzó 0,5 h después, con un ≥ max de (2 841,18 ± 473,03) ng·mL-1 y T1 /2 is (19. 29 ± 3. 44) h, AUC0-t es (27 161. 63 ± 8 116. 88) ng · h · ML-1, y otros estudios han encontrado que si el ginseng saponin Rd se administra por vía oral o intravenosa, metabolitales como Rg3, Rh2, Rd y Rb1 se pueden detectar en la orina de rata [19]. Wang et al. [20] investigaron la farmacocinética de la Rd ginsenósido en perros mediante la administración intravenosa (0,2 mg·kg-1) y oral (2 mg·kg-1). El AUC de la Rd con ginsenósido tras la administración intravenosa y oral en perros fue (76.451,1 ± 15.874,8) y (1.930,3 ± 647,4) ng·h·mL-1, respectivamente, y la biodisponibilidad oral absoluta fue de 0,26%.
2 estudio farmacocinético de los ginsenósidos en compuesto de medicina tradicional China
El compuesto de medicina tradicional China es la esencia de la teoría de la medicina tradicional China, y es el foco y punto caliente de la investigación de la medicina tradicional China moderna. En los últimos años, los investigadores también han estudiadoFarmacocinética de los ginsenósidos en compuesto. Jiang Jie et al. [21] estudiaron las características farmacocinéticas del Shengmai Yin (un preparado compuesto de la medicina tradicional China compuesto de ginseng, ophiopogon japonicus y schisandra chinensis, con ginseng como ingrediente principal) en seres humanos. Después de una dosis oral única de 300 mL de Shengmai Yin se administró a 12 voluntarios sanos, los perfiles farmacocinéticos de los ginsenósidos Rg1 y ER siguieron un modelo de un solo compartimento.
Los tiempos pico promedio tmáx para GRR y ER fueron (4. 86 ± 1. 07) y (4. 75 ± 1. 04) h, respectivamente, y las concentraciones pico promedio ≥ max fueron (26. 33 × 12. 74) y (43. 32 × 16. 47) − g · mL-1, respectivamente. Las semividas de eliminación t1/2ke fueron (7. 99 ± 4. 63) y (7. 91 × 4. 56) h, respectivamente, el aclarcl fue (2. 73 ± 2. 50) y (1. 23 × 1. 12) mL · H-1, respectivamente, y el volumen aparente de la distribución V fue (31. 10 × 32. 26) y (11. 96 ± 9. 40) mL, respectivamente. AUC0-30 were (205. 96 × 114. 57) y (338. 73 ± 89. 10) − g · h · mL-1, respectivamente.Ginseng saponinas Rg1 y ReEstán sujetos a absorción cinética de primer orden y eliminación en el cuerpo humano. Mientras tanto, Lin Li et al. [22] usaron un modelo del saco intestinal de rata para estudiar el efecto del compuesto compuesto ginseng en la absorción de los ginsenósidos Rg1, Re, Rb1 y Rd. Los resultados mostraron que, en comparación con un solo componente, el grupo compuesto de dosis baja (0. 281 mg · mL-1) puede promover la absorción de los ginsenósidos Rg1, Re, Rb1 y Rd, el grupo compuesto de dosis media (0. 563 mg · mL-1) y el grupo de dosis alta (1. 125 mg · mL-1) no mostraron diferencias significativas en la absorción de los cuatro ingredientes, y la absorción de estos cuatro ingredientes tendió a ser inhibida con un aumento en la dosis del compuesto.

3 factores que afectan a la farmacocinética de los ginsenósidos
La absorción y distribución de los fármacos es un proceso muy complejo, y sus factores de influencia incluyen las diferencias de especie en los sujetos, las formas farmacéuticas de los fármacos, las vías de administración y las dosis administradas.
3. 1 sujetos
Debido a las diferencias de especie entre los animales de ensayo, los modelos farmacocinéticos de los ginsenósidos en diferentes animales de ensayo son diferentes. Gu et al. [18] estudiaron la farmacocinética deGinsenósido Rh2En perros y ratas. El modelo farmacocinético de ginsenósido Rh2 después de inyección intravenosa en perros Beagle (0.1 mg·kg-1) fue un modelo abierto de tres compartimentos, mientras que en ratas (0.1 mg·kg-1) fue un modelo de dos compartimentos.
3. 2 dosis de fármaco
La forma farmacéutica tiene un efecto significativo sobre la farmacocinética del medicamento de ensayo. Los cambios en la forma farmacéutica darán lugar a cambios en los parámetros farmacocinéticos.Ginseng saponin preparadosNo son una excepción. Rode Feng et al. [23] investigaron la tasa de liberación in vitro y las características de absorción de las nanopartículas lipísólidas de Rd de ginsenósido (renglc) en varios segmentos intestinales de ratas y las compararon con los monómeros de Rd de ginsenósido. La tasa acumulada de liberación de fármaco de glc-renc después de 120 h fue de 89,6 ± 1,6 %, mientras que la solución de control de Rd ginsenósido se liberó casi por completo (97,21 ± 1,19%) en el mismo medio después de 12 h. Las tasas de absorción de glc-reny Rd en los segmentos intestinales de ratas también fueron diferentes.
No hubo diferencia significativa en la absorción de los dos en los segmentos duodeno y yeyuno, y la diferencia en las tasas de absorción de los dos fue significativa en el íleon y los segmentos del colon. Bajo las mismas condiciones de dosificación, la concentración máxima en sangre del grupo de GLC fue significativamente mayor que la del grupo de Rd, y t1/2 y TRM se prolongaron significativamente. El AUMC, AUC0-t y AUC0→∞ del primero eran aproximadamente 2 veces, 1,5 veces y 2 veces las del segundo, respectivamente. Los resultados muestran que el renglc puede retrasar la liberación del fármaco, aumentar la absorción del fármaco en el intestino, mejorar significativamente la biodisponibilidad de la administración oral y prolongar su semivida en sangre. Además, Gu et al. [18] investigaron los cambios en los parámetros farmacocinéticos de 20(R) -ginsenósido Rh2 antes y después de la micronización en perros Beagle. Los perros Beagle fueron administrados por vía oral (1 mg·kg-1) 20(R) -ginsenósido Rh2 y su polvo micronizado, respectivamente, las concentraciones de fármaco en sangre fueron muestrey probados a 0,25, 0,5, 0,75, 1,0, 1,5, 2, 3, 5, 7, 9, 12, 24 y 36 h después de la administración. Los resultados mostraron que el ≥ max, AUC y biodisponibilidad deMicronizado 20(R) -ginsenósido Rh2Fueron aproximadamente el doble de los de la droga original, lo que indica que micronizado 20(R) -ginsenósido Rh2 puede disolverse mejor en el líquido intestinal y entrar en la sangre más fácilmente.

3. 3 vías de administración
Gu et al. [24] investigaron elCambios farmacocinéticos del ginsenósido 20(R) -Rh2Tras administración oral e intravenosa en perros Beagle. La curva farmacocinética de 20(R) -Rh2 tras inyección intravenosa (0. 1 mg · kg-1) se ajustó a un modelo de tres compartimentos, y los principales parámetros farmacocinéticos t1/2, CL y AUC0- ≤ fueron (8. 0 − 2. 8) h, (0.1 − 0.03) L · kg-1 · H-1, (857.0 − 209.6) ng · h · mL-1, y una larga vida media de eliminación terminal, lo que sugiere que 20(R) -Rh2 puede acumularse hasta cierto punto en el cuerpo; El modelo farmacocinético tras administración oral (1 mg·kg-1) es un modelo de dos compartimentos. Los principales parámetros farmacocinéticos tmax, − max, t1/2, y AUC0- − son (2.6 − 1.3) h, (371.0 − 199.6) ng·mL-1, (5.8 − 2.6) h, (1215.7 − 598.6) ng·h·mL−1. La lenta absorción de 20(R)-Rh2 en perros Beagle puede estar relacionada con su pobre solubilidad y dispersión. Además, debido al flujo de salida de la glicoproteína p y a la acción metabólica de la flora intestinal, la biodisponibilidad absoluta del fármaco en perros Beagle es baja, solo (16,1 ± 11,3 %). Por lo tanto, el desarrollo de formas farmacéuticas para 20(R) -Rh2 debe tener en cuenta el método de administración para reducir la transformación y aumentar la absorción del fármaco.
3. 4 dosis
La investigación actual ha encontrado que paraGinsenósidos de la misma configuraciónDentro del intervalo de dosis establecido, los parámetros farmacocinéticos de cada grupo de dosis aumentan con el aumento de la concentración de dosis, pero no hay diferencia significativa (P > 0. 05). Deng Yuanhui et al. [25] estudiaron las características farmacocinéticas de la inyección de ginsenoside-Rd después de una infusión intravenosa única en 12 voluntarios chinos sanos. Los resultados mostraron que los principales parámetros farmacocinéticos de las tres dosis (10, 40, 75 mg·kg-1): − max fueron (2,84 ± 0,47), (10,48 ± 1,74), (19,34 ± 2,62) mg·L-1, y t1/2 fueron (19,29 ± 3,44), (18,41 ± 2,92), (17,67 ± 2,01) h, y AUC0-t fueron (27,26 ± 8,12), (112,62 ± 24,08), y (208,36 ± 51,36) mg·h·L-1, respectivamente. Los valores ≥ max, AUC0-t y la dosis tienen una buena relación lineal, aumentando proporcionalmente con el aumento de la dosis del fármaco. Después de la corrección de dosis y la transformación logaritmo natural, no hay diferencia significativa entre las tres dosis de cada parámetro por análisis de varianza. Peng Ying et al. [26] estudiaron las características farmacocinéticas de la ER con ginsenósido a diferentes dosis en ratas. Después de la inyección intravenosa de tres dosis diferentes (20, 30, 40 mg·kg-1) de ginsenósido Re, la farmacocinética de los tres grupos de ratas fueron todos modelos de doble compartimiento. Los t1/2α fueron 6,505, 6,817, y 4,499 min, T1 /2 β fueron 28. 96, 30. 49 y 27. 57 min, respectivamente, y AUC fue de 599. 31, 1 025. 65 y 1 415. 7 min · mg · L-1, respectivamente. Los principales parámetros cinéticos de los tres grupos de ratas fueron similares, y el AUC aumentó proporcionalmente con el aumento de la dosis, lo que indica que la eliminación de ER es lineal dentro de este rango de dosis.
4 nuevas ideas para el estudio farmacocinético de los ginsenósidos
4.1 estudio farmacocinético de los metabolitos
La administración Oral es actualmente el principal método de administración para la mayoría de los compuestos de saponina. Los estudios han encontrado que después de la administración oral, los compuestos de saponin son fácilmente metabolizados por la flora intestinal, y la concentración sanguínea de la droga original es baja. Por lo tanto, algunos estudiosos han estudiado la farmacocinética de los ginsenósidos mediante la medición de la concentración sanguínea de sus metaboli. Ren et al. [27] establecieron un método HPLC-APCI-MS para la determinación de 20(S)-protopanaxadiol (PPD) en plasma y estudiaron las características farmacocinéticas de PPD después de la administración oral en ratas. Los resultados mostraron que el ≥ max de PPD en ratas fue (130.2 ± 41.5) ng·mL-1 y el tmax fue (150.0 ± 73.5) min. La biodisponibilidad absoluta de PPD fue (36.8 ± 12.4)%, 10 veces la de ITSProdrugs ginsenósidos Rg3 y Rh2Esto indica que la PPD se absorbe más fácilmente en el torrente sanguíneo. Por lo tanto, la medición de la concentración sanguínea de PPD puede reflejar con mayor precisión las características farmacocinéticas de los ginsenósidos Rg3 y Rh2.
4.2 farmacocinética de diferentes modelos de enfermedad
En el modelo del síndrome, el proceso farmacocinético de la medicina tradicional China es diferente del de los animales fisiológicos normales. Por lo tanto, es más instrucestudiar la farmacocinética de la medicina tradicional China sobre la base de síndromes. Zhou Wei et al. [28] estudiaron los cambios farmacocinéticos de los componentes efectivos de Qingnao Xuanqiao Fang, inclusoGardenoside, ginsenósido Rg1, Rb1 y notoginsenósido R1En ratas en condiciones normales y en las fases aguda y de recuperación del accidente cerebrovascular. Los resultados mostraron que los componentes efectivos de la fórmula Qingnao Xuanqiao: gardenia, ginseng saponin Rg1, y notoginseng saponin R1 fueron todos modelos abiertos de dos compartimentos en el grupo normal y el grupo modelo, y ginseng saponrb1 se conforma un modelo de un solo compartimento. La absorción de los cuatro componentes en ratas fue rápida, alcanzando − max en aproximadamente 45 minutos. La eliminación de gardenoside, ginsenósido Rg1 y notoginsenósido R1 es más rápida, mientras que el ginsenósido Rb1 es más lento. Para diferentes animales modelo, la concentración máxima en sangre y el área bajo la curva de concentración en sangre y tiempo de los cuatro componentes son, de mayor a menor, grupo modelo agudo > Modelo de recuperación > Grupo normal. La biodisponibilidad del grupo modelo al fármaco es mayor que la del grupo normal, lo que indica que los animales modelo tienen una mayor absorción de Qingnao Xuanqiao Fang en comparación con los animales normales.
4. 3 farmacocinética integrada multicomponente
Los efectos de la medicina tradicional China tienen un mecanismo de efectos multicomponente y multiobjetivo. Es más unilateral explicar el proceso farmacocinético de la medicina tradicional China y las prescripciones por los parámetros farmacocinéticos de un solo componente. Por lo tanto, Li Xiaoyu et al. [29] usaron saponinas de Panax notoginseng como fármaco modelo para establecer un modelo de investigación farmacocinética integrado basado en el área bajo la curva (AUC0-∞) de cada componente de saponinas de Panax notoginseng con un coeficiente de peso personalizado. A las ratas se les administraron saponinas totales de Panax notoginseng (300 mg·L-1) por sonda y (10 mg·L-1) por vía intravenosa, y las concentraciones del fármaco de notoginsenosideR1,Ginsenósido Rg1, Rd, Re y Rb1En plasma de rata se determinó utilizando LC-ESI-MS. Después de la administración por sonda, las saponinas totales de notoginseng se absorben rápidamente en el cuerpo de las ratas, pero el t1/2 de las saponinas de diol Rb1 y Rd es mucho mayor que el de las saponinas de triol Rg1, Re y R1, Y los resultados del modelo de estudio farmacocinético integrado establecido utilizando el área porcentual bajo la curva (AUC0-∞) de cada componente como un factor de ponderautodefinido mostraron que la curva de concentración en tiempo combinada se ajustaba a la ley de eliminación de fármacos administrados por gavage o por inyección intravenosa. Las saponinas totales de Panax notoginseng se absorben rápidamente en las ratas. Las t1/2 y AUC farmacocinéticas integradas tras sonda y administración intravenosa fueron de 18,88 y 19. 15 h y 25. 33, 84. 83 mg · h · L-1, respectivamente. Este modelo se ajusta a las características de los modelos farmacocinéticos clásicos, y los parámetros obtenidos pueden caracterizar la disposición general de la medicina tradicional China en mayor medida. Esto proporciona una nueva idea de investigación y método para establecer la investigación farmacocinética en la medicina tradicional China que se ajusta a las características de la medicina tradicional China.
5 perspectivas
Los ginsenósidos tienen diversas actividades biológicas y una eficacia clínica significativa. Se han realizado extensas investigaciones sobre sus efectos farmacológicos y comportamiento farmacocinético, y se han obtenido algunos resultados. Sin embargo, todavía hay algunas áreas que necesitan mejoras.
Por un lado,Los ginsenósidos son fácilmente metabolizados por el tracto gastrointestinalEn el hígado, y sus concentraciones en sangre en el cuerpo son bajas y no fáciles de detectar. Por lo tanto, las técnicas analíticas modernas de alta sensibilidad (GC-MS/MS, LC-MSn, LC-NMR, etc.) necesitan ser aplicadas a la detección de ginsenósidos in vivo. Al mismo tiempo, dado que las sustancias que ejercen efectos sobre los tejidos diana in vivo pueden ser sus metabolitos, también debe prestarse atención a la detección y análisis de metabolide ginsenósidos. Por otro lado, los estudios farmacocinéticos de los ginsenósidos en el país y en el extranjero solo han estudiado la relación entre la concentración sanguínea y el tiempo desde una perspectiva química [15,21], ignorando la conexión con la eficacia.
Por tanto, en futuras investigaciones, la farmacocinética deLos ginsenósidos deben combinarse con farmacodinámicaIndicadores para explorar la relación tridimensional entre la concentración-tiempo-efecto y establecer un modelo de análisis farmacocinético y farmacodinámico simultáneo, reflejasí de forma más realista y objetiva el proceso farmacocinético de los ginsenósidos en el cuerpo y proporcionando una cierta base para la eficacia clínica. Además, hay muchos tipos de ginsenósidos en el ginseng de la medicina tradicional China y los parámetros farmacocinéticos de cada individuo son diferentes [30], los cuales no se pueden usar para caracterizar el comportamiento farmacocinético general y las características del ginseng. Por lo tanto, debemos guiarnos por la teoría de la medicina tradicional China y combinar técnicas experimentales modernas como la metabolómica, la proteómica y los chips genéticos para explorar nuevos métodos de investigación farmacocinética sobre los componentes multiefecto de la medicina tradicional China desde una perspectiva de biología de sistemas [31].
Referencia:
[1] ZHANG ZHANGG,LIU A,ZHOU Y,et al.Panax ginseng ginsenoside- Rg2 Protege el deterioro de la memoria a través de anti-apoptosis en un modelo de rata Con demenvascular [J]. JEthnopharmacol,2008,115 (3) : 441 — 448.
[2] YU XT,WANG WANGS P. Observación clínica sobre el tratamiento del cáncer de estómago crónico por ginsenoside Rg3 en con Quimio-terapia [J]. Chin J Cancer Prev Treat, 2010,17 (10) :779-781.
[3] ZHANG Z,JIANG B,ZHENG X,et Al. Inmune Mejorar la Efectos de Rg3 Sobre linfocitos periféricos in vitro en pacientes con cáncer Tratado con radioterapia [J]. Chin Pharm J, 2004,39(4) : 261-264.
[4] SUI D Y,YU X F,QU S C,et al.Effects dePanax quinquefoli- um 20S-2protopanaxdiol saponins on experimental ventricular re- modeling in rata[J]. Chin Pharm J,2007,42 (2) : 108-112.
[5] LEE Y,JIN Y,LIM W,et al.A ginsenoside-Rh1, un componente del ginseng Saponin, se activa estrogen Receptor receptor in humana Carcinoma de mama de células MCF-7 [J]. J Steroid Biochem,2003,84 (4) : 463-468.
[6] WILLIAM C S,CHUNG W S,SALLY K W,et al.Ginsenoside El Re de Panax ginseng posee un importante antioxidante y antiperlipidémico eficacia in Estreptozotocina inducida Diabéticos diabéticos La rata [J]. Eur J Pharmacol,2006,550(1-3) : 173-179.
[7] KIM S E,LEE Y H,PARK H J,et al.Ginsenoside-Rs4,a New Tipo de saponina ginseng al mismo tiempo induce apoptosis y selec- tivamente eleva los niveles de proteínas de p53 y p21WAF1 en hepato- ma SK-HEP-1 células europeas [J]. Cáncer,1999,35 (3) : 507-511.
[8] LI H,SUN J G,XIE H T,et al.Study on absorciónmechanism of ginsenoside Rg1 usando rata everted Gut sac [J]. Chin J Clin Pharmacol Ther,2004,9 (5) : 510-513.
[9] FENG L,HU C J,YU L Y,et al.farmacocinética de ginsen- oside Rg1 Y sus metabolitos en ratas [J]. Acta Pharm Sin,2010,45 (5) : 636-640.
[10] LEE J,LEE E,KIM D,et al.Studies on absorption,distribu- tion ymetabolism of ginseng in Humans despuésoral Administration [J]. J Ethnopharmacol,2009,122(1) : 143-148.
[11] YANG X W,GUI F J,TIAN J M,et al.farmacocinética de ginsenoside-Rg2 En ratas [J]. Chin Pharmacol Bull,2009,25 (7) : 967-970.
[12] GUI F J,YANG X W,LI L Y,et al.determinación simultánea de enantiómero de 20 (R) - y 20 (S) -ginsenoside-Rg2 en plasma de rata después de administración intravenosa utilizando el método HPLC [J]. J cromatob,2007,850(1-2) : 1-6.
[13] HUANG Y,LIU J H. farmafarmafarma estudio Of ginsenoside20 (S) -Rg3 En ratas por HPLC-ELSD[J]. J Pr Med Theory,2005,12(9) : 2564-2566.
[14] CAI Z,QIAN T,WONG R,et al.Liquid cromato-elec - trospray ionimass spectrofor metabolism yPharma - cokinetic studies of ginsenoside Rg3[J]. Anal Chim Acta,2003, 492(1-2) : 283-293.
[15] LIU L,HUANG J,HU X,et al. Determinación simultánea de ginsenósido (G-Re,G-Rg1,G-Rg2,G-F1,G-Rh1) Y proto- panaxatriol en plasma y orina humana por LC-MS/MS y su aplicación en un estudio farmacocinético de G-Re en voluntarios [J]. J cromatob,2011,22(15) : 2011-2017.
[16] JOO K,LEE H J,JEON H Y,et al.estudio farmacocinético de la Re ginsenósido con puros ginsenoside Re y ginseng La fruta Extractos extractos Ratón ratón usando ultra Publicaciones periódicas Mass spectrometric method [J] (en inglés). J Pharmaceut Biomed,2010,51 (1-2) : 278-283.
[17] QIAN T,JIANG Z H,CAI Z. Croma - tografía líquida de alto rendimiento acoplada con espectrode masas en tándem aplicada para el estudio meta-bólico del ginsenósido Rb1 en rata [J]. Anal Biochem,2006, 352(1) : 87-96.
[18] GU Y,WANG G J,SUN J G. Caracterización farmacocinética del ginsenósido Rh2, un nutriente del ginseng contra el cáncer, en ratas y perros [J]. Food Chem Toxicol,2009,47 (9) : 2257-2268.
[19] YANG L,DENGY,XU S,et al.In vivo pharmacokinetic and Metabolismo studies of ginsenoside Rd [J]. J cromatob, 2007,854(1-2) :77-84.
[20] WANG W,WANG G J,XIE H T,et al.determinación de gin- senoside Rd en plasma de perro por cromatografía líquida after Fase sólida Extracción de extracción y su aplicación in Perro perro Estudios farmacocinéticos [J]. J cromatob,2007,852 (1-2) : 8-14.
[21] JIANG J,LI S,GONG P L,et al.farmacocinética de Shengmaiyin solución oral después de una dosis única en humanos [J]. Acta Med Univ Technol Huazhong, 2007,36(2) : 272-274.
[22] LIN L,ZU F Y,ZHANG W W,et al.efectos de la compatibilidad de compuestos sobre la absorción in vitro de saponinas ginsenósidas [J]. La bar J Mod Drug Appl,2010,4 (13) : 150 — 152.
[23] LUO D F,YE J T,ZHANGY S,et al.Studies on Drug release in vitro and absorption in rata in vivo of ginsenoside Rd sólido lípidos Nanopartículas [J]. Chin Pharmacol Bull, 2009,25 (7) : 923-926.
[24] GU Y,WANG G J,SUN J G,et al.estudio farmacocinético de ginsenoside 20(R) -Rh2 En perros Beagle por LC-ESI-MS [J]. Chin J Clin Pharmacol Ther,2006,11 (3) : 159-163.
[25] DENG Y H,ZENG X,FENG Y,et al.farmacocinética Y Tolerancia a dosis únicas de goteo intravenoso de ginsenoside-Rd en voluntarios sanos chinos [J]. Chin J Clin Pharmacol,2009,25 (2) : 116-120.
[26] PENG Y,WANG S J,PAN W S,et al.farmacocinética del ginsenósido Re en rata [J]. J Shenyang Pharm Univ,2006,23 (4) : 197-200.
[27] REN H C,SUN J G,WANG G J,et al. determinación sensible Dosis de 20 (S) -protopanaxadiol in rat plasma usando HPLC-APCI-MS: Aplicación del estudio farmacocinético en ratas [J]. J Pharm Bi- omed,2008,48 (5) : 1476-1480.
[28] ZHOU W,SHI R B,SUN J N,et al.farmacocinética de fracciones eficaces de la fórmula Qingnaoxuanqiao en diferentes modelos de rata [J]. J Beijing Unit Tradit Chin Med, 2008,31 (4) : 265-268.
[29] LI X Y,HAO H P,WANG G J,et al.Integrated pharmacokinet- IC Study of multiple effective components conteniin total Panax Notoginsenósidos [J]. Chin J Nat Med,2008, 6(5) : 377-381.
[30] SONG M,ZHANG S,XU X,et al. Determinación simultánea Tres saponinas de Panax notoginseng en sub-nanograms por LC-MS / MS en plasma de perro para farmacocinética del compuesto Danshen tab- lets [J]. J cromatob,2010,878 (32) : 3331-3337.
[31] WANG Z,MA X,CHEN X,et actual métodos and Ad - vancesin microbial metabolom ICS [J]. Prog Chen, 2010,22(1) : 163-172.


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés