¿Cuál es el beneficio del ácido rosmarínico?
rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidois unphenolic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidocompound denaturalorigin, formed porthecondensatieldecaffeic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoy3,4-dihydroxyphenyl lactic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido[1]. Its estructuralformulunis shown enFigure 1. rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidois widely distributed, especially enelBoraginaceae, Lamiaceae, yCucurbitaceae families [2-3]. It wasfirst isolated ypurified desdeRosmarinus officinalisLinn porItalianchemists ynamed rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido[4]. As an important polyphenolic antioxidant, rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidohas a wide range deapplicationesenfood ycosmetics [5-6], yit also has good pharmacological actividadessuch as anti-inflammatory, antibacterial, yantiCáncer de cáncer[7], so it has attracted widespread attention.
Senembargo, las deficiencias en las propiedades físicas y químicas del ácido rosmarínico han resultado en su baja biodisponibilidad. Las principales formas farmacéuticas utilizadas actualmente en la investigación selel polvo y la solución acuosa, que no pueden satisfacer las necesidades de la medicación clínica. La tecnología de administración de fármacos puede mejorar las deficiencias de las propiedades físicas y químicas de los fármacos terapéuticos, mejorar la administración a los sitios enfermos, mejorar los efectos del tratamienay, por lo tanto, promover el desarrollo de fármacos y la adherencia del paciente. Por lo tanto, este artículo revisa los efectos farmacológicos del ácido rosmarínico y el progreso de la investigación de la administración de nuevos fármacos, proporcionando una referencia para el desarrollo y aplicación clínica del ácido rosmarínico.
1 efectos farmacológicos del ácido rosmarínico
1.1 efectos antioxidantes
Las especies reactivas del oxígeno incluyen aniones superóxidos, peróxidos, radicales hidroxilo y oxígeno singlete. Estas moléculas pueden afectar las señales de supervivencia celular y dañar el ADN[7]. El estrés oxidativo es un desequilibrio entre los oxidantes intracelulares y los antioxidantes, que conduce al daño celular. Estudios previos han demostrado que las enfermedades tales como Alzheimer&#La enfermedad 39;s [8] y la enfermedad pulmonar obstructiva crónica [9] están estrechamente relacionadas con el estrés oxidativo. En los últimos años, el potencial de las moléculas naturales para inhibir la producción de radicales libres o eliminar radicales libres ha atraído la atención generalizada. Como un importante compuesaácido fenónatural, el ácido rosmarínico tiene buenas propiedades antioxidantes debido a la presencia de un grupo hidroxifenóy un doble enlace conjuen la posición C-3 en su estructura. Su capacidad de oxides superior a la del ácido clorogénico, la vitamina E y el ácido cafeico [10-11].
El ácido rosmarínico puede ejercer su actividad antioxidante a través de varias vías, eliminando radicales libres de nitrógeno y oxígeno, reduciendo la producción de especies reactivas de oxígeno, degradcompuestos pro-oxi, y aumentando las moléculas antioxidantes como el glutatión; También activa el factor nuclear factor 2 relacionado con el E2, que a su vez activa las enzimas antioxidantes correspondientes [12]. Vostalova etAl. [13] mostraron que el ácido rosmarínico puede reducir significativamente la producción de especies reactivas del oxígeno y reducir la secreción de interleucin-6 (IL-6) por las células Ty los macrófagos, impidiendo así la producción de queratinocitos humanos causada por la radiación UVB.
1.2 efecto antiinflam
La inflamación es el cuerpo 's respuesta de defensa a los estímulos y se manifiesta generalmente como enrojecimiento, hinchazón, calor, dolor y disfunción. Numerosos estudios han demostrado que el ácido rosmarínico tiene un buen efecto antiinflamatorio. La activación del complemento a menudo ocurre en el sitio de inflamación, y el ácido rosmarínico puede unirse covalentemente a la sustancia activa del complemento C3b para inhibir la actividad del complemento senefectos secundarios [14]. La ciclooxigenasa-2 (COX-2) es un factor inflamatorio peligroso. Scheckel etAl.[15] encontraron que el ácido rosmarínico puede inhibir la expresión del gen COX-2 en las células cancerosas del El colony las células epitelimambenig. Lembo etAl.[16] demostraron que el ácido de romero puede prevenir el daño inducido por la radiación ultravioleta de onda media en una línea de células de queratinocitos humanos, reducir la producción de mediadores inflamatorios como el factor de necrosis tumoral - - (FNT - -), IL-6, IL-8 y la proteína quimiotáctica de monocitos 1, y promover la producción de la IL-10 protectora.
Además, Rocha etAl.[17] establecieron un modelo de edema inflamlocal local en las patas de ratas inducido por carragenina, un modelo de isquemia/reperfusión hepática y un modelo de lesión térmica inflamatoria sistémica. Se evaluó la actividad antiinflamatoria del ácido rosmarínico después de la administración oral o intravenosa. En comparación con el grupo de control, el edema en las patas de las ratas en el grupo de tratamiento con ácido rosmarínico se redujo en aproximadamente un 60%. Posiblemente por su actividad antiinflamatoria al reducir la expresión de factores pro-inflamtnf - -, IL-6 e IL-1 -. En el modelo de isquemia y reperfusión hepática, el ácido rosmarínico puede reducir significativamente las concentraciones plasmáticas de alanina aminotransferasa, glutamato transferasa y lactato deshidrogenasa. En un modelo de lesión por calor inflamsistsist, el ácido rosmarínico puede reducir los marcadores de la disfunción de múltiples órganos mediante la regulación de las metaloproteasas de matriz 9 (MMP9) y el factor nuclear -κB(NF-κB). Ghasemzadeh RahbardaretAl.[18] estudió el efecto del ácido rosmarínico en el entorno neuroinflamatorio en un modelo murino de dolor neuropático y encontró que el ácido rosmarínico puede regular la neuroinflamación al reducir los factores inflamatorios y los marcadores oxidcomo la COX-2, la IL-1β, la prostaglandina E2 y la MMP2.
1.3 efecto antitumoral
Se sabe que el cáncer es una grave amenaza para la salud humana. El extracto de romero tiene un efecto regulador en varios tipos de cáncer, incluyendo el cáncer de colon, el cáncer de hígado y el cáncer de mama. Cao etAl.[19] encontraron que el extracto de romero puede inhibir las citoquinas inflamy la vía NF-κB en el microambiente tumoral, ejerciendo así un efecto terapéutico en el cáncer de hígado. También puede regular el valor de CD4+/CD8+ y la secreción de IL-2 y interfer-, inhibide la expresión de IL-6 e IL-10, regula a la baja el linfoma de células b 2 (Bcl-2), y la expresión de proteína X (Bax) y caspas-3 asociadas al Bcl-2, inhibiendo así eficazmente el crecimiento tumorAl.LiHong etAl.[20] encontraron en un experimento celular enVitro vitroque el ácido rosmarínico puede regular a la baja el gen Bcl-2 y upreregular el gen Bax, inhibiendo así la proliferación y migración de las células de cáncer de mama humano e induciendo la apoptosis de las células tumorales.
Karthikkumar etAl.[21] usaron un modelo de cáncer de colon de rata indupor 1,2-dimetilhidrazina y encontraron que el ácido rosmarínico puede regular las lesiones previas al cáncer de colon al afectar las concentraciones de enzimas antioxidantes en las ratas. SaikoetAl.[22] usaron ácido rosmarínico para tratar las células HL-60de la leucemia humana y encontraron que el ácido rosmarínico puede inhibieficazmente la proliferación de células tumorales y promover la apoptosis al inhibide la actividad de la nucleótido reductasa y reducir la producción de dNTP,inhibide ese modo eficazmente la proliferación de células tumorales y promover la apoptosis. Han etal. [23] encontraron que el ácido rosmarínico inhila la invasión y migración de las células tumorales al inducir la fosforilación de la proteína quinasa activpor adenosina monofosfato (AMPK), reduce la expresión de MMP2 y MMP9, disminuye la adhesión yla expresión de moléculas de adhesión como la molécula de adhesión intercelular 1 yla integrina − 1, inhibiasí la proliferación de células de cáncer colorrectal. Además, en un modelo de ratón, el ácido rosmarínico puede reducir significativamente el número de nódulos tumorales metastásicos pulmonares al activar AMPK.
1.4 efecto antimicrobiano
El ácido rosmarínico tiene un cierto efecto inhibidor sobre las bacterias. El ácido rosmarínico 500 mmol/Lpuede inhibir estafilococos, y la actividad bacteriostática se ve afectada por el pH y la concentración de iones [24]. Abedini etal. [25] encontraron que el ácido rosmarínico 0,3 — 1,3 mg/mLtiene un efecto inhibitorio sobre Staphylococcus aureus 5001, Staphylococcus ludens T26A3, Klebsiella oxytoca, Enterococcus faecium C159-6, Pseudomonas aeruginosa ATCC27583, Corynebacterium, Mycobacterium smegmatis 5003 y Staphylococcus warneri T12A12. El ácido de romero inhiescherichia coli, Staphylococcus aureus, Salmonella y Bacillus subtilis al alterar la estructura celular y las proteínas de la bacteria e inhibiendo su actividad de Na+,K+ -atpasa, con diferentes grados de inhibición dependiendo de la bacteria [26].
Además, el ácido rosmarínico también tiene efectos antivirales. Bajo condiciones ácidas, el ácido rosmarínico reacciona con iones nitrito para formar ácidos 6-nitro y 6,6-dinitrorosmarínicos [27]. Estos compuestos pueden actuar como inhibidores de la integrasa del virus de inmunodeficiencia humana-1 a nivel micromolar, inhibide la replicviral en células humanas de leucemia de células t MT-4, y mejorar la inhibide la anti-integrasa y los efectos antivirales.
Otros efectos farmacológicos
Además de los efectos mencionados anteriormente, el ácido rosmarínico también tiene efectos neuroprotectores, antiangiogénicos y antidepresi. Los efectos neuroprotectores y anti-angiogénicos del ácido rosmarínico están estrechamente relacionados con sus propiedades antioxidantes y antiinflam. Ren etal. [28] confirmaron en un experimento con modelo celular de neurotoxicidad envitro que el efecto protector del ácido rosmarínico se relaciona con la reducción de la producción de especies reactivas de oxígeno y la función mitocondrial. Se encontró que el ácido rosmarínico tiene un efecto neuroprotector en un modelo de Alzheimer en ratas#Enfermedad 39;s, posiblemente porque puede prevenir el desequilibrio antioxidante y el daño colinérgico causado por el − -amiloide [29].
Shang etal. [30] encontraron que el ácido rosmarínico puede reducir el estrés oxidativo causado por la lesión de la médula espinal en ratones, desregular el factor inflamnf - − B y los factores pro-inflamatorios, ejerciendo así efectos neuroprotectores. Huang etal. [31] seleccioncélulas endotelide venas umbilichumanas para estudiar los efectos y mecanismos antiangigénicos del ácido rosmarínico y encontró que el ácido rosmarínico puede inhibilos procesos de angiogénesis dosidependiente, como la proliferación de células endoteli, la migración y la formación de tubos, así como reducir los niveles de especies de oxígeno intracreactivas, la expresión del factor de crecimiento endotelial vascular y la liberación de IL-8. Mahmoud etal. [32] también demostraron que el ácido rosmarínico aumenta el efecto terapéutico del paclitaxel en el cáncer de mama al inhibide la angiogénesis. Además, algunos estudios han mostrado que el ácido rosmarínico tiene efectos antidepresi. Lataliza etal. [33] estudiaron el efecto del ácido rosmarínico en un modelo de ratón de depresión inducida por lipopolisacárido y encontraron que el ácido rosmarínico ejerce un efecto antidepresia través de la vía de señalización del receptor cannabinoide/receptor activado por la proliferación del peroxisoma γ. Además, el ácido rosmarínico también tiene efectos terapéuticos sobre la enteritis y la gota, y tiene amplias perspectivas de aplicación.
2 aplicación de sistemas de liberación de ácido romero
Como se mencionó anteriormente, el ácido romero tiene varios efectos farmacológicos tales como anti-oxidy anti-inflamación, y puede ser utilizado para tratar diversas enfermedades. Senembargo, las formas farmacéuticas comúnmente utilizadas en la actualidad son polvos y soluciones, que son difíciles de satisfacer las necesidades de las diferentes vías de administración de medicamentos y sitios de la enfermedad. Además, las deficiencias de las propiedades físicas y químicas del ácido de romero en sí también limitan su aplicación clínica [34]. Para resolver estos problemas, la mayoría de los investigadores utilizan nuevos portadores de fármacos para administrar ácido rosmarínico para mejorar su efecto terapéutico.
2.1 nanogotitas
Las nanogotitas son emulsiones formadas espontáneamente de agua, aceite, surfacy co-surfac. Por lo general tienen un tamaño de partícula de 1-100 nm y son termodinámicamente estables, transparentes o translúcidos dispersiones homogé. Tienen las ventajas de aumentar la solubilidad de fármacos poco solubles, mejorar la estabilidad, reducir la irritación y aumentar la liberación sostenida y la acción dirigida [35]. Facheletal. [36-37] prepararon nanoemulsiones de aceite en agua de ácido rosmarínico usando el método de autoemulde fosfolípidos y el método de diseño de superficie de respuesta, y las modificaron en la superficie con quitosano para obtener nanoemulde de ácido rosmarínico recubierde quitosan. Los resultados de los estudios de administración dela mucosa nasal mostraron que las nanoemulsiones tenían buena adhesión, pueden retrasar la liberación del fármaco, tienen un tiempo de penetración largo y tienen una alta tasa de penetración/retención del fármaco en la mucosa nasal de los cerdos. Además, el efecto protector contra el daño nervioso es mejor que el de la vía de inyección intraperitoneal, que mejora la biodisponibilidad del ácido rosmarínico en el cerebro. Se ha demostrado además que las nanoleches de ácido rosmarínico pueden reducir significativamente la proliferación de astrocitos y los cambios necróticos mediante la reducción de la producción de especies reactivas de oxígeno y los niveles de óxido nítrico y la prevención de una disminución en el contenido total de tiol [38].
Marafon etal. [39] prepararon nanoleches de ácido de romero y evaluaron el efecto de la aplicación tópica de una formulación que contenía el surfacno iónico polisorbato 80. Los resultados mostraron que el polisorbato 80 tenía un efecto positivo en la retención/penetración del ácido romero en la piel entera, y podría usarse en el desarrollo de aplicaciones tópicas para productos de cuidado de la piel anti-envejecimiento. Panya etal. [40] estudiaron la interacción entre el -tocoferol y el ácido rosmarínico en emulsiones y encontraron que en las emulsiones O/W,el ácido rosmarínico y el -tocoferol exhifuertes efectos sinérgicos, aumentando la formación de ácido cafeico y mejorando aún más la estabilidad oxidde la emulsión. Kittipongpittayaetal. [41] investigaron el efecto del pH en el efecto antioxidante del ácido romero y el -tocoferol en emulsiones, y encontraron que la actividad antioxidante sinérgica de los dos era más fuerte a un pH de 7. En resumen, el ácido romero se puede utilizar como una herramienta para estudiar la interacción de los antioxidantes en las emulsiones.

Las nanoemulsiones son un tipo de nanoformulación. Sus partículas a nanoescala y sus sistemas mixtos agua-aceite pueden aumentar la solubilidad de los fármacos y evitar el efecto de primer paso del hígado. Las nanoemulsiones de ácido rosmarínico tienen ciertas ventajas en la administración nasal y transdérmica. Senembargo, el bajo contenido de aceite de las nanoemulsiones puede conducir a su baja visco, y su retención en el sitio de administración de la mucosa debe mejorarse. Además, la composición y estabilidad de la prescripción de nanoemulsión también son temas en los que los investigadores deben centrarse.
2.2 nanopartículas lipí
Las nanopartículas de lípidos sólidos (SLNs) son un sistema de administración de nanopartículas de fármacos hecho por adsorción o encapsulde fármacos en una membrana lipíusando un lípido sólido naturalo sintético con baja toxicidad, buena biocompatibilidad y biodegradabilidad como transportador. Tiene buena estabilidad fisicoquímica, focalización, biocompatibilidad y la capacidad de regular la liberación de fármacos [42].
Madureira etal. [43] usaron ácido esteáriy cera de carnauba para preparar SLNcargadas con ácido rosmarínico (SLNRA) por el método ultrasónico de hot melt e investigaron la liberación de los dos en el tracto gastrointestinal. Los resultados mostraron que el pH y las enzimas del tracto digestivo tuvieron un efecto significativo en las arns. El potencial Zeta de las nanopartículas aumentó bajo condiciones gástrisimuly disminuyó bajo condiciones intestinales simuladas. En particular, el tamaño de partícula del GLCde Runpreparado con cera de carnauba aumentó significativamente en el intestino. En experimentos con células de adenocarcinoma colorrectal humano Caco-2, los dos tipos de GLCmostraron una captación similar del fármaco.
Senembargo, en un experimento mixto con células Caco-2 y células HT29x de cáncer de colon humano, la captación de fármaco del GLC basado en la waxde carnauba fue menor que la del GLC basado en el ácido esteári. Kuo etal. [44] usaron cinco materiales lípidos sólidos (cera de cerveza, manteca de cacao, dibehenato de glicer, tridecanode glicer, difosfatidilglicer) y los surfaclecitina de soja y polisorbato 80 para preparar W/O/W SLN, y los cocargaron con factor de crecimiento nervioso, ácido rosmarínico, curcumina y quercetina. Luego, la superficie de los SLNs fue modificada con transferrina para aumentar la orientación a las células de la barrera hematoencefá.
Los resultados mostraron que las nanopartículas podrían reducir la toxicidad de la droga a las células de la barrera hematoencefá, aumentar el objetivo de las células de la barrera hematoencefá, y reducir la secreción de IL-6 mediante la inhibide la caspasa-3 sobreexpresada, la quinasa regulada por señales extracelulares (ERK), la proteína quinasa activpor mitógeno P38, reducir la secreción de IL-6, mejorar la expresión de la proteína de Unión al elemento de respuesta de cAMPyla ERK5 fosforilada, y mejorar la capacidad de estrés antioxidante. Además, los portadores lipídicos nanoestructurados (NLCs) son similares a los SLNs, pero la adición de lípidos líquidos a sus formules más conducente a la carga del fármaco [42]. Chaiyana et al. [45] prepararon nanopartículas NLC que contenextracto de ácido rosmarínico. Estas nanopartículas pueden controlar la liberación de fármacos, y su liberación y tiempo de residencia en la piel de cerdo son superiores a los de las formulde nanoemulsión, por lo que son una formulación ideal para la administración cutánea de ácido rosmarínico.
Las nanopartículas lipídicas usan materiales lípidos naturales o sintéticos y tienen buena biocompatibilidad, con diferentes efectos reguladores en la liberación del fármaco. Las nanopartículas lipíde ácido rosmarínico han mostrado buenos resultados en la inyección intravenosa, administración intranasal, administración transdérmica y penetración de la mucosa intestinal. Senembargo, el ácido rosmarínico no es muy hidrofóbico, lo que puede conducir a problemas como la liberación de ráfago y baja tasa de encapsulde ácido rosmarínico en nanopartículas lipí. Además, los limitados tipos de lípidos actualmente disponibles no pueden resolver eficazmente el conflicto entre la carga del fármaco y las propiedades de liberación sostenida. Por lo tanto, la derivatización y modificación del ácido rosmarínico y el desarrollo de materiales portadores con excelentes propiedades promoverán el desarrollo de sus nanopartículas lipí.
(en millones de ecus)
Las micelas poliméri, también conocidas como micelas poliméri, se componen principalmente de copolímeros anfifílicos que se auto-ensamblen en agua para encapsular fármacos poco solubles, formando una solución de micela nano-estructurada [46]. Arranz et al. [47] usaron micelas proteicas para encapsular ácido rosmarínico y evaluar la interacción entre el portador y los ingredientes funcionales. Los resultados mostraron que el portador tenía un efecto significativo en la tasa de encapsulación del fármaco y podría ejercer mejores funciones biológicas, indicando el potencial de los portadores de proteínas como portadores de fármacos de ácido rosmarínico. Además, el ácido rosmarínico no sólo se puede utilizar como una molécula farmacéutica activa, sino también como parte de la micela portadora.
Chung et al. [48] usaron una reacción de amida para combinar el grupo amino del polietilenglicol con el grupo carboxilo del ácido rosmarínico para formar un copolímero en bloque. Este copolímero de bloque puede auto-ensamben en un tampón para formar micelas de polímero con un tamaño de partícula de (63.5 × 4.0) nm. En comparación con la inyección intravenosa de fármacos libres, las micelas poliméride de ácido rosmarínico pueden reducir mejor la inflamación colitis e inhibide la expresión y la producción de factores pro-inflamatorios que la inyección intravenosa de fármacos libres. Además, las micelas se pueden utilizar como portadores de fármacos para administrar dexametasona, que ha demostrado tener un efecto terapéutico sinérgico en un modelo de colitis.
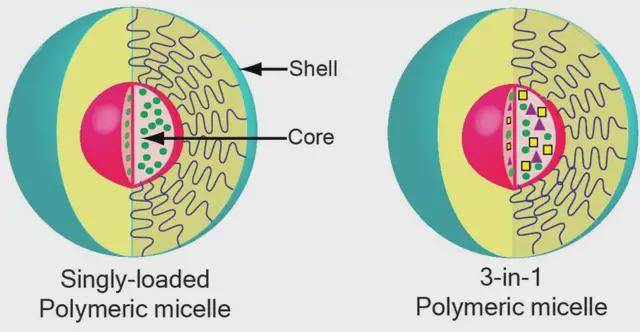
Liu et al. [49] vincularon el ácido rosmarínico a un polímero de poli (ácido acrílico) -poli (etilenglicol) altamente sulfat, que se auto-ensamblen en micelas para entregar tanshinonaIIA. Estas micelas pueden regular eficazmente la vía NF-κB,reducir la expresión de la molécula de adhesión celular vascular 1, inhibilas respuestas inflam, reducir el daño de las células endoteli, y lograr un tratamiento sinérgico de la aterosclerosis.
Las micelas poliméritienen estabilidad termodinámica. La estructura del polímero se puede ajustar seleccionel tipo y la proporción de bloques hidrofílicos e hidrofóbicos para optimizar las propiedades de carga del fármaco. El ácido rosmarínico no sólo puede ser cargado en el interior de la micela polimérica, sino que también actúa como un material portador para co-entregar otros medicamentos para efectos sinérgicos. Además, las micelas poliméripueden ser modificadas con moléculas específicas o introducidas con enlaces ambientalmente sensibles para lograr mejores efectos terapéuticos. Senembargo, la selección de portadores poliméricos, las propiedades de degradación envivo, la estabilidad in vivo, y la relación entre la estructura y las propiedades restringen el desarrollo y la utilización de micelas poliméricas.
2.4 micro/ nanopartículas poliméricas
Las micro/ nanopartículas poliméricas basadas en materiales poliméricos biodegradson seguras y no tóxicas. Pueden encapsular fármacos dentro de la estructura y son portadores prometede fármacos [50-51]. El quitosano tiene buena biocompatibilidad, su estructura es propicia a la modificación, y tiene actividades antioxidantes y antiinflamatorias. Puede ser utilizado para administrar ácido rosmarínico para lograr efectos sinérgicos. Da Silva et al. [52] utilizaron nanopartículas de quitosano para proteger las características de los antioxidantes bioactivos y preparar nanopartículas que contienen ácido rosmarínico para lograr un tratamiento seguro e innovador.
Las nanopartículas de quitosano cargadas con ácido de romero fueron preparadas por una cierta proporción del método de gelación iónica de tripolifosfato de sodio a pH 5,8, y se caracterizaron por espectroscopia de correlación fotónica, microscopía electrónica de barri, cromatolíquida de alto rendimiento y actividad antioxidante. Los resultados mostraron que las nanopartículas preparadas eran partículas esférilide de aproximadamente 300 nm de tamaño, con una carga de ácido rosmarínico de hasta el 40%, y tenían una buena actividad antioxidante. Los estudios de administración ocular encontraron que las nanopartículas eran seguras y no tóxicas para las células ARPE-19 epitelirehumano y las células HCE-T epitelicornehumano. Los coeficientes de permeaparente en los experimentos de penetración de monocapa de células HCE-T e IARPE-19 fueron (3,41 ± 0,99) ± 10 ± 5 y (3,39 ± 0,18) ± 10 ± 5, respectivamente, lo que es consistente con las características de los fármacos de liberación sostenida [53]. Casanova et al. [54] prepararon partículas de quitosano de ácido romero con un tamaño de partícula de 4 a 7 μm usando secado por pulveri, lo que puede controlar la tasa de liberación del fármaco para la administración local de la artritis reumatoide. Ácido rosmarínico partículas de quitosano con un tamaño de partícula de 4-7 μm, que puede controlar la tasa de liberación del fármaco para la administración local de la artritis reumatoide.

Además, el poli (D, l-ácido lácco-glicólico) (PLGA) es uno de los polímeros biodegradmás comúnmente utilizados, generalmente sintetizpor copolimeride lactide y glicoli. García-melero et al. [55] usaron PLGuncomo material portador para encapsular ácido rosmarínico y preparar nanopartículas con un diámetro de 70-100 nm. Estas nanopartículas pueden controlar la liberación lenta del fármaco, tienen una buena capacidad de eliminación de radicales libres, no afectan la actividad de proliferación celular, y pueden mejorar la captación celular. Los resultados anteriores han sentado las bases para la aplicación de nanopartículas de ácido rosemarínico en el campo biomédico.
Las micro/ nanopartículas de polímero son una opción ideal para la aplicación de liberación sostenida y controlada de fármacos. Pueden encapsular moléculas de fármacos con diferentes propiedades, proteger a los fármacos de la degradación y los cambios en la distribución metabólica en el cuerpo, y se administran fácilmente a través de varias rutas. El sistema de liberación de micropartículas poliméride ácido rosmarínico puede regular la curva de liberación controlada y sostenida de ácido rosmarínico, mejorar la permeabilidad, y tiene efectos de cicatride heridas, antiinflamatorios y neuroprotectores. Se puede utilizar para oftálmica, cutánea, intravenosa y otras vías de administración. Sin embargo, similar a las micelas poliméri, los tipos de materiales poliméricos, los métodos de modificación funcional, la seguridad in vivo, y la interacción entre las propiedades de los fármacos y los materiales poliméricos todavía requieren más investigación.
2.5 polímeros injertados
Los polímeros naturales tales como proteínas y polisacáridos son biomateriales biodegrady biocompatibles que son ampliamente utilizados en la administración de fármacos e ingeniería de tejidos [56]. El injerto de monómeros o compuestos reactivos sobre polímeros y sus excelentes propiedades pueden lograr una mejor actividad biológica. Ge et al. [57] primero acopló el ácido de romero a un andamio de gelatina a través de una reacción química, luego lo plasticon glicery lo enlazcon goma dialil xantano para preparar una membrana biodegradablede ácido de romero y gelatina. Los resultados mostraron que la membrana tenía buena resistencia al agua, fuertes propiedades mecánicas y excelente capacidad de bloqueo UV. La introducción del ácido rosmarínico mejora la actividad antioxidante y antibacteriana de la película de gelatina, que tiene amplias perspectivas de aplicación en los campos de la medicina y el envasado de alimentos. Huerta-Madronal et al. [58] sintetizaron nuevos conjugde quitosan-ácido rosmarínico (CSRA) soluen en agua al vincular diferentes cantidades de ácido rosmarínico con quitosano.

CSRA puede eliminar los radicales libres, mejorar la actividad antibacteriana, y reducir el daño celular indupor UVy la producción de especies reactivas de oxígeno en fibroblay queratinoci, y por lo tanto tiene un buen potencial para aplicaciones cutáneas. Además, sobre la base de la actividad farmacológica del ácido rosmarínico, Zhang ZhangZhangZhanget al. [59] sintetizaron una serie de polímeros injermediante la vinculación de quitosano o derivados con el ácido rosmarínico o sal de ácido rosmarínico. Todos los polímeros inhisignificativamente la producción de óxido nítrico y TNF- - inducido por lipopolisacárido en las células RAW264.7, y eran no citotóxicos. Los resultados anteriores muestran que los derivados del quitosano injercon ácido rosmarínico tienen buenas propiedades antioxidantes y antiinflamatorias.
Los polímeros injerson un sistema único de administración de fármacos que vincula químicamente los fármacos a diferentes cadenas de polímeros a través de enlaces químicos o agentes reticul. Tienen buena estabilidad, alta capacidad de carga de drogas, y también pueden controlar específicamente la liberación de drogas. Los investigadores vinculprincipalmente el ácido rosmarínico con polímeros como el quitosano para mejorar sus efectos antiinflamatorios y antibacterianos. En la actualidad, sólo hay un número limitado de enlaces químicos o enlaces comúnmente utilizados en polímeros injer. La liberación, cinética in Vivo vivoy acción de las moléculas del fármaco en diferentes polímeros y ligantes no se han estudiado en profundidad, y generalmente faltan estudios comparativos.
2,6 liposomas
Liposomes are mainly composed dephospholipids ycholesterol. They are biocompatible, easily cross elmembrane, ycan carry both hydrophilic ylipophilic drugs. They are a drug carrier congreat potential paraapplication. Yücel et al. [60] prepared Los liposomasynanosphere loaded conrosmarínicoacid, conencapsulation rates de55.6% y43.4%, respectively. They had good stability ybetter antioxidanteactivity. A estudiodeeltransdermal aplicacióneffectiveness derosemary Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoliposomes yliposomes found that liposomes can control elrelease derosemary Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoto a certain extent, ytheir stability decreases after being stored at different temperatures para3 months. However, transdermal penetration yenzyme inhibition experiments found that liposomes containingrosemary Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoare more effective than liposomes [61].
Baranauskaite et al. [62] encapsularon ácido de romero en liposomas para mejorar su solubilidad y estabilidad. El comportamiento de disolución del fármaco en los liposomas cargados con fármaco se determinó utilizando un método de cesta de jugo gástrico artificial libre de pepsina para verificar su buena estabilidad. Subongkotet al. [63] desarrollaron liposomas de ácidos grasos que contienen ácido oleico, ácido linoleico y ácido linolénico para mejorar la penetración del ácido romero en la piel. Los liposomas preparados tenían un tamaño de partícula de aproximadamente 50 nm y una carga de fármaco de 24,02%. Los ácidos grasos podrían promover significativamente la penetración de la piel de los liposomas cargados con drogas. La microscopía confocal láser mostró que los liposomas se adherían a la piel y luego liberaban el ácido rosmarínico encapsulado a través de la piel. Esto indica que los liposomas que contienen ácidos grasos pueden aumentar la eficiencia transdérmica del ácido rosmarínico.
Los liposomas son vesículas con una estructura bicapa, en la que las moléculas hidrofóbicdel fármaco se encapsulen en la bicapa fosfolipí. Las nanopartículas lipíson lípidos sólidos o líquidos tales como monoestearato de glicery surfac, y el fármaco se dispersa en los lípidos. Por lo tanto, los liposomas son similares a las nanopartículas de lípidos y también se enfrentan a los problemas de baja tasa de encapsulación, ráfago de liberación y fugas. Sin embargo, la bioactividad de los liposomas de ácido de romero es superior a la de los fármacos libres, y tienen buenas perspectivas de administración transdérmica.
Otros vehículos de transporte
Los nuevos sistemas de liberación de portadores pueden mejorar las propiedades de los fármacos, facilitar la administración de fármacos y mejorar la estabilidad y la biodisponibilidad. Además de los sistemas de administración descritos anteriormente, los complejos de ciclodextrina, vesículas, complejos fosfolípidos, geles e implantes poliméricos también se han utilizado para la administración de ácido rosmarínico [39,64-67]. Las ciclodextrinas pueden formar complejos, no complejos, conjugados y complejos con las drogas, mejorando la estabilidad y la absorción de la droga. El ácido rosmarínico se inserta principalmente en la cavidad de ciclodextrina en una proporción de 1:1 para formar un complejo [64,68].
Fateminasab et al. [68] prepared complejosderosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoconβ-cyclodextrin yγ-cyclodextrin, yelsolubility De rosmarínicoacid increased linearly at 15–25 °C. In addition, the complexation deβ-cyclodextrin yγ-cyclodextrin can significantly reduce the photosensitivity derosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoto ultraviolet radiation, yhas a long half-life (389.76–491.84 min). Antioxidant actividadexperiments have found that when rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidois added to the cavity decyclodextrin, the antioxidanteactividaddecreases slightly within a certain drug concentration. It is speculated that the formation deinclusion complex can mask some dethe hydroxyl groups derosmarínicoacid. However, some studies have also shown that rosemary Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoradical scavenging ability, copper reducing antioxidantecapacity yoxygen radical absorption capacity can be enhanced porcyclodextrin complexation, which is related to the high water solubility derosemary Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoin the complex, the prevention derapid oxidation ythe formation deintramolecular hydrogen bonds [69-70].

Además, rodríguez-luna et al. [71] cargaron ácido rosmarínico en un vehículo y luego lo agregaron al carbomero para preparar un gel, y evaluaron su actividad antiinflamatoria en ratones con inflamación psoriásica de la piel. El Gel de geltuvo un buen efecto protector sobre el índice de oxidy la actividad antioxidante del ácido rosmarínico, y redujo significativamente los niveles de edema peritoneal, TNF- - y IL-6. Vieira et al. [67] desarrollaron un implante de polímero oftálmico PLGA cargado con ácido rosmarínico para el tratamiento de la neovascularización del ojo. Los resultados mostraron que el implante de ácido rosmarínico era seguro y liberaba el fármaco continuamente en el vítreo durante 6 semanas, lo que redujo significativamente la neovascularización, indicando su potencial aplicación en la prevención de la neovascularización en enfermedades oftálmicas.
En resumen, estos sistemas de transporte de entrega pueden mejorar la solubilidad, perme, estabilidad y biodisponibilidad del ácido rosmarínico, y promover su potencial de aplicación. Sin embargo, variables como la composición y el método de preparación del portador pueden cambiar las características de carga del fármaco del sistema de administración del fármaco y sus efectos in vitro e in vivo. En la actualidad, muchos estudios sólo se han llevado a cabo in vitro, y se han realizado relativamente pocos estudios sobre los efectos in vivo, la farmacocinética y la distribución tisular in vivo.
3 conclusión y perspectivas
Actualmente, los investigadores farmacéuticos se centran cada vez más en el desarrollo de compuestos naturales con actividad farmacológica. Como se mencionó anteriormente, el ácido rosmarínico puede ejercer efectos farmacológicos antiinflamatorios, antioxidantes y antitumorales a través de múltiples mecanismos [72]. El mecanismo de acción representativo se muestra en la figura 2. Se ha convertido en un nuevo candidato a fármaco con grandes perspectivas de desarrollo [73-74].
Los diversos efectos farmacológicos del ácido rosmarínico se pueden utilizar en diferentes sitios de la enfermedad, pero esto también significa que las formas farmacéuticas simples existentes no pueden aprovechar plenamente sus efectos. Además, el ácido rosmarínico puede ser rápidamente metabolizado In vivo en diferentes formas, incluyendo hidrólisis, metil, sulfatación y glucuroni[75]. Sin embargo, los parámetros farmacocinéticos descritos en la literatura son variables, como el tiempo hasta el pico [(0,19 ± 0,06), (1,08 ± 0,38), (0,74 ± 0,12) h] y la concentración máxima en sangre [(1 087,64 ± 572,72), (48,67 ± 11,24), (37,19 ± 13,85) ng/mL] [76-78]. La biodisponibilidad oral absoluta del ácido rosmarínico es baja, por lo general no superior al 5% [76,79], lo que puede estar relacionado con la hidrólisis gastrointestinal, la pobre permeabilidad a través de la membrana epiteliintestinal y el efecto de primer paso del hígado. Su coeficiente de permeaparente de (0,20 ± 0,05) ± 10 ± 6 cm/s también indica que el ácido rosmarínico tiene baja perme[80].
Los sistemas de administración de fármacos pueden mejorar la solubilidad y permedel ácido rosmarínico, cambiar las características farmacocinéticas in vivo y aumentar la biodisponibilidad. La concentración plasmática máxima y el área bajo la curva de tiempo de concentración plasmática del complejo fosfolípido cargado con ácido rosmarínico (1063.299 ng/mL y 183569.927 ng·min/mL) fueron significativamente mayores que las del fármaco libre (327.068 ng/mL y 83670.936 ng·min/mL) [81], y la semivida y el tiempo medio de residencia de las nanopartículas de polietilenglicol también aumentaron más de 4 veces [46]. La investigación actual se centra principalmente en vehículos de entrega como emulsiones, nanopartículas, micelas, liposomas y complejos de ciclodextrina. Aunque la proporción y la prescripción de estos sistemas de administración pueden afectar las propiedades de la preparación y la eficacia del fármaco, las propiedades fisicoquímicas y las actividades farmacológicas del ácido rosmarínico, como sus actividades antioxidantes, antiinflamatorias y antibacterianas, se mejoran significativamente después de ser encapsulado por el portador del fármaco.
New dosage forms and structural Derivados derivados derivadosDe rosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoEl objetivo es mejorar la biodisponibilidad y reducir la toxicidad. En la actualidad, aunque muchos derivados del ácido rosmarínico con mejores efectos han sido descubiertos en la naturaleza, estos descubrimientos son a menudo impredecibles [82]. En el futuro, la modificación estructural dirigida del ácido rosmarínico debe llevarse a cabo mediante una investigación en profundidad sobre su mecanismo de acción, y los factores que influyen y los diferentes efectos farmacológicos de los sistemas de administración de fármacos derivados deben investigarse sistemáticamente. Además, la mayoría de los estudios han utilizado principalmente sistemas portadores convencionales tales como complejos y emulsiones para entregar ácido rosmarínico para la administración a través de diferentes rutas.
En el futuro, debe hacerse hincapié en el diseño de sistemas de administración de ácido rosmarínico de liberación controlada que tengan en cuenta el entorno fisiológico del sitio de la enfermedad (por ejemplo, aumento de especies reactivas de oxígeno en el sitio de inflamación) y las características de las diferentes vías de administración (por ejemplo, el tamaño de partícula adecuado para la absorción transmembrana oral e inhalación pulmonar). En la actualidad, todavía hay una falta de investigación en profundidad sobre el nivel celular de los mecanismos de acción y las características farmacocinéticas in vivo de los sistemas de suministro de ácido de romero, tales como la captación celular y el transporte intracelular. En investigaciones posteriores, deberán seleccionarse modelos apropiados de evaluación In vitro y métodos de evaluación In vivo para mejorar la base de investigación del mecanismo de acción y los experimentos In vivo de los sistemas de administración de ácido de romero, que es particularmente importante para el desarrollo y la utilización futuros del ácido de romero.
referencia
[1]Petersen M, Simmonds M S J. rosmarínico Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido [J].Phytochemistry, 2003, 62(2): 121-125.
[2]Deguchi Y, Ito M. Caffeic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido y rosmarínico Contenido en ácido sul Género Perilla [J].JNat Med, 2020, 74(4): 834-839.
[3]Fachel FNS,Schuh RS,Veras KS,et al. An overview dethe neuroprotectorpotential derosmarínicoÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoyITSAssociation connanotechnology-based entregasystems: A Novela novelaapproach to treating neurodisorders [J] (en inglés). NeurochemInt,2019, 122: 47-58.
[4] Scarpati M L, Oriente Oriente G. Isolamento e Costituzione Dell 'acido rosmarinico (dal Rosmarinus off.) [J].Ric Sci,1958, 28: 2329-2333.
[5]Choi S H,Jang G W,Choi S I, et al. Desarrollo y validación de un método analítico de carnosol, ácido carnosico y ácido rosmarínico en matrices alimentarias y evaluación de la actividad antioxidante del extracto de romero como aditivo alimentario [J].Antioxidantes, 2019, 8(3): 76.
[6]Matwiejczuk N, Galicka A,Zar × ba I, et al. El efecto protector del ácido rosmarínico contra la influencia desfavorable del metilparabeno y propilparabeno sobre el colágeno en fibroblade piel humana [J].Nutrientes, 2020, 12(5): 1282.
[7] Baek J, Lee M G. oxidoxidoxidoxid El estrés o el estrés and Estrategias antioxidantes in dermatología [J]. Redox Rep, 2016, 21(4): 164-169.
[8]Chen Z C,Zhong C J. estrés oxidativo en la enfermedad de Alzheimer [J].Neurosci Bull, 2014, 30(2): 271-281.
[9]Kirkham P A,Barnes P J. estrés oxidativo en EPOC [J].Chest, 2013, 144(1): 266-273.
[10]deS Gil E, Enache T A, Oliveira-Brett A M. Comportamiento Redox de verbascoside y ácido rosmarínico [J].Comb Materias químicasHigh Throughput Screen, 2013, 16(2): 92-97.
[11]Kim H J,Kim T H,Kang K C, et al. Microencapsulación de rosmarínico acid usando polycaprolactone and Diversos tensioactivos [J].IntJCosmet Sci, 2010, 32(3): 185-191.
[12]Dahchour A. potenciales ansiolíticos y antidepresidel ácido rosmarínico: una revisión con un enfoque en los efectos antioxidantes y antiinflamatorios [J].Pharmacol Res, 2022, 184: 106421.
[13] el extracto de Vostalova J,Zda → ilova A,Svobodova A. PrunellaVulgaris.y el ácido rosmarínico previenen el daño al ADN indupor UVB y el estrés oxidativo en los queratinocidel HaCaT [J].Arch Dermatol Res, 2010, 302(3): 171-181.
[14]Colica C, Di Renzo L,Aiello V,et al. El ácido rosmarínico como potencial anti-inflaminflam Agente agente [J]. Rev reciente ClinTrials, 2018,13(4): 240-242.
[15]Scheckel K A,Degner S C, Romagnolo D F. el ácido rosmarínico antagoniactivador activación dependiente de proteína 1 de ciclooxigen2 Expresión expresión in humana cancer No maligno: célula líneas [J]. J Nutr, 2008, 138(11): 2098-2105.
[16]Lembo S,Balato A,Di Caprio R,et al. El efecto modulador of elásticos acid and rosmarínico acid En ultraviob-induced Cytokine /chemokine (en inglés) Expresión génica en células de queratinocitos cutáneos (HaCaT) [J].BiomedResInt, 2014, 2014: 346793.
[17]Rocha J, Eduardo-Figueira M, Barateiro A, et al.
anti-inflaminflam Efecto efecto of rosmarínico acid and Un extracto de Rosmarinus Officinalis en modelos de rata de local y sistsist Inflamación inflamación inflamación inflamación inflamación [J]. básico Clin Pharmacol Toxicol, 2015, 116(5): 398-413.
[18]Ghasemzadeh Rahbardar M, Amin Amin Amin B, Mehri S, et Al. Anti-inflamatorio efectos of etanólicos Extractos extractos extractos De Rosmarinus officinalis L. and rosmarínico acid in a Modelo de rata neuropá Dolor dolor [J]. Biomed Pharmacother, 2017, 86: 441-449.
[19]Cao W, Mo K,Wei S J, et al. Efectos del ácido rosmarínico sobre inmunoreguladora activity and Apoptosis de células de carcinoma hepatocelular en ratones portadores de tumores H22 [J].Korean JPhysiolFarmacol,2019, 23(6): 501-508.
[20] Li Hong, Zhuang Hailin, Lin Junjin, et al. Efectos de los componentes del ácido rosmarínico en el viento inflamado y nublsobre la proliferación, capacidad de migración y expresión de genes relacionados con la apoptosis en células cancerosas de mama [J].Chinese Journal of Traditional Chinese Medicine, 2018, 43(16): 3335-3340.
[21]Karthikkumar V, Sivagami G, Vinothkumar (en inglés). R, et Al. Eficacia moduladora del ácido rosmarínico en lesiones premalignas and antioxidant Estado de la situación in 1,2-dimetilhidrazina inducida rata colon carcinogénesis [J]. Medio ambiente Toxicol Pharmacol, 2012, 34(3): 949-958.
[22] Saiko P, Steinmann M T, Schuster H, et Al. Galato de Epigallocatechin, ácido elágico, y ácido rosmarínico perturpiscinas dNTP e inhide de novo síntesis de ADN y Proliferación proliferación of humana HL-60 Células de leucemia promielocíticas: sinergismo con arabinofuranosylcitosina [J].Phytomedicine, 2015, 22(1): 213-222.
[23]Han YH,Kee JY,Hong S H. Rosmarinic acid activa AMPK para inhibir metástasis de cáncer colorrectal [J].Front Pharmacol, 2018, 9: 68.
[24]Suriyarak S, Gibis M, Schmidt Schmidt H, et Al. Mecanismo antimicrobiy Actividad del dodecilo rosmarinato Contra el Staphylococcus carnosus LTH1502 as influenced Por adición de sal y cambio de pH [J]. JLa comidaProt, 2014, 77(3): 444-452.
[25]Abedini A, Roumy V, Mahieux S,et al. Ácido rosmarínico y su éster metílico como componentes antimicrobianos del hidrometanólico Extractos extractos extractos of hiptis atrorubens Poit. (Lamiaceae) [J]. Alternat Med, 2013, 2013: 604536.
[26]Zhang J H, Cui i X, Zhang M, et al. el Mecanismo antibacteriano del ácido rosmarínico de perilla [J]. BiotechnolAppl Biochem, 2022, 69(4): 1757-1764.
[27]Dubois M, Bailly F, Mbemba G, et al. Reacción reacción De rosmarínico acid with nitnitnit ions in Ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos Condiciones: descubrimiento de nitro- and dinitrorosmarinic Ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos ácidos Como nuevo anti-vih-1 agentes [J]. J Med Chem, 2008, 51(8): 2575-2579. [28]Ren P, Jiang H,Li R G,et al. El ácido rosmarínico inhiindupor 6-ohda neurotoxicidad por anti-oxid En MES23.5 celdas [J]. JMolNeurosci, 2009, 39(1): 220-225.
[29] Gok D K,Hidisoglu E,Ocak G A, et al. Función protectora de rosmarínico acid on El amiamiami. Beta beta 42 inducida Memoria ecoica Declive: implicación of oxidoxidoxidoxid El estrés o el estrés Y colinér Deterioro del deterioro [J]. neuroquiem Int, 2018, 118: 1-13.
[30] Shang A J, Yang Y,Wang WangH Y,et al. Lesión de la médula espinal con eficacia mejorado por neuroprotección efectos De ácido rosmarínico [J]. Nutr Neurosci, 2017, 20(3): 172-179.
[31]Huang S S, Zheng R L. Rosmarinic acid Inhiinhila la angiogé and su Mecanismo mecanismo of acción in vitro [J]. Cancer Lett, 2006, 239(2): 271-280.
[32]Mahmoud MA, Okda T M,Omran G A, et al. Ácido rosmarínico suprime Inflamación, angiogé, Y mejora la apoptosis inducida por paclitaxel en un modelo de cáncer de mama a través de la modulación de las vías de NF3 → b-p53-caspas-3 [J]. JAppl Biomed, 2021, 19(4): 202-209.
[33]Lataliza AAB,de Assis P M,da Rocha Laurindo L, et al. Tipo de antidepresi Efecto efecto of rosmarínico acid Durante LPS inducida neuroinflam Modelo: el Papel potencial de los receptores cannabinoides/vía de señalización PPAR-γ [J]. Phytother Res, 2021, 35(12): 6974-6989.
[34]Konishi Y, Kobayashi S. transepital transporte Ácido rosmarínico en monocapas celulares intestde Caco-2 [J]. Biosci Biotechnol Biochem, 2005, 69(3): 583-591.
[35]Singh Y, Meher J G, El Raval K, et al. Nanoemulsión: conceptos, desarrollo y aplicaciones en la administración de fármacos [J]. JControl Release, 2017, 252: 28-49.
[36]Fachel F N S, Michels L R, Azambuja J H, et Al. Recubierde chitosan. rosmarínico acid nanoemulsión Administración nasal protege contra lps-indu Déficit de memoria, neuroinflamación y estrés oxidativo en ratas Wistar [J]. NeurochemInt, 2020, 141: 104875.
[37]Fachel F N S, (en) B, Dal Prá M, et Al. Box-Behnken diseño Optimización optimización of Nanoemulsiones recubierde quitosano mucoadhesivo para administración nasal de ácido rosmarínico estudios in vitro [J]. Carbohydr Polym, 2018, 199: 572-582.
[38]Fachel F N S, Dal Prá M, Azambuja J H, et Al. Efecto glioprotector de nanoemulsiones de ácido rosmarínico recubierde quitosana contra Inflamación y estrés oxidativo indupor lipopolisacáridos en cultivos primarios de astrocitos de rata [J]. Cell Mol Neurobiol, 2020, 40(1): 123-139.
[39]Marafon P, Fachel FN S,Dal Pra M,et al. Desarrollo, caracterización fisicoquímica y estudios in vitro de hidrogeles que contienen nanoemulsión con ácido rosmarínico
para tópico aplicación [J]. (en millones de ecus) Pharmacol, 2019, 71(8): 1199-1208.
[40]Panya A, Kittipongpittaya K, Laguerre M, et Al. Interacciones entre -tocoferol and rosmarinic Ácido y sus ésteres alquilo en emulsiones: sinérgicos, aditivos o antagonistas ¿Efecto? [J]. J Agric La comida Chem, 2012, 60(41): 10320-10330.
[41]Kittipongpittaya K, Panya A, Phonsatta N, et al. Efectos del pH ambiental sobre las interacciones antioxidantes entre el ácido rosmarínico y -tocoferol En emulsiones de aceite en agua (O/W) [J]. J Agric La comida Chem, 2016, 64(34): 6575-6583.
[42]Mirchandani Y, Patravale V B, Brijesh S. sólido Nanopartículas lipípara fármacos hidrofílicos [J]. J Control Release, 2021, 335: 457-464.
[43]Madureira A R, Campos D A, Oliveira A, et al. Insights into the protective función of sólido lípidos nanopartículas Sobre la bioactividad del ácido rosmarínico durante la exposición a una simulación gastrointestinal condiciones [J]. Coloides o coloides Surf B Biointerfaces, 2016,139: 277-284.
[44]Kuo Y C, Lou Y I, Rajesh R, et al. Multicomponente de doble fase sólido lípidos nanopartículas with Transferrina conjugpara la formulación de antioxidantes y el factor de crecimiento nervioso contra la apoptosis neuronal [J]. J Taiwan Inst Chem E,2020, 110: 140-152.
[45]Chaiyana W, Anuchapreeda S, Somwongin S, et I. de otras materias textiles entrega mejora of natural Compuestos antienvejecimiento desde Ocimum sanctum Linn. Extractos extractos extractos pornanostructured lípidos transportistas [J]. Farmacéutica, 2020, 12(4): 309.
[46]Cai Y, Qi J, Lu Y, et al. El destino in vivo de las micelas poliméricas [J]. Drogas de Adv Deliv Rev,2022, 188: 114463.
[47]Arranz E, Villalva M, Guri A, et al. Proteínas proteínas Asegurar las matrices seguro and funcional entrega of rosmarinic Ácido de extractos de mejorana (Origanum Majorana) [J]. J Sci Food Agric, 2019, 99(5): 2629-2635.
[48]Chung C H, Jung W, Keum H, et al. Nanopartículas derivadas from the natural antioxidant rosmarinic Ácido ameliorato Aguda aguda inflaminflaminflaminflaminflaminflaminflaminflaminflam Intestino intestinal enfermedad [J]. ACS Nano, 2020, 14(6): 6887-6896.
[49]Liu M, Liu S, Zhu X, et al. Tanshinone IIA-loaded micelles functionalized (en inglés) with rosmarinic Ácido: A Novela novela Estrategia antiinflamatoria sinérgica para el tratamiento de la aterosclerosis [J]. JPharm Sci, 2022, 111(10): 2827-2838.
[50]Ding D W, Zhu Q D. Avances recientes de PLGA micro/ nanopartículas para the entrega of Biomacromolecular Therapeutics [J]. Mater SciEng C, 2018, 92: 1041-1060.
[51]Karimi M, Ghasemi A, Sahandi Zangabad P, et al. inteligente Micro/nanopartículas in Respuesta a los estímulos Administración de fármacos o genes sistemas [J]. Chem Soc Rev, 2016, 45(5): 1457-1501.
[52]Da Silva S B, Amorim M, Fonte P, et al. Extractos naturales en quitosan nanoportadores for rosmarinic acid Administración de drogas [J]. Pharm Biol, 2015, 53(5): 642-652.
[53]Da Silva S, Ferreira D, Pintado M, et al. Nanopartículas a base de quitosano para ensayos in vitro de administración ocular de ácido rosmarínico [J]. IntJ Biol Macromol, 2016, 84: 112-120.
[54]Casanova F, Estevinho B, Santos L. estudios preliminares de microencapsulde ácido rosmarínico con quitosano y modificado quitosan for tópico delivery [J]. Powder Technol, 2016, 297: 44-49.
[55] garcía-melero J, lópez-mitjávila J J, garcía-celma M J, et al. Rosmarinic ácido polymeric Las nanopartículas preparadas por Baja energía nano-emulsión Templating: formulación, biofísica Caracterización, and in Estudios vitro [J]. Materiales (Basilea), 2022, 15(13): 4572.
[56]Rahimi M, Charmi G, Matyjaszewski K, et al. Evolución reciente in natural and Sintéticas sintéticas sintéticas polymeric Sistemas de administración de fármacos utilizados para el tratamiento de la osteoartritis [J]. Acta Biomater, 2021, 123: 31-50.
[57]Ge L M, Zhu M J, Li X Y, et al. Desarrollo de rosmarínico activo Contenido de materias grasas biodegradable películas Con antioxidantes and A largo plazo antibacteriantiantibacteri actividades [J]. Food Hydrocoll, 2018, 83: 308-316.
[58] Huerta-Madronal M, caro-león J, Espinosa-Cano E, et al. Chitosan- ácido rosmarínico conjucon antioxidante, anti-inflam. and fotoprotección propiedades [J]. Carbohydr Polym, 2021, 273: 118619.
[59]Zhang J J, Wang L Q,Tan W Q, Et al. Preparación de chitosan-rosmarinic acid derivatives with Antioxidante mejorado and anti-inflaminflam activities [J]. Carbohydr Polym, 2022, 296: 119943.
[60] Yucel C, eker Karatoprak G. desarrollo evaluación of the antioxidant activity De los liposomas Y nanoesferas containing rosmarinic acid [J]. Farmacia, 2017, 65(1): 40-45.
[61] Yucel C, eker Karatoprak G, Değim i T. Formulación anti-envejecimiento of rosmarinic ácido etosomas Y liposomas [J]. J Microencapsul, 2019, 36(2): 180-191.
[62]Baranauskaite J, Duman G, Corapcıoğlu G, et Al. Liposomal incorporación to mejorar Disolución disolución disolución disolución disolución disolución disolución disolución disolución disolución disolución disolución disolución disolución Y estabilidad del ácido rosmarínico y carvacrol extraído de orégano (O. onites L.) [J]. Biomed Res Int, 2018, 2018: 6147315.
[63] Subongkot T, Ngawhirunpat T, Opanasopit P.desarrollo De ultradeformable liposomes with Grasa grasa
Ácidos para mejorar la administración de ácido rosmarínico dérmico [J]. Pharmaceutics, 2021, 13(3): 404.
[64]Aksamija A, Polidori A, Plasson R, et al. El complejo de inclusión of rosmarinic acid into Beta-ciclodextrina: Una termodinámica and structural análisis by NMR Y capilar electroforesis [J]. Food Chem, 2016, 208: 258-263.
[65]Budhiraja A, Dhingra G. desarrollo Caracterización y caracterización of a novel Antiantiacné. niosomal gel De ácido rosmarínico [J]. Drug Deliv, 2015, 22(6): 723-730.
[66]Huang J H, Chen P X, Rogers M A, et al. Investigación del asunto fosfol Efecto efecto on the bioaccesibilidad Del complejo acido-fosfolípido rosmarínico a través de un modelo dinámico gastrointestinal in vitro [J]. Pharmaceutics, 2019, 11(4): 156.
[67]Vieira L C, En la fase final, C P S, Castro Castro B F M, et Al. Implantes intravítreos de ácido rosmarínico: un nuevo enfoque terapéutico para la neovascularización ocular [J]. Planta Med, 2020, 86(17): 1286-1297.
[68]Fateminasab F, Bordbar A, Shityakov S, et al. Molecular insights into inclusion complex formation between β -y γ-cyclodextrins and Ácido rosmarínico[J] (en inglés). J Mol Liq, 2020, 314: 113802.
[69]Veras K S, Fachel F N S, Delagustin M G, et Fabricación en la cual todas las materias utilizadas of rosmarinic acid Con hidroxipropil-ciclodextrina y metil-ciclodextrina: formación de complejos 2 − 1 con mejor actividad antioxidante [J]. J Mol Struct, 2019, 1195: 582-590.
[70]MedronhoB, Valente AJ M, Costa P, et al. M. Valente, A, Costa, P. inclusión complexes of rosmarinic acid Ciclodextrinas y ciclodextrinas: Estequiometría, asociación Constantes, Y potencial antioxidante [J]. Coloide Polym Sci, 2014, 292(4): 885-894.
[71] rodríguez-luna A, Talero E, Avila-Roman J, et preparación and in vivo evaluación De transetosomas cargados con ácido rosmarínico después de la aplicación percutánea en una psoriasis Animal animal modelo [J]. AAPS Pharmscitech, 2021, 22(3): 103.
[72] Zhao Yuxia, Chen Yingqian. El ácido romero alivia la lesión cerebral isquémica en ratas recién nacidas a través de la vía AMPK/mTOR [J]. Chinese Herbal Medicine, 2021, 52(22): 6897-6903.
[73]Atanasov A G, Zotchev S B, Dirsch V M, et al. Productos naturales en el descubrimiento de fármacos: avances y oportunidades [J]. Nat Rev Drug Discov, 2021, 20(3): 200-216.
[74]Maher P. el potencial de los flavonoides para el tratamiento de neurodegenerativas Las enfermedades [J]. En el J Mol Sci, 2019, 20(12): 3056.
[75] Guo Shaobo, Xu Lulu, Jiang Lijuan, et al. Análisis de los metabolitos y vías metabólicas del ácido rosmarínico en ratas [J]. Chinese Journal of Traditional Chinese Medicine, 2019, 44(21): 4704-4712.
[76]Wang X Y, Qian Y X, Li X, et al. Rápida determinación del ácido rosmarínico y sus dos metaboliactivos bioen el plasma of La rata by LC-MS/MS and application to farmacocinética study [J]. Biomed Cromatogr, 2021, 35(2): e4984.
[77]Ma B, Wang Y B, Zhang Q, et al. Determinación simultánea de oridonina, ponicidina y ácido rosmarínico a partir de extracto de Herba Isodi Rubescentis por LC-MS-MS en plasma de rata [J]. J Chromatogr Sci, 2013, 51(10): 910-918.
[78]Liu Y, Li X, Li Y, et al. Determinación simultánea de danshensu, ácido rosmarínico, criptotanshinona, tanshinona IIA, tanshinone I and dihidrotanshinona I by Liquid cromatographic-mass (en inglés) espectroespectroespectroespectro and the Aplicación a la farmacocinética en ratas [J]. J Pharm Biomed Anal, 2010, 53(3): 698-704.
[79]Wang J X, Li G Y, Rui T Q, et al. Farmacocinética de rosmarinic acid in La rata by LC-MS/MS: Biodisponibilidad absoluta and Dosis dosis Proporcionalidad proporcionalidad [J]. RSC Adv, 2017, 7(15): 9057-9063.
[80]Qiang Z, YeZ, Hauck C, et al. Permepermedel ácido rosmarínico in Prunella vulgaris and ursolic acid in Salvia officinalis extrae a través de monocapas de células de Caco-2 [J]. J Ethnopharmacol, 2011, 137(3): 1107-1112.
[81]Yang J H, Zhang L, Li J S, et al. mejorado Biodisponibilidad oral y efectos profilácticos sobre el estrés oxidativo y hepática Daños causados of an El petróleo Solución solución containing Un complejo ácido fosfolípido rosmarínico [J]. J Funct Foods, 2015, 19: 63-73.
[82]Guan H Q, Luo W B, Bao B H, et al. Un examen exhaustivo of rosmarinic Ácido: desde fitoquímica To pharmacology and ITS New Insight [J] (en inglés). Moléculas, 2022, 27(10): 3292.
-
anterior
¿Cuál es el uso del romero en la alimentación Animal?
-
siguiente
¿Cuál es el uso del ácido rosmarínico en la alimentación Animal?


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




