¿Cuáles son los beneficios de Centella Asiatica?
Centella asiaticais the dried whole herb of the plant Centella asiatica (L.) Urb. in the family Apiaceae. It has the effects of clearing away heat and dampness, detoxifying and reducing swelling. It is mainly used to treat damp-heat jaundice, heatstroke diarrhea, stone dysuria, hematuria, carbuncle and swelling caused by toxin, bruises and contusions, etc.[1]. When previous scholars analyzed the chemical composition of Centella asiatica, they found that its main components include triterpenoids, essential oils, polyacetylenes, flavonoids, etc., and triterpenoids are the most abundant [2]. Madecassoside is a triterpenoid compound found in Centella asiatica. Its molecular formula is C48H78O19 and molecular weight is 959.12[3]. As one of the main pharmacologically active ingredients in Centella asiatica, madecassoside has a variety of pharmacological effects, such as anti-tumor, anti-inflammatory, protecting the nervous system, and promoting wound healing[4].

1. Efecto antitumoral y mecanismo del extracto de Centella asiatica
1.1. Inhibir la proliferación de células tumorales
Zhou et al. [5] Zhou et al. [5] mostraron que los asicosidos pueden inhibir la proliferación de células de cáncer colorrectal al inhibir la vía de señalización del factor de transcrinuclear κB (NF-κB). Además, los asicosidos también pueden inhibir la proliferación de células cancerosas de páncreas al inhibila fosforilación de la proteína quinasa activpor mitógeno P38 (p38MAPK) yla proteína NF- − B P65 [6].
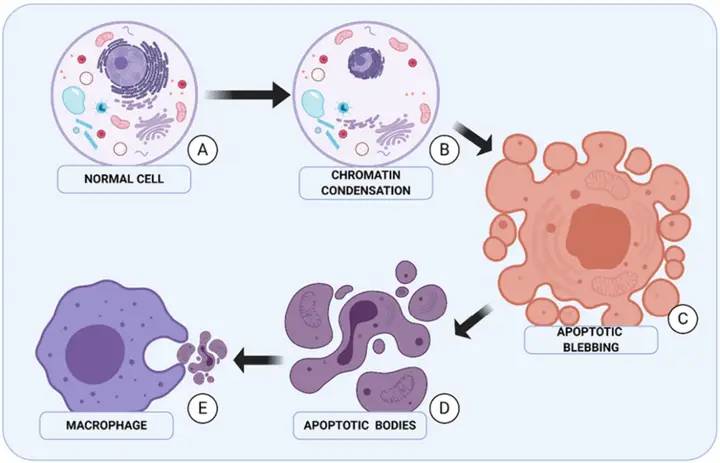
1.2 inducir apoptosis en células tumorales
Zeng Manhong et al. [7] usaron diferentes concentraciones de asiaticosidos para tratar las células de cáncer gástrico SGC-7901 y las células mostraron un pico apoptótico significativo. La microscopía electrónica de transmisión reveló características típicas de la apoptosis, tales como concentración citoplasmática, contracción y ruptura nuclear, y agregmitocon. El extracto de Centella asiatica también promueve la apoptosis en las células de cáncer de mama MCF-7: a medida que el tiempo de intervención del extracto de Centella asiatica se prolonga, la morfode las células MCF-7 se vuelve irregular, el citoplasma se disemina gradualmente, los núcleos primero se fusiony luego desaparecen gradualmente, formando finalmente cuerpos apoptóticos. Investigación adicional encontró que asiaticoside puede reducir significativamente los niveles de expresión de las proteínas del factor de crecimiento endotelial vascular (fcev) y del factor de crecimiento fibroblbásico (FCBF) en las células MCF-7 [8]. Wu Qian et al. [9] encontraron que diferentes concentraciones de asicosido pueden inducir apoptosis en las células del osteosarcoma Saos-2, y pueden reducir los niveles de expresión de fosfatidilinositol 3-quinasa (PI3K), proteína quinasa B (Akt), Akt fosforilada (p-Akt), glicógeno sintasa quinasa 3β (GSK-3β), glicógeno sintasa quinasa 3β (GSK-3β), lo que indica que asicosido puede inducir apoptosis en las células del osteosarcoma Saos-2 al regular la actividad de la vía de señalización PI3K/Akt/GSK-3β. Otros estudios también han demostrado que los asicosidos pueden inducir apoptosis en las células de cáncer de hígado QGY-7703 y Bel-7402 al inhibir la actividad de las vías de señal de la quinasa regulada por señal PI3K/Akt y MAPK/ extracelular regulada por señal quinasa (ERK) [10].
Bax, una proteína X relacionada con bcl-2-, pertenece a la familia Bcl-2 y es el principal regulador de la apoptosis en el cuerpo humano [11]. Pan Jinli [12] encontró que la inducción de la apoptosis en células de cáncer de ovaria2780 por asiaticoside puede estar relacionada con la regulación a la baja de la expresión del factor antiapoptótico Bcl-2 y la regulación positiva del factor proapoptótico Bax. Estudios relacionados han mostrado que después de 48 horas de actuar sobre las células de cáncer de mama MCF-7, asiaticoside induce significativamente apoptosis en las células, y el nivel de expresión de caspasa-3 (c-asiaticoside p-asiaticoside E-3) en las células se incrementa significativamente, el factor de necrosis tumoral (TNF- -) y la interleucina 1 - (IL-1 -) se redujeron significativamente [13-14]. Además, Li et al. [15] encontraron que los asiaticosidos pueden ejercer efectos antitumorales sobre la línea celular de mieloma resistente a los medicamentos KM3/BTZ. El mecanismo está relacionado con la inducde autofagia, la activación de la actividad c-asiaticoside p-asiaticoside E-3, y la inhibide la migración celular, la invasión, y el transducde señal y activador de la transcripción 3 (STAT-3) vía de señalización. Por lo tanto, asicoside puede inducir la apoptosis en las células tumorales mediante la regulación de la expresión de proteínas relacionadas con la apoptosis y la mediación de las vías de señal relacionadas con la apoptosis (como la vía de señal PI3K/Akt/GSK-3β), lo que inhila la proliferación, la migración y la invasión de las células tumorales.
2. Efecto Anti-fibrosis y mecanismo de asiaticoside
Estudios relacionados han encontrado que cuando la concentración de masa de asiaticoside es de 400 μg/mL, exhibe efectos inhibitsobre los fibroblade la piel embrionhumana y fibroblade los pulmones humanos [16-17]. En un experimento de fibrosis mesenquimal pulmonar de rata indupor pimecrolimus, se encontró que asiaticoside mejoró la fibrosis mesenquimal pulmonar indupor pimecrolimus al aumentar la regulación del nivel de expresión de los receptores de adenosina 2A (A2AR) y disminuir la regulación de los niveles de expresión de IL-4, TNF- - y transformar el factor de crecimiento beta 1 (TGF- ≤ 1) [18]. Zhu Dewei et al. [19] encontraron que los asiaticosidos pueden inhibir la producción de citocinas inflamatorias, reducir el nivel de expresión de TGF- ≥ 1 ARNm y ejercer un efecto antifibrótico.
Wang Ce [20-21] encontró que asiaticoside puede mejorar significativamente la fibrosis renal en ratas con obstrucción ureteral unilateral. El mecanismo puede estar relacionado con la regulación descendente de la expresión del factor de crecimiento del tejido conectivo (CTGF) y colágeno tipo III (Col III) en el intersticio renal. Además, el mismo autor también encontró que asiaticoside puede mejorar la fibrosis miocárdica después de infarto de miocardio en ratas. Zhao Sixia et al. [22] establecieron un modelo de rata con fibrosis hepática inmunpara investigar el efecto de asiaticosido en las concentraciones de alanina aminotransferasa (ALT) y aspartato aminotransferasa (asiaticoside T) en el suero e hidroxiprolina (Hyp) en el tejido hepático de la rata modelo. Los resultados mostraron que asiaticoside puede reducir el grado de fibrosis en el tejido hepático de la rata y redujo significativamente los niveles de ALT y asiaticoside T en el suero y el nivel de Hyp en el tejido hepático de ratas, lo que indica que asiaticoside tiene un efecto beneficioso sobre la fibrosis hepática mediada por inmunidad. Ji et al. [23] encontraron que los asiaticosidos pueden mejorar la fibrosis pulmonar inducida por bleomicina (BLM) en ratas y que el mecanismo de acción puede estar relacionado con la regulación de la vía TGF- ≥ 1/Smad.
Otro estudio encontró queAsiaticoside puede reducir significativamente el grado de fibrosisEn el tejido pulmonar de ratones con modelo de fibrosis pulmonar. Y el mecanismo de acción puede ser para mejorar la fibrosis pulmonar mediante la activación de la a2ar asistida por monofosfato cíclicde adenosina (cAMP)/R asperasociada proteína 1 (RAP1) vía de señalización [24]. Zhang et al. [25] indujeron fibrosis pulmonar en ratones de tipo silvestre (WT) y ratones con A2AR knockout (A2AR-/-) que usaron BLM y luego estudiaron el efecto de intervención de asiaticoside. Los resultados mostraron que los niveles de expresión de la proteína morfogenética ósea 7 (BMP7) y p-Smad1/5 en el tejido pulmonar de ratones WT y ratones A2AR-/- fueron significativamente elevados, lo que sugiere que asiaticoside puede reducir el grado de fibrosis pulmonar mediante la regulación ascendente de la vía de señalización BMP7/p-Smad1/5 a través de A2AR. Por lo tanto, asiaticoside puede reducir el grado de fibrosis en diversos tejidos y órganos, tales como el pulmón, hígado, riñón y corazón. Su mecanismo de acción está relacionado con la regulación descendente de TGF- − 1, CTGF, ALT, asiaticoside T y expresión de Hyp.
3 efecto antiinflamatorio y mecanismo de asiaticoside
La vía de señalización NF-κB está estrechamente relacionada con las respuestas inflamatorias y juega un papel importante en la regulación de las respuestas inflamcelulares. Cuando las células son estimuladas, NF- − B puede ser activado, lo que a su vez causa la sobreexpresión de factores inflamaguas abajo de la vía de señalización NF- − B, como TNF- -, IL- 1 -, IL-2, IL-6, óxido nítrico sintasa (iNOS), y ciclooxigenasa-2 (COX-2) [26]. Estudios relacionados han encontrado que, por un lado, asiaticoside puede ejercer un efecto antiinflamatorio mediante la inhibición de la vía de señalización NF-κB y la regulación de la expresión de óxido nítrico (NO), TNF- -, y IL-6 [27-28]. Por otro lado, los asiaticosidos también pueden ejercer un efecto antiinflamatorio regulando la vía de señalización de la heme oxigenasa 1 (HO-1), inhibiendo la producción de factores pro-inflamatorios y la actividad de la peroxid[29].
Como tal, puede reducir la respuesta inflamcausada por condiciones hipóxicas mediante la inhibición de la vía de señalización NF- − B/ P38 [30], y reducir la respuesta inflamcausada por condiciones hiperoxicas mediante la regulación negativa de la expresión de microRNA-155 (miR-155) y la regulación hacia arriba de la expresión de transducde señal y la proteína inhibi1 (SOCS1) [31]. El efecto protector del asiaticoside sobre el daño de las células endoteliindupor − -amilo1-42 (A − 1-42) puede lograrse mediante la inhibición de la liberación de IL-1, IL-6 y TNF- - de las células endoteli[32]. También se ha reportado que los asicosidos pueden inhibir la inflamación alérgica mediada por mastocitos, y el mecanismo puede estar relacionado con la vía del receptor de alta afinidad IgE (Fc − RI) [33]. Wu et al. [34] usaron la toxina de la rana de lluvia para replicar un modelo murde de pancreaguda leve para estudiar el efecto de intervención de los asiaticosidos. Los resultados mostraron que asiaticoside puede ejercer un efecto antiinflamatorio mediante la inhibide la vía TLR4 yla reducción de los niveles de expresión de la proteína quinasa reactiva 3 (RIP3) y fosforilated mixto linaje quinasa que contiene proteína de dominio (p-MLKL) en el tejido pancre. Por lo tanto, asiaticoside puede mejorar varias respuestas inflamatorias. Su mecanismo de acción está relacionado con la regulación negativa de la expresión de IL-6, IL-1 - y TNF- - en la vía NF- - B e inhibidel estrés oxidativo.
4. anti-alzheimer#39;s efecto de la enfermedad y mecanismo de asiaticoside
Alzheimer y#La enfermedad de 39;s (EA) es una enfermedad neurodegenercomún caracterizada por una disfunción cognitiva progresiva. Se ha encontrado que la patogénesis de la da está relacionada con la respuesta inflamatoria, la deposición anormal de A − y la apoptosis [35].
Según reportes de la literatura, asicoside puede aliviar la neuroinflamación al reducir el nivel de NO y la expresión de ARNm iNOS en astrocitos [36]. Cai Pengfei [37] encontró que los asiaticosidos pueden mejorar el daño causado por Aβ A las células endotelide la vena umbilical humana (HUVEC), y su mecanismo de acción puede estar relacionado con la inhibición de la apoptosis y la expresión de IL-1, IL-6 y TNF-α. Song et al. [38] estudiaron el efecto de la intervención de asiaticoside en la apoptosis indupor − 1-42 de las células endotelimicrovasculares (hBMECs) del cerebro humano. Los resultados mostraron que los asiaticosidos pueden inhibir la apoptosis de hBMECs, yel mecanismo de acción está relacionado con la inhibición de la vía de señalización TLR4/NF-κB, la expresión de TLR4, el factor de diferenciación mieloide 88 (MyD88), el factor 6 asociado al receptor del factor de necrosis tumoral (TRAF6), la proteína p-NF-κB P65 y la translocación nuclear de NF-κB, así como la expresión de TNF-α y IL-6.
Centella asiatica extracto can regulate the production of Aβ before neuropathy, thereby preventing the occurrence of AD [39]. Centella asiatica extract has a protective effect on HUVEC damage caused by Aβ1-42, and its mechanism of action may be related to up-regulating Bcl-2 expression and down-regulating Bax expression [40]. Xu et al. [41] found that aspertilloside has a significant reversing effect on 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP)-induced AD, and its mechanism of action is related to the increase in the Bcl-2/Bax ratio. Aspertilloside also has strong blood-brain barrier penetration and has the potential to treat neurodegenerative diseases [42]. Thus, asiaticoside can improve AD, and its mechanism of action is related to the inhibition of HU-VEC apoptosis, the activity of the TLR4/NF-κB signaling pathway, and the expression of the inflammatory factors IL-1, IL-6, and TNF-α.

5. The effect and mechanism of asiaticoside in improving learning and memory (en inglés)
Centella asiatica extract can improve learning and memory in mice, and its mechanism of action may be related to reducing the deposition of Aβ in hippocampal tissue and upregulating the expression of synaptophysin (SYN) protein [43-44]; it may also be related to upregulating the expression of peroxisome proliferator-activated γ receptor (PPARγ) protein and downregulating the expression of inflammatory factors IL-6, TNF-α, and IL-1 [45]. Related studies have found that asiaticoside also has a good preventive effect on cognitive dysfunction in diabetes, and its mechanism of action may be related to the regulation of oxidative stress and the PI3K/Akt/NF-κB pathway [46].
6. Efecto antidepresivo y mecanismo de asiaticoside
Wang et al. [47] usaron ratones modelo de estrés crónico leve (cm) para estudiar el efecto antidepreside los asiaticosidos. Los resultados mostraron que asiaticoside puede ejercer un efecto antidepresimediante la regulación de la ruta de señalización cAMP/ proteína quinasa A (PKA). Otro estudio encontró que los asicosidos pueden ejercer un efecto antidepresial activar la vía de señalización del factor neurotrófico derivado del cerebro (BDNF) [48]. Hou et al. [49] compararon los efectos antidepresidel asiaticosido y una fórmula asiaticosida-borneol (FAB) y encontraron que ambos tienen cierto efecto antidepresi; la FAB es más eficaz que el asiaticosido. FAB también tiene un efecto más significativo en la regulación ascendente de BDNF y seroton(5-HT) expresión.
7 el efecto y el mecanismo de asiaticoside en la inhibición de la hiperplasia cicatricial y reparación del daño cutáneo
Los estudios han encontrado que asiaticoside tiene ventajas únicas en la inhibición de la proliferación de la cicatriz y la reparación del daño de la piel: por un lado, asiaticoside puede mejorar la actividad de migración celular y aumentar la tasa de curación de heridas [50-51]; Por otro lado, los asiaticosidos pueden inhibila proliferación de fibroblacicatriy la síntesis de colágeno, inhibila proliferación de la cicatriz [52]. Experimentos In vitro han demostrado que el mecanismo por el cual asiaticoside inhila la proliferación de fibroblade la cicatriz puede estar relacionado con la inhibición de la expresión de proteínas que participan en la vía de señalización RhoA/Rho quinasa Ⅰ (RhoA/ROCK Ⅰ) [53], y también puede estar relacionado con la regulación a la baja de la expresión de colágeno tipo I y III y TGF- ≥ 1 ARNm [54]. Estudios relacionados han encontrado que en un modelo de cicatriz de oreja de conejo, a medida que el tiempo de administración aumenta, el área de la cicatriz disminuye gradualmente, y el mecanismo de acción puede estar relacionado con la expresión reducida de TGF- ≥ 1 [55]. Sobre esta base, Huang et al. [56] también encontraron que los asiaticosidos pueden inhibir la formación de cicatrices proliferativas en conejos al disminuir la regulación de la expresión del colágeno I y III y del ARNm de IL-1 -, IL-6 e IL-8, así como aumentar la regulación de la expresión del ARNm de Smad7 y PPAR -, y esto depende de la dosis. En otro estudio, se encontró que la razón para la inhibición de la formación de cicatriz por asiaticoside puede estar relacionada con la regulación de la expresión de la proteína de choque térmico 47 (HSP47) [57].
Wu Yanwen [58] estableció un profundo modelo de rata de segundo grado quemada e intervino con asiaticoside. Los resultados mostraron que los niveles de expresión de ciclina y del antígeno nuclear de células proliferantes (PCNA) en el tejido cutáneo de la herida de rata estaban elevados. Al mismo tiempo, asiaticoside puede inhibir la respuesta inflamatoria excesiva mediante la inhibide la translocación nuclear de la proteína NF-κB P65, lo que promueve la cicatride heridas y acortar el tiempo de curación. Zhu et al. [59] encontraron que las nanofibras coaxicargadas con asicosido pueden promover la curación de heridas profundas de quemaduras de segundo grado en ratas al aumentar la regulación de la expresión de VEGF, PCNA y moléculas de adhesión de células endoteli(CD31) y la regulación negativa de la expresión de TNF- - y IL-6. Además, el papel de asiaticoside en las diferentes etapas de la reparación de heridas es diferente: puede promover la proliferación de la cicatriz durante la fase proliferativa de la reparación de heridas, pero inhila la formación de cicatriz durante la fase plástica de la reparación de heridas [60]. Otro estudio encontró que los asiaticosidos también pueden promover la producción de la proteína quimiotáctica de monocitos 1 (MCP-1) para promover la cicatride heridas [61].
Nie et al. [62] found that the asiaticoside complex can reduce the inflammatory response in the wound of rats with diabetic skin ulcers (DCU) model, inhibit bacterial growth in the wound, promote wound healing, and upregulate the expression of VEGF, iNOS, endothelial nitric oxide synthase (eNOS) and CD34. The mechanism of action is related to downregulating the Wnt/β-catenin signaling pathway. Free skin flaps are a common means of skin burn and surgical repair. A skin flap is selected according to the skin defect, an area similar to the damaged skin is selected, and the flap is then transferred to the defect area for repair to achieve the purpose of repairing the skin defect [63]. A study found that asiaticoside can increase the survival area of skin flaps in rats, and the mechanism of action may be related to up-regulating the expression of superoxide dismutase (SOD) and VEGF and down-regulating the expression of inflammatory factors [64]. It has also been found that Centella asiatica-sodium alginate repair patches [65] and Centella asiatica nanoemulsions [66] prepared from asiaticoside have a good repair effect on skin damage.
Esto muestra que asiaticoside puede inhibila hiperplasia cicatriy reparar el daño en la piel. Su mecanismo de acción está relacionado con la inhibición de la expresión de colágeno tipos I y III y TNF- -, IL-6, y IL-1 -, así como la actividad de la vía de señalización Wnt/ - - catenina, y upreregulación de la expresión de TGF- - -1, VEGF, iNOS, y MCP-1.
8 The ameliorative effect and mechanism of asiaticoside on liver, Lung and Kidney damage (en inglés)
Los estudios han demostrado que asiaticoside tiene un efecto de mejora tanto en el daño pulmonar indupor la sepy lesión renal aguda en la sepsis. Por un lado, los asiaticosidos pueden inhibir la actividad de las rutas de señales MAPK y NF- − B mediante la regulación ascendente de la expresión de PPAR- -, mejorando así el daño pulmonar [67]. Por otro lado, la saponina de centella asiática puede mejorar el daño renal al regular la expresión de IL-6 en el suero y la expresión de la proteína iNOS en el tejido renal [68]. Zhang et al. [69] usaron un ratón modelo de daño hepático inducido por lipopolisacárido/d-galactosamina e intervinieron con centella asiatica saponin. Los resultados mostraron que ASG puede mejorar la lesión hepática mediante la inhibición de la expresión de TNF- - y MAPK. Además, Wang et al. [70] encontraron que el ASG puede mejorar la lesión renal en ratas con enfermedad renal, y el mecanismo puede estar relacionado con la regulación hacia arriba de la expresión de ARNm de la sinaptfisina, endorfinas y podocina y la regulación hacia abajo de la expresión de ARNm de la proteína juncional.
Dang et al. [71] estudiaron el efecto de asiaticoside en la mejora de la lesión pulmonar causada por la hiperoxia mediante experimentos in vitro e in vivo. Los resultados mostraron que asiaticoside puede reducir los niveles de mieloperoxid(MPO) y malondialdehído (MDA) en el suero de ratas con modelos de lesión pulmonar, así como los niveles de TNF- -, IL-1 - y IL-6, y aumentar el nivel de capacidad antioxidante total (TAOC), para ejercer su efecto de mejorar el daño pulmonar en ratas. Más experimentos in vitro usando células alveolde tipo II (AEC II) aisladas de tejido pulmonar de rata mostraron que asiaticoside puede inhibisignificativamente la apoptosis de células AEC II. El mecanismo de acción puede estar relacionado con la upreregulación de la expresión del factor nuclear relacionado con el factor 2 (Nrf2) y HO-1. Por lo tanto, asiaticoside puede mejorar el hígado, pulmón y daño renal, y su mecanismo de acción está relacionado con la inhibidel estrés oxidativo y la inflamación y la mejora de la capacidad antioxidante.
Otros 9
Estudios relacionados han encontrado que el asiaticosido puede usarse para prevenir el daño al ADN inducido por la radiación: después del tratamiento con radiación, los ratones tratados con asiaticoside tuvieron mayores tasas de supervivencia y niveles séricos de TAOC, los niveles de TGF- ≥ 1 se redujeron, y el mecanismo de acción puede estar relacionado con una mayor capacidad antioxidante [72]. Luo et al. [73] investigaron el efecto de intervención de asiaticoside en ratas con un modelo de lesión de la médula espinal (SCI). Los resultados mostraron que los niveles de iNOS, TNF- -, IL-1 -, IL-6, y NF- - - B P65 en suero de rata se redujeron, y los niveles de MDA, SOD, glutatión reducido (GSH) y glutatión peroxid(GSH-Px) se increment. Otros estudios encontraron que el nivel de expresión de p38MAPK en el tejido de la médula espinal de la rata se redujo significativamente, lo que indica que asiaticoside puede mejorar la lesión de la médula espinal en ratas a través de antioxidante, anti-inflamatorio y la inhibición de la vía de señalización p38MAPK. Fan et al. [74] encontraron que el ascorbósido puede restaurar la función motora en ratas con SCI y mejorar el daño neurológico de la médula espinal. El mecanismo de acción está relacionado con la reducción de la expresión de TNF- - y c-ascorboside p-ascorboside E-3 proteína en el tejido de la médula espinal. Eka et al. [75] investigaron el efecto hipoglucémico del ascorboside en ratones diabéticos. Los resultados mostraron que después de la intervención con asicosido, los niveles de glucosa en sangre en ayunos y hemoglobina glicosilada de ratones modelo diabéticos se redujeron, y el nivel de insulina se incrementó, lo que sugiere que asiaticoside puede tener un buen efecto terapéutico sobre la diabetes.
10 conclusión
En los últimos años, con la profundización de la investigación en asiaticoside por los estudiosos en el país y en el extranjero, los principales efectos farmacológicos y mecanismos de asiaticoside se han aclarinicialmente: asiaticoside puede ejercer efectos antitumorales mediante la inhibide la proliferación de células tumorales e inducir apoptosis de células tumorales; Puede ejercer efectos anti-fibrosis mediante la regulación hacia abajo de los niveles de TGF- − 1, CTGF, ALT, T asiaticoside, y los niveles de Hyp, que ejerce un efecto anti-fibrosis; Ejerce un efecto antiinflamatorio al regular la expresión de IL-6, IL-1 -, y TNF- - en la vía de señalización NF- - B e inhibidel estrés oxidativo; Ejerce un efecto anti-da al inhibir la apoptosis de las células endotelivasculares, la actividad de la vía de señalización TLR4/NF-κB y la expresión de los factores inflamatorios IL-1, IL-6 y TNF- -; Ejerce un efecto anti-AD mediante la inhibición de la expresión de los tipos I y III de colágeno y la expresión de TNF- -, IL-6, IL-1 - y la actividad de la vía de señal Wnt/ - - catenina, upregulato TGF- - -1, VEGF, iNOS, la expresión de MCP-1, y desempeñar un papel en la inhibide la hiperplasia cicatriy la reparación del daño de la piel; Al mediar la vía de la señal MAPK/NF-κB, inhila la MDA, iNOS, TNF- -, la expresión de IL-6 y mejora la capacidad antioxidante, ejerciendo un papel en la mejora del daño hepático, renal y pulmonar.
En la actualidad, la mayor parte de la investigación sobre asiaticoside's los efectos antitumorales se centran en los mecanismos moleculares de las células in vitro, mientras que faltan estudios farmacológicos basados en experimentos in vivo. Por lo tanto, la investigación antitumoral posterior puede centrarse en modelos animales. Además, la investigación sobre asiaticoside's anti-inflammatory and anti-fibrosis effects most of the research focuses on the expression of related proteins, lacking research on the mechanism of action of specific signal pathways. Therefore, subsequent research can be conducted on the pharmacological effects and mechanisms of Centella asiatica extract from the perspective of signal pathways.
referencias
[1] National Pharmacopoeia Commission (en inglés). Pharmacopoeia of the People& (en inglés)#39;s República de China: parte I [s]. Edición 2020. Beijing: China Medical Science and Technology Press, 2020: 296.
[2] Weng Xiaoxiang, Huang Wenwu, Kong Deyun. Avances en la investigación sobre los componentes triterpenoides y las actividades farmacológicas de Centella asiatica [J]. Chinese Journal of Pharmaceutical Industry, 2011, 42 (9): 709-716.
[3] Li Yanan, Li Zhihui, Huo Lini, et al. Investigación sobre la composición química de Centella asiatica[J]. Guangxi Traditional Chinese Medicine, 2015, 38(2): 78-80.
[4] DING Y, ZHANG Z, WANG S. Research progress of asiaticoside[J]. Medicina nacional de Shizhen, 2016, 27(3): 697-699.
[5] ZHOU X, KE C L, LV Y, et al. Asiaticoside suprime la proliferación celular al inhibir la vía de señalización NF-κB en el cáncer colorrectal [J]. Int J Mol Med, 2020, 46(4):
1525-1537.
[6] HE Y G, PENG X H, ZHENG L, et al. Asiaticoside inhila la transición epitelimesenquimal y las propiedades similares a las células madre de las células de cáncer de páncreas PANC-1 al bloquear la activación de P65 y p38MAPK[J]. J Gastrointest Oncol, 2021, 12(1): 196-206.
[7] Zeng Manhong, Chen Lingfeng. Estudio sobre el efecto de asiaticoside en la línea celular de cáncer gástrico humano SGC-7901 [J]. Journal of Jiangxi College of Traditional Chinese Medicine, 2011, 23(6): 57-59.
[8] Liu Chenxu, Qin Sida, Xu Tao, et al. Efectos de asiaticoside sobre la apoptosis y los niveles de expresión proteica de VEGF y bFGF en células de cáncer de mama MCF-7 [J]. Avances en biomedicina moderna, 2018, 18(7): 1314-1317.
[9] Wu Qian, Jiang Bo. The effect of asiaticoside on apoptosis of Human osteosarcoma Saos-2 cells [J]. Modern Medicine and Clinical, 2019, 34(8): 2262-2267.
[10] MA Y, WEN J, WANG J, et al. Los asiáticos antagonila proliferación y resistencia a fármacos quimioterapéuticos en células de carcinoma hepatocelular (CHC) [J]. Med Sci Monitor, 2020, 26: e924435.
[11] Yang Lianjun. Bcl-2, Bax y apoptosis de células tumorales [J]. Chinese Journal of Cancer Biotherapy, 2003, 3 (3): 232-234.
[12] Pan Jinli. Estudio sobre el mecanismo del asiaticoside que induce la apoptosis de células humanas de cáncer de ovaria2780 [J]. Journal of Traditional Chinese Medicine, 2018, 33(4): 521-524.
[13] AL-SAEEDI F J. estudio de la citotoxicidad de los asiaticosidos en ratas y células tumorales [J]. BMC Cancer, 2014, 14(1): 220.
[14] AL-SAEEDI F J, BITAR M, PARIYANI S. efecto de asiaticoside en la absorción de 99mtc-tetrofosmina y 99mTc- sestamibi en MCF- 7 células [J]. J Nucl Med Technol, 2011, 39 (4): 279-283.
[15] Li Y C, WANG H H, ZHANG R, et al. La actividad antitumoral de los asicosidos contra las células cancerosas resistentes a los medicamentos del mieloma múltiple está mediada por la inducde autofagia, la activación de las caspasas efectoras y la inhibición de la migración celular, la invasión y la vía de señalización de stat3 [J]. Med Sci Monit, 2019, 25: 1355-1361.
[16] Qi Luyu. Efectos de asiaticoside y madecassoside en fibroblaembrionhumanos in vitro [D]. Taiyuan: universidad médica de Shanxi, 2012.
[17] Qian Xingjia. Estudio Experimental sobre el efecto de la intervención de matrina y asiaticoside en fibroblade pulmón humano [D]. Nanjing: universidad de Nanjing de medicina tradicional China, 2012.
[18] Ye Wenjing, Zhu Xiaochun, Wang Xiaobing, et al. Asiaticoside atenúa la fibrosis mesenquimal pulmonar indupor la inhibide la inflamación y la fibrosis[J]. Chinese Journal of Pharmacology and Toxicology, 2016, 30 (1): 29-37.
[19] Zhu Dewei, Shen Yunhui. Efecto protector de asiaticoside sobre la fibrosis pulmonar inducida por micofenolato mofetien en ratones [J]. Journal of Shanghai University of Traditional Chinese Medicine, 2020, 34 (6): 41-46.
[20] Wang Ce. Estudio sobre el efecto de asiaticoside en la fibrosis renal en ratas con obstrucción ureteral unilateral [J]. Chinese Medicine Clinical Research, 2017, 9(20): 1-4.
[21] Wang Ce. Estudio Experimental sobre el efecto de asiaticoside en la fibrosis miocárdica en ratas con infarto de miocardio [J]. Chinese Journal of biomedical Drugs, 2014, 34(8): 19-22.
[22] Zhao Sixia, Zhang Ruzong, Yang Subei. Estudio sobre el efecto de los asiaticosidos en la fibrosis hepática inmune en ratas [J]. Chinese Journal of Modern Applied Pharmacy, 2017, 34(5): 666-670.
[23] Ji Qijian, Xu Tie. Efecto protector de los asiaticosidos sobre la fibrosis pulmonar inducida por bleomicina en ratas [J]. Modern Medicine, 2014, 42 (11): 1304-1309.
[24] LUO J, ZHANG T, ZHU C W, et al. Los asiaticosipodrían atenuar la fibrosis pulmonar inducida por bleomicina activando cAMP y la vía de señalización RAP1 asistida por A2AR [J]. J Cell Mol Med, 2020, 24(14): 8248-8261.
[25] ZHANG T, DAI J Y, YE W J, et al. Asiaticoside atenúa la fibrosis pulmonar inducida por bleomicina en ratones A2AR-/- mediante la promoción de la vía de señalización BMP7/Smad1/5 [J]. Biochem Biophys Res Commun, 2020, 527(3): 662-667.
[26] Guo Limin, Lv Jieli, Zhang Laibin. Progreso de la investigación sobre el mecanismo antiinflamatorio de sesquiterpenoids naturales [J]. Chinese Journal of Traditional Chinese Medicine, 2018, 43(20): 3989-3999.
[27] Linghu Lang, Jia Youjing, Chen Jing, et al. El efecto de asiaticoside en el daño inflamindupor lipopolisacáridos en astrocitos [J]. Journal of Zunyi Medical College, 2018, 41(2): 160-164.
[28] Jiang Chengcheng, Zhao Hengguang, Wu Yamei. Efectos de asiaticoside en la activación indupor lipopolisacáridos del factor de transcripción nuclear κB y la respuesta inflamen células RAW264.7 [J]. Chinese Journal of Respiratory and Critical Care Medicine, 2010, 9 (4): 422-425.
[29] WAN J Y, GONG X, JIANG R, et al. Efectos antipiréticos y antiinflamatorios de Asiaticoside en ratas tratadas con lipopolisacáridos a través de la regulación de la heme oxigenas-1 [J]. Phytother Res, 2013, 27(8): 1136-1142.
[30] Zhang T, Cai HJ, Yang L, et al. La Asperulosid reduce la hipertensión pulmonar hipóxica en ratones al inhibir la vía NF- − B/ P38. Chinese Journal of pathophysiology, 2019, 35(9): 1600-1607.
[31] MAI L J, FU X X, HE G, et al. Efecto de asiaticoside en la displasia broncopulmonar inducida por hiperoxien ratas neony mecanismo relacionado [J]. Zhongguo Dang Dai Er Ke Za Zhi, 2020, 22(1): 71-76.
[32] ZHANG Z, CHEN L J, SUN Y H, et al. Efectos de asiaticoside en la expresión de factores inflamatorios en células endoteliindupor A − 1-42 [J]. Chinese Journal of biomedical Drugs, 2015, 35(1): 46-48.
[33] JIANG J Z, YE J, JIN G Y, et al. Asiaticoside mitiga la inflamación alérgica mediante la derogación de la degranulación de los mastocitos [J]. J Agr Food Chem, 2017, 65(37): 8128 — 8135.
[34] WU K Y, YAO G H, SHI X L, et al. Asiaticoside mejora la necrosis de células acinares en la pancreatitis aguda a través de la vía del receptor de tipo toll 4 [J]. Mol Immunol, 2020, 130: 122-132.
[35] Liu Chang, Meng Xianyong, Dong Xiaohua. The Genesis of Alzheimer& (en inglés)#39;s enfermedad y avances en la investigación de fármacos terapéuticos [J]. Journal of Neuropharmacology, 2020, 10(4): 36-40.
[36] Mo Jucai, Ying Na, Xu Changliang, et al. Efectos de asiaticoside en la liberación de mediadores inflamde astrocitos indupor Aβ [J]. Zhejiang Traditional Chinese Medicine Journal, 2012, 47(11): 835-837.
[37] CAI P. efectos y mecanismo de asiaticoside en un daño de células endoteliindupor ≥ 1-42 [D]. Luzhou: Luzhou Medical College, 2014.
[38] SONG D, JIANG X, LIU Y, et al. Asiaticoside atenatenla la inhibición del crecimiento celular y la apoptosis indupor A − 1- 42 vía inhibide la vía de señalización TLR4/NF- − B en las células endoteliasasasdel microv del cerebro humano [J]. Front Pharmacol, 2018, 9: 28.
[39] HOSSAIN S, HASHIMOTO M, KATAKURA M, et al. Medicinal value of asiaticoside for Alzheimer& (en inglés)#Enfermedad 39;s evaluada mediante espectroscopia de correlación de fluorescde detección de una sola molécula, microscopía de escaneo por láser, microscopía electrónica de transmisión y acoplamiento in silico [J]. BMC complemento Altern Med, 2015, 15(1): 118.
[40] ZHANG Z, CAI P, ZHOU J, et al. Efectos de los asiaticosidos sobre la apoptosis de las células endotelide la vena umbilical humana inducida por A ≥ 1-42 [J]. Int J Clin Exp Med, 2015, 8(9): 15828-15833.
[41] XU C L, WANG Q Z, SUN LM, et al. Asiaticosido: atenude la neurotoxicidad indupor MPTP en un modelo de rata de parkinsonismo a través de mantener el equilibrio redox y la regulación de la relación de Bcl-2/Bax [J]. Pharmacol Biochem Behav, 2012, 100(3): 413-418.
[42] HANAPI NA, MOHAMAD A S, ABDULLAH J M, et al. Permede barrera hematoencefáde Asiaticoside, madecassoside y ácido asiático en el modelo de células endotelidel cerebro porcino [J]. J Pharm Sci, 2020, 110(2): 698-706.
[43] Ying N, Yin ZJ, Yu H, et al. Efecto de la intervención de asiaticoside en la función cognitiva en ratones con diabetes modelo [J]. Zhejiang Journal of Integrated Traditional and Western Medicine, 2014, 24(3): 203-206, 184.
[44] Wang Xiaojing, Wang Dongxing, Xu Chunjing, et al. Efecto terapéutico del asiaticoside sobre el Alzheimer#39;s enfermedad [J]. Chinese Journal of Pharmaceutical Sciences, 2016, 6(13): 37-39, 92.
[45] HUANG Y L. correlación entre PPARγ Y expresión de factores inflamatorios después de inyección intraperitoneal de A ≥ 1-42 en ratas Y estudio de intervención de asiaticoside [D]. Luzhou: Southwest Medical University, 2017.
[46] YIN Z J, YU H Y, CHEN S, et al. Asiaticoside atenúa los déficits cognitivos indupor la diabetes mediante la regulación de la vía PI3K/Akt/NF-κB [J]. Behav Brain Res, 2015, 292: 288-299.
[47] WANG L Q, GUO T, GUO Y F, et al. Asiaticoside produce un efecto similar al de los antidepresien un modelo crónico de estrés leve impredecible de la depresión en ratones, que implica la reversión de la inflamación y la vía de señalización PKA/pCREB/BDNF [J]. Mol Med Rep, 2020, 22(3): 2364-2372.
[48] LUO L, LIU X L, MU R H, et al. BDNF hipocampal señalización restaurada con el tratamiento crónico Asiaticoside en ratones similares a la depresión [J]. Brain Res Bull, 2015, 114: 62-69.
[49] HOU T H, LI X B, PENG C S. Borneol mejora los efectos antidepreside Asiaticoside mediante la promoción de su distribución en el cerebro [J]. Neurosci Lett, 2017, 646: 56-61.
[50] WARINTORN R, CHIRANAN K, et al. Extracción de centella asiatica despigmentada por tratamiento previo con dióxido de carbono supercrítico líquido para la aplicación de cicatride heridas [J]. Processes, 2020, 8(3): 277.
[51] LEE J H, KIM H L, LEE M H, et al. Asiaticoside mejora la migración normal de las células de la piel humana, la adhesión y el crecimiento in vitro modelo de curación de heridas [J]. Phytomedicine, 2012, 19(13): 1223-1227.
[52] Ouyang Danwei, Shao Yan, Kong Deyun, et al. Efecto inhibidor de asiaticoside y sus constituyentes químicos sobre la proliferación de fibroblade la cicatriz [J]. World Clinical Drugs, 2014, 35(4): 215-220.
[53] Dai Libing, Pan Shu, Shen Yan, et al. Efectos de asiaticoside sobre el factor de crecimiento del tejido conectivo y las señales reguladoras RhoA/ROCK-I en fibroblade la cicatriz proliferativa [J]. Chinese Journal of Pharmacy, 2010, 45 (14): 1067-1072.
[54] Li Shanshan. Efectos de asiaticoside sobre la proliferación de fibroblade la cicatriz y la expresión de colágeno y TGF- ≥ 1 mRNA [D]. Wuhan: universidad de Hubei de medicina tradicional China, 2011.
[55] Zhou Z, Xiong W, Huang X, et al. Efectos de asiaticoside sobre las fibras de colágeno y la expresión de TGF- − 1 en tejido cicatriproliferativo de orejas de conejo [J]. Chinese Journal of Aesthetic Medicine, 2015, 24(21): 32-37.
[56] HUANG J, ZHOU X B, XIA L L, et al. Inhibide la formación de cicatriz hipertrófica con tratamiento oral Asiaticoside en un modelo de cicatriz de oreja de conejo [J]. Int Wound J, 2021 [2021-06-12].
[57] HU R, JIANG R. efectos de asiaticoside en la cicatride heridas y la expresión de la proteína de choque térmico 47 en la formación de cicatrices en ratas con quem[J]. Zhejiang Medical Journal, 2020, 42(1): 36-38, 101.
[58] WU Y. Research on the mechanism of asiaticoside in the treatment of burn wounds [D]. Nanjing: universidad de Nanjing de medicina tradicional China, 2019.
[59] ZHU L F, LIU X Y, DU L, et al. Preparación de nanofibras Asiaticosi- descargadas coaxialmente electrohily su efecto en la herida profunda de quemde espesor parcial [J]. Biomed Pharmacother, 2016, 83: 33-40.
[60] Chen L, Wang T, Liu M, et al. Efectos de asiaticoside sobre la intervención en diferentes etapas de reparación de heridas y expresión inmunohistoquímica del factor de crecimiento transformador ≥ 1 y Smad3 en heridas de oreja de conejo [J]. Hebei Traditional Chinese Medicine, 2019, 41(10): 1532-1535, 1539.
[61] HOU Q, LI M, LU Y H, et al. Propiedades curativas de heridas por quemde Asiaticoside y madec Assoside [J]. Exp Ther Med, 2016, 12(3): 1269-1274.
[62] NIE X U, ZHANG H, SHI X J, et al. El gel de óxido nítrico Centella asiatica iaticoside acelera la cicatride úlceras cutáneas diabéticas al activar la vía de señalización Wnt/ − -catenina [J]. Int Immunopharmacol, 2020, 79: 106109.
[63] CHENG X F, WANG Z Y. aplicación de colgajos cutáneos locales en la reparación de defectos cutáneos faci[J]. World Latest Medical Information Digest, 2017, 17(11): 53.
[64] FENG X G, HUANG D, LIN D S, et al. Efectos del tratamiento asiatico-coside sobre la supervivencia de colgajos cutáneos aleatorios en ratas [J]. J Invest Surg, 2021, 34(1): 107-117.
[65] Guo Jiaqi, Guo Minhui, Kong Songzhi, et al. Preparación del parche de reparación de glucosilídico alginato de Centella asiática y su efecto de reparación de heridas [J]. Chinese Herbal Medicine, 2020, 51(19): 4934-4942.
[66] PENG Q, LI J Y, LI H M, et al. Preparación y evaluación de calidad de nanoleches asiaticosidas [J]. Chinese Journal of New Drugs, 2019, 28(10): 1276-1280.
[67] ZHANG LN, ZHENG JJ, ZHANG L, et al. Efectos protectores de Asiaticoside sobre la lesión pulmonar séptica en ratones [J]. Exp Toxicol Pathol, 2011, 63(6): 519-525.
[68] ZHENG J J, ZHANG L N, WU M J, et al. Efectos protectores de los asiaticosidos en la lesión renal aguda inducida por la sepsis en ratones [J]. Zhongguo Zhong Yao Za Zhi, 2010, 35(11): 1482-1485.
[69] ZHANG L, LI H Z, GONG X, et al. Efectos protectores de los asiaticosidos sobre la lesión hepática aguda inducida por lipopolysac- charide/ d-galactosamina en ratones [J]. Phytomedicine, 2010, 17(10): 811-819.
[70] WANG Z, LIU J T, SUN W S. efectos de Asiaticoside sobre los niveles de proteínas citoesqueléde podocito y proteínas del diafragma de slit renal en la nefropatía de rata indupor adriamicina [J]. Life Sci, 2013, 93(8): 352-358.
[71] DANG J W, LEI X P, LI Q P, et al. Asiaticoside atenúa la lesión pulmonar inducida por hiperoxiin vitro e in vivo [J]. Iran J Basic Med Sci, 2019, 22(7): 797-805.
[72] SHEN H Y, ZHU F, LI J S, et al. Efecto protector de los asiaticosidos en la inhibición de la proliferación inducida por radiación y daño al ADN de fibroblay muerte de ratones [J]. Open Life Sci, 2020, 15(1): 145-151.
[73] LUO Y, FU C F, WANG Z Y, et al. Asiaticoside atenúa los efectos de la lesión de la médula espinal a través de los efectos antioxidantes y antiinflamatorios, y la inhibición del mecanismo p38-MAPK [J]. Mol Med Rep, 2015, 12(6): 8294-8300.
[74] FAN L, LI X B, LIU T. Asiaticoside inhila la apoptosis neuronal y promueve la recuperación funcional después de una lesión de la médula espinal en ratas [J]. J Mol Neurosci, 2020, 70(12): 1988-1996.
[75] EKA F, ELIN Y S, ELFAHMI E, et al. Actividad antidiabética del extracto de fracciones, y compuesto asaticosido aislado de Centella Asiatica Linn. Hojas en ratones diabéticos inducidos por aloxano [J]. Asia J Pharm Sci, 2017, 10(10): 268-272.
-
anterior
¿Cuáles son los beneficios de Centella Asiatica extracto Asiaticoside?
-
siguiente
Estudio sobre el extracto asiático de Gotu Kola para la curación de heridas


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




