Estudio sobre el extracto asiático de Gotu Kola para la curación de heridas
Centellaasiatica L, Urban is the dried whole grass of Centella asiatica of the genus Centella of the family Umbelliferae, which was first published in the Divine Husbandman's clásico de la Materia médica, clasificado como un grado medio, también conocido como Lok Dak Ta, Bun Da Bowls, hierba de herradura, hierba de dinero de hoja grande y así sucesivamente, es una hierba perenne rastrera con dulzura, pungencia y frescura, y tiene la eficacia de eliminar el calor, inducir humedad, eliminar toxinas, eliminar inflamaciones, activar la circulación sanguínea, y detener la hemorragia [1].
Gotu Kola has a wide distribution range, mainly concentrated in the northern and southern hemispheres and subtropical regions, mainly produced in South Africa, India, Malaysia, Australia, China and other regions. It is mainly found in South Africa, India, Malaysia, Australia, China and other regions. It is mainly distributed in South China, East China, Central and Southwest China. Asiaticoside (structural formula see Figure 1) is one of the main components of triterpenoid saponins in Centella asiatica extract, and modern pharmacological studies have confirmed that asiaticoside has the function of inhibiting scar formation, promoting trauma healing, anti-tumor, neuroprotection, anti-anxiety, immunomodulation, etc. Now, we present the results of the study of Centella asiatica extract. Now, the extraction process, pharmacological activity, content determination and pharmacological effects of centella asiatica glucoside are summarized.
1 proceso de extracción y determinación del contenido de centella asiatica glucoside
Con la aplicación continua de nuevas tecnologías y métodos, decocción, método de reflujo, método ultrasónico, método enzim, etc apareció en la extracción de glucósidos Centella asiatica, Han Wei et al. [2] utilizaron la extracción enzimde glucósidos Centella asiatica, enzima celulasa y el sustrde Centella asiatica relación de masa de m(E) → m(S) = 1 − 50, la relación de masa material-líquido de (Centella asiatica y el solvente del agua) 1 − 25, pH 6.0, la temperatura de la enzima se estableció en 40 ∶, El tiempo de la enzima era de 1 hora, y la temperatura de la enzima era de 40 ℃, y el tiempo de la enzima era de 1.0 ℃, y la temperatura de la enzima era de 40 ℃. La temperatura de digestión de la enzima se estableció en 40 ℃ y el tiempo de digestión de la enzima fue de 1.5 h. Se obtuvo la mayor cantidad de asiaticosido, es decir, 29.6%.
The separation and purification methods of Asiaticoside include chromatography, solvent extraction, high performance liquid chromatography (HPLC) and high speed countercurrent chromatography (HSCCC). Preparative high performance liquid chromatography (HPLC) is a preparative liquid chromatography method that uses a high pressure, high flow rate liquid delivery system to separate samples with high purity on a high resolution, large internal diameter, high capacity separation column. The purity, recovery and separation efficiency of the product separated by this method are much better than that of the traditional preparative method. Gao Mingzhe et al. [3] used preparative HPLC to complete the separation within 20 min separation time, and prepared two fractions of centella asiatica glucoside and hydroxycentella asiatica glucoside, and the purity of the product reached more than 98% through the test.
Actualmente, para la determinación del contenido del fármaco de centella asiatica glucósido, se dispone de cromatolíquida de alta eficacia, análisis titrimétrico, método de escaneo de capa fina y método espectrofotométrico, entre los cuales la cromatolíquida de alta eficacia es más adecuada para el control de calidad de las hierbas. Los informes de la literatura muestran que la separación de cumquat glucoside es mejor cuando se utiliza la eludel gradiente acetonitri- agua y ajustar la relación de acetonitrilo al agua a 29:7l [4].
Liang Liguang et al. [5] used HPLC to determine the asiaticosides in Centella asiatica of different origins and different times, and concluded that the content of asiaticosides in Centella asiatica harvested from June to October in Nanning, Guangxi was higher. It was concluded that the content of asiaticoside in Centella asiatica was mainly enriched in the leaves, and the content of total asiaticoside was as high as 6.12%, while that in the stems was 2.43%, and the content in the roots was lower, containing only 1.11%.
2 efectos farmacológicos
2.1 promover la curación de heridas
Estudios han confirmado que asiaticoside puede promover la proliferación de fibroblay la síntesis de matriz extracelular en el proceso de cicatride heridas. Jeong-Hyun Lee et al. [6] encontraron que al interferir con fibroblahumanos con centella asiatica glucoside, centella asiatica glucoside fue capaz de aumentar la adhesión y la migración de las células humanas, y promover la proliferación de fibroblahumanos, que podría aplicarse a la curación de heridas de la piel. LU L et al. [7] usaron la tecnología de micromatrices de cDNA para examinar los perfiles de expresión génica de fibroblade la piel humana tratados in vitro con asiaticosido (30 mg/ml) y encontraron que los genes responsables de la proliferación celular y la síntesis de la matriz extracelular estaban regulados en diferentes momentos. Además, el ARNm y los niveles de proteínas de colágeno tipos I y III también se incrementsignificativamente bajo el efecto de asiaticoside.
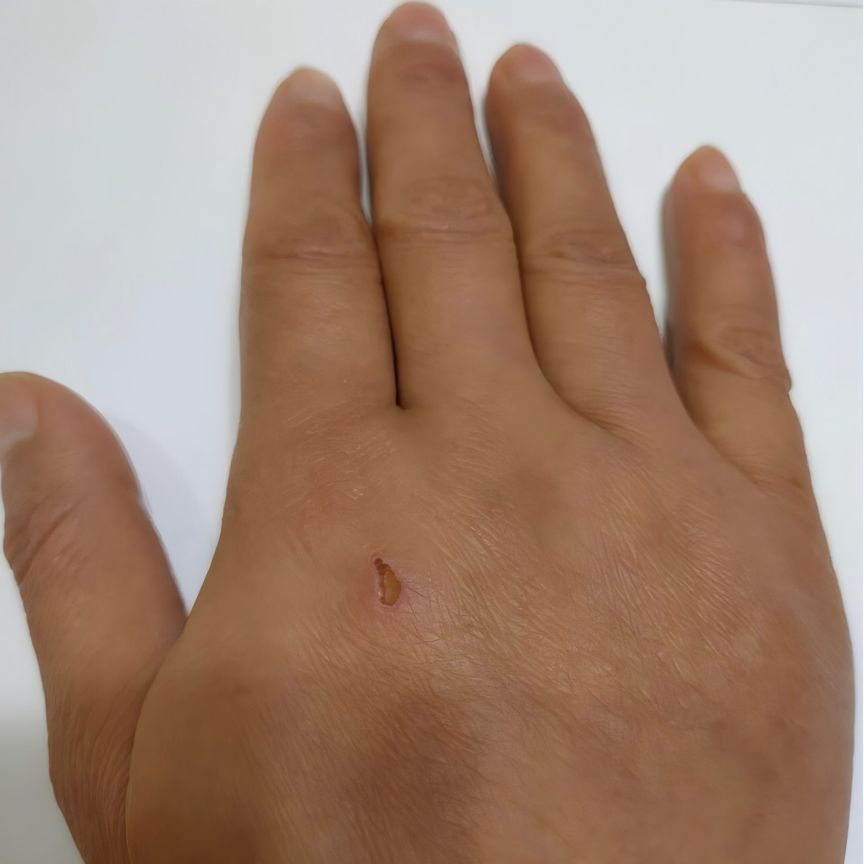
2.2 inhibide la formación de cicatriz cutánea
Al estudiar la morfoy proliferación de fibroblacultivados in vitro, se encontró que el asiaticosido podría inhibir la proliferación de fibroblacicatri, y la proliferación de fibroblase inhisignificativamente cuando la concentración de asiaticoside varió de 0.1 mg/ml a 1.0 mg/ml. Esto sugiere que el asiaticosido reduce la síntesis de matrices extracelulares, como los tejidos de granulación y el colágeno, y por lo tanto reduce la formación de cicatrices al inhibir el crecimiento de fibrobla. Mientras tanto, a 1,0 mg/ml, asiaticosido podría inhibir la expresión de ARNm de colágeno tipo I y III en fibroblade la cicatriz, lo que sugiere que asiaticoside reduce la síntesis de la matriz extracelular y la formación de la cicatriz al disminuir la producción de colágeno. Este experimento confirma que el cumquat glucoside inhila la producción de colágeno y la formación de cicatrices al suprimir la secreción de colágeno de fibroblahiperactivos [8].
Pan Shu et al. [9] used flow cytometry analysis, RT-PCR and protein technology to study the effects of centella asiatica glycoside on the proliferation of scar fibroblasts and Smad pathway, and found that centella asiatica glycoside could inhibit scar proliferation, and its mechanism mainly increased the expression of Smad 7, an I-Smad transduction signal, and inhibited the pathological effects of TGF-β1, which caused fibroblasts to proliferate, and then inhibited the collagen secretion. Its mechanism mainly works by increasing the expression of I-Smad transduction signal Smad 7, inhibiting the pathological effect of TGF-β1 and blocking the proliferation of fibroblasts.
Lee et al. [10] encontraron que centella asiatica glucoside podría inducir fosforilación de Smad2 y Smad3. Al mismo tiempo, también encontraron que el clorde cumquat induce la Unión de Smad3 y Smad4, y al mismo tiempo induce la translocación nuclear del complejo, lo que sugiere que la acción del clorde cumquat está relacionada con la vía de señalización Smad. Sin embargo, SB431542, un inhibidor de la quinasa TGF-β receptor I, no pudo inhibir la fosforilación de Smad2 yla síntesis de colagenasa tipo I inducida por clorde cumquat. Basado en esto, Lee concluyó que la síntesis de colagenasa tipo I inducida por clorde cumquat se logró a través de la vía Smad independiente de TGF- − cinasa.
Tang B et al [11] también confirmó que en el tejido cicatricial, centella asiatica glucoside fue capaz de inhibir la expresión de TGF - − 1 proteínas del receptor y ARNm y aumentar la expresión de las proteínas Smad7 y ARNm, mientras que no tuvo efecto sobre los complejos fosforilsmad2 y Smad3, Smad2, Smad3, y Smad4. Basado en esto, creía que el mecanismo de la inhibición de la proliferación de colágeno por cumquat glucoside es principalmente a través de aumentar la expresión de Smad7, que a su vez inhiel efecto patológico de TGF- − 1 y bloquea la proliferación de fibrobla. Bylka et al. [12] creyeron que el glucósido cumquat tiene el doble efecto de promover la cicatride heridas e inhibide la formación de cicatrices.
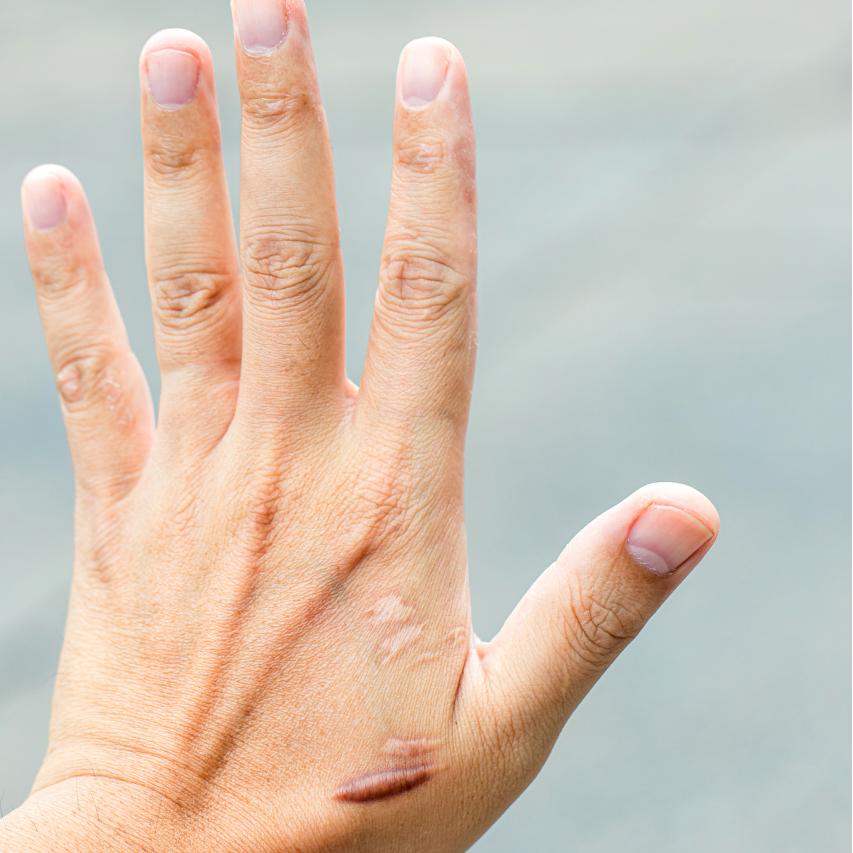
2.3 efectos antitumorales
Estudios farmacológicos modernos han confirmado el efecto antitumoral de centella asiatica glucoside. Su mecanismo consiste principalmente en inducir la apoptosis de las células tumorales, bloquear la síntesis de ADN de las células tumorales e inhibide la proliferación de células tumorales. En el estudio antitumoral del glucósido de cumquat, se encontró que el glucósido de cumquat podía inducir apoptosis de células del carcinoma epidermoide oral y tenía un efecto sinérgico con la vincristina. El mecanismo sinérgico fue aumentar la concentración de Ca+ intracy reducir el potencial de membrana de las células, aumentando así la sensibilidad de las células a los fármacos antitumorales, y al mismo tiempo, el cumquat glucoside podría aumentar el bloqueo de fase G2/ m inducido por vincristina. La citometría de flujo, la natación en gel de agarosa y las pruebas de morfopueden confirmar esto [13], y Fatma J Al-Saeedi [14] también confirmó que el glucósido de centella asiatica puede promover la apoptosis de las células de cáncer de mama humano y mejorar la actividad antitumoral. Sun Shengmei et al [15] encontraron que Centella asiatica tenía un efecto inhibitsignificativo sobre las células Hela del cáncer de cuello uterino con concentración y dependencia del tiempo cuando investigaron los efectos de los glucósidos de Centella asiatica sobre las células Hela del cáncer de cuello uterino. El mecanismo se analizó como el aumento de la expresión de Spase-3 y la disminución de la proteína de la supervivencia inducida por Asiaticoside, que es un miembro de la familia de inhibide la apoptosis y puede inhibir la expresión de Spase-3, bloqueando así el proceso de apoptosis Bunpo et al [16] encontraron que Centella asiatica glucoside inhila la síntesis de ADN en las células tumorales, y luego inhila la variante de focos quísticos indupor óxido de metileno, lo que retrasla la proliferación de las células tumorales e inhila la carcinogénesis.
Ku Jung Kwon et al. [17] encontraron que Gotu Kola Fue capaz de reducir la melanogénesis en los melanocitos, y estudios posteriores confirmaron que los glicósidos de centella asiatica fueron capaces de inhibila melanogémediante la reducción de la expresión de ARNm tirosinasa a través del factor de transcripción asociado al ojo.
2.4 efectos antifibróticos
Asiaticoside tiene un efecto antifibrótico. Wang Ce [18] utilizó centella asiatica glucoside para intervenir en el modelo post-infarto de ratas, y encontró que centella asiatica glucoside podría mejorar la expresión de colágeno en el área no infartada de los tejidos del miocardio de ratas infartadas, y aliviar la acumulación de matriz extracelular, ejerciendo así un efecto antifibrótico sobre la fibrosis intersticial del miocardio. El mecanismo se realiza principalmente mediante la regulación de la expresión del factor de crecimiento de transformación de la matriz extracelular TGF- − 1. Asiaticoside también puede aumentar la expresión de genes de sinaptopodina, nefrina y podocina y disminuir la expresión del gen de desmina en nefroesclerosis indupor adriamicina en ratas, reduciendo así la expresión de colágeno intersticial renal y retarel desarrollo de fibrosis intersticial renal [19].
Yang Guang et al. [20] encontraron que el clorde cumquat fue capaz de reducir la fibrosis hepática en el estudio de la fibrosis hepática inducida por tetraclorde de carbono, pero el mecanismo del estudio no estuvo involucrado.
HOU Shiqiang et al [21] estudió el mecanismo de la intervención de la reestenosis del stent con clorde cumquat de in vitro ein vivo diseño experimental, y encontró que el clorde cumquat puede reducir significativamente la síntesis y secreción de la matriz extracelular por la regulación de la expresión de la proteína Smad7 y la supresión de la expresión de TGF- − 1, inhibir la proliferación de endomembrano después de la colocación de un stent, y aliviar el daño de las células endoteli, Y es un regulador bioquímico eficaz de la rapamicina. Es un regulador bioquímico eficaz de la rapamicina, que también demuestra que Asiaticoside tiene un efecto muy bueno en la inhibide la fibrosis.
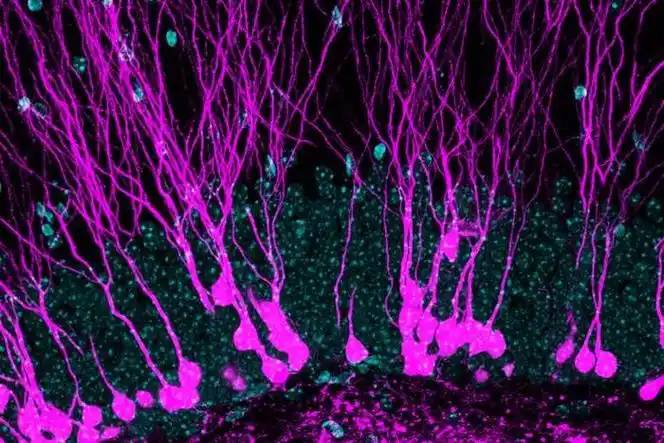
2.5 efectos sobre el sistema nervioso
2.5.1 efecto neuroprotector
Jin Yan et al [22] usaron estreptozotocina para crear un modelo de neuralgia periférica diabética y administraron dosis altas y bajas de asiaticosido después de un modelo exitoso. Los resultados mostraron que asiaticoside podría inhibisignificativamente la activación de la microglia en el cuerno dorsal de la médula espinal, y down-regular la liberación de la médula espinal IL - − 1 y TNF - -, que podría inhibieficazmente la hipersensibilidad nociceptérmica y la hiperalgeevoctácindupor la lesión diabética del nervio periférico.
Qi Fengyan et al. [23] usaron un modelo de cultivo primario de la lesión de n-metil-d-asparato en las neuronde la corteza cerebral y encontraron que el glucoside cumquat tenía un efecto protector significativo en la lesión neuronal indupor el n-metil-d-asparato de una manera dependiente de la concentración. Se encontró que Centella asiatica tenía un efecto protector significativo en el daño neuronal inducido por n-metil-d-asparde una manera dependiente de la concentración. El mecanismo es que asiaticoside puede down-regular la expresión del receptor de glutamato N2B, y luego inhibir o inhibiparcialmente el glutamato N2B mediada por el receptor intracde sobrecarga de calcio, y reducir la expresión de la apoptosis asociada a la proteína Bcl-2, con el fin de proteger a las neuroncorticde la excitotóxico daño inducido por el ácido n-metil-d-aspártico. D-aspartato, proteasí las neuroncorticde la excitotoxicidad indupor n-metil-d-aspar.
Ma Shiping [24] usó 1-metil-4-fenil-1,2,3,6-tetrahidropiridina (MPTP) en un modelo de rata de Parkinson's y encontró que podría antagonila neurotoxicidad inducida por MPTP. El tratamiento con centella asiatica glucoside puede antagonineurotoxicidad indupor MPTP, proteger las neurondopaminérgicas, y mejorar la disfunción motora. Otro estudio demostró que centella asiatica tenía un efecto protector sobre la disfunción cognitiva inducida por colchicina y el daño oxidativo relacionado [25].
2.5.2 efectos ansiolíticos y antidepresi.
La eficacia de los fármacos antidepresiutilizados actualmente en la práctica clínica no es satisfactoria, y hay muchas reacciones adversas. La patogénesis de la depresión no está clara, y los principales fármacos antidepresiutilizados en la práctica clínica se desarrollan dirigidos a receptores monoamincomo la norepinefr, la 5-hidroxitriptamina y la dopamina. Chen Yao et al. [26] encontraron que el clorde cumquat desempeña una función antidepresial aumentar el cuerpoy#39;s resistencia a diversos estímulos inespecíficos y evitar la disfunción de los ejes hipotalámico-hipopituit- adrenocortical e hipotalámico-pituit- tiroides causada por la sobreestimulación del cuerpo. El estudio de Liu et al [27] también confirmó que asiaticoside puede ser antidepresivo, y asiaticoside puede restaurar BDNF, PSD95, y sinapsina I en el hipocampo de ratas deprimial nivel de ratas normales, y el mecanismo es que asiaticoside puede jugar un efecto antidepresia través de la vía de señalización BDNF.
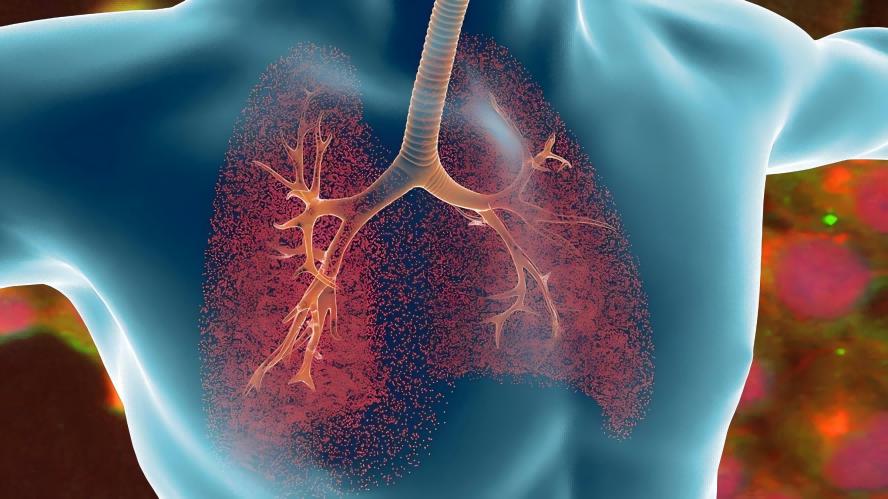
2.6 antiinflamatorio y protección pulmonar
Jing Yuan Wan et al. [28] injected lipopolysaccharide into rats to create a fever and inflammation model, and then administered centella asiatica glucoside, and found that centella asiatica glucoside had the effects of antipyretic and anti-infective, and its mechanism of action was to inhibit the expression of pre-inflammatory factors, including tumor necrosis factor-α, interleukin-6, cyclooxygenase-2 and prostaglandin E2, and the expression of cyclooxygenase-2 and prostaglandin E2. The mechanism of action is to inhibit the expression of pre-inflammatory factors, including tumor necrosis factor-α, interleukin-6, cyclooxygenase-2, and prostaglandin E2, by regulating heme oxygenase-1. In this paper, researchers used ZnPPIX, an inhibitor of heme oxygenase-1, to intervene, and found that this blocker could block the antipyretic effect of cumquat chloride, and partially change the effect of cumquat chloride in inhibiting the levels of tumor necrosis factor-α and interleukin-6.
Zhang Zhuo et al [29] also demonstrated that centella asiatica glucoside could inhibit the expression of the inflammatory factors Tumor Necrosis Factor-α and Interleukin-6, and increase the expression of Interleukin-10 in an experimental study, and concluded that centella asiatica glucoside could maintain the dynamic balance between inflammation and play a protective role in lipopolysaccharide-induced lung inflammation.
Sin embargo, Jiaming Qiu et al. [30] indicaron que el mecanismo de protección pulmonar por centella asiatica glucoside funciona a través de la vía de señalización NF-κB. En este estudio, se encontró que los asiaticosidos, dosis dependiente, redujeron la inflamación, la lesión pulmonar patológica, las citocinas y el edema pulmonar. Asiaticoside redujo significativamente la activación de NF- − Bp65 y la expresión de I - B -.
Además, los glucósidos de centella asiática tienen efectos hepatoprotectores [31], demencognitiva [32], antiulcer[33].
Bajo la guía de la farmacología moderna, Centella asiatica y sus componentes se aplican gradualmente a la clínica para servir a los pacientes. Con la amplia aplicación de las técnicas de biología celular y molecular en el estudio del mecanismo de los medicamentos, el mecanismo de acción de Centella asiatica y sus componentes sobre las enfermedades se hará más claro y más claro, lo que sin duda proporcionará amplias ideas para el desarrollo de la medicina China en China.
Referencias:
[1] Comisión nacional de farmacopea. Chinese Pharmacopoeia [M] (en inglés). Beijing: China Medical Science and Technology Press, 2010 :266.
[2] Han Wei, Chen Huidan, Fan Liang, et al. Extracción enzimde glucósidos de Centella asiática [J]. Journal of Nanjing University of Technology (Natural Science Edition), 2009, 31 (3) : 18.
[3] Gao Mingzhe, Yuan Xiaoyan, Xiao Hongbin. Cromatolíquida de alto rendimiento preparativa para la separación y purificación de asiaticoside e hidroxiasiaticoside a partir de extracto de Centella asiatica [J]. Cromato, 2008, 26 (3) : 362.
[4] LU Xingyi, FENG Lijuan. Determinación de hidroxicitrina y citrina en los glucósidos totales de Centella asiatica por HPLC[J]. Farmacéutico chino, 2008, 11 (1), 62.
[5] Liang Li-Guang, Ma W. determinación de cumquatosido e hidroxicumquatosido en Centella asiática de diferentes orígenes y diferente tiempo por HPLC[J]. West China Journal of Pharmacy, 2009, 24(2): 186.
[6] Lee JH, Kim HL, Lee MH, et al. Asiaticoside mejora la migración normal de las células de la piel humana, la adhesión y el crecimiento modelo de curación de heridas vitro vitro [J]. Asiaticoside mejora la migración normal de las células de la piel humana, la adhesión y el crecimiento modelo de curación de heridas vitro vitro [J].
[7] Lu L, Ying K, Wei S, et al. Inducción Asiaticoside para pro- gresión del ciclo celular, proliferación y síntesis de colágeno en fibro blastos dérmicos humanos [J]. Inducción Asiaticoside para pro- gresión del ciclo celular, proliferación y síntesis de colágeno en fibro blastos dérmicos humanos [J]. Int J Dermatol, 2004, 43 (11) : 801.
[8] Li Shanshan, Wang Weichen, Zeng Xianyu. Efectos de asiaticoside sobre la expresión de colágeno → y → y TGF- → 1mRNA en fibroblade tejido cicatri[J]. Chinese Journal of lepra and Skin Diseases, 2013, 29(5): 310.
[9] PAN Shu, LI Tianzeng, LI Yeyang, et al. Efectos de asiaticoside sobre la proliferación de fibroblade la cicatriz proliferativa y la vía de señalización Smad [J]. Chinese Journal of Repair and Reconstructive Surgery, 2004, 18 (4) : 291.
[10] Lee J, Jung E, Kim Y, et al. Asiaticoside induce la síntesis de colágeno humano I a través de TGFbeta receptor I quinasa (TbetaRI quinasa)-inde- pendent Smad señalización [J]. Asiaticoside induce la síntesis de colágeno humano I a través de TGFbeta receptor I quinasa (TbetaRI quinasa)-inde- pendent Smad señalización [J].
[11] Tang B, Zhu B, Liang Y, et al. Asiaticoside suprime la expresión de colágeno y la señalización TGF- - / Smad a través de la inducde Smad7 e inhibide TGF- - - RI y TGF- - - RII en los fibroblaqueloides [J]. Arch Dermatol Res, 2011, 303 (8) : 563.
[12] Bylka W, Znajdek -Awize → P, Studzi → ska -Sroka E, et al. Centella asiatica in Dermatology: an overview[J]. Phytother Res Phytother Res, 2014, 28 (8) :1117.
[13] Huang Yunhong, Zhang Shenghua, Zhen Ruixian, et al. Inducde apoptosis en células tumorales y aumento del efecto antitumoral de la vincristina por glucósidos de Centella asiática [J]. Cancer, 2004, 23 (12): 1599.
[14] Al-Saeedi FJ. Estudio de la citotoxicidad de los asiaticosidos en ratas y células tumorales [J]. BMC Cancer, 2014, 14 :220.
[15] Sun Shengmei, Li Peiling, Guan Yadong, et al. Apoptosis de células de cáncer cervical humano Hela inducido por asiaticoside y su mecanismo [J]. J]. Heilongjiang Medical Science, 2007, 30(2):42.
[16] Bunpo P, Kataoka K, Arimochi H, et al. Efectos de Centella asiatica sobre la formación de focos de cripta aberrindupor azoximetany carcinogénesis en el cérvix intestinal [J]. Carcinogénesis en los intestinos de las ratas F344 [J]. 2004, 42 (12) : 1987.
[17] Kwon KJ, Bae S, Kim K, et al. Asiaticoside, un componente de Centella asiatica, inhila la melanogénesis en el melanoma de ratón B16F10 [J]. Mol Med Rep. 2014. Mol Med Rep. 2014, 10(1) : 503.
[18] Wang C. estudio Experimental sobre el efecto de los glucósidos de centella asiática en la fibrosis miocárdica en ratas infartadas [J]. Chinese Journal of biomedical Drugs, 2014, 34(8): 19.
[19] Wang Z, Liu J, Sun W. efectos de asiaticoside sobre los niveles de cy podocito - proteínas toesqueléy proteína del diafragma de slit renal sin adriamicina - en - nefropatía de rata producida [J]. Life Sci, 2013, 93 (8) : 352.
[20] Yang Guang, Tan Jiaju, Chen Huajin, et al. Efecto bloqueante de los asiaticosidos en la fibrosis hepática inducida por tetracloruro de carbono en ratas [J]. Journal of Gastroenterology and Hepatology, 2009, 18 (5) : 397.
[21] Hou Shqiang, Fang Ming, Chen Shasha, et al. Mecanismo de regulación bioquímica de la prevención de la reestenosis del stent por glucósidos de centella asiática [J]. Chinese Journal of Traditional Chinese Medicine, 2014, 39(8) : 1479.
[22] Jin Yan, Gao Xiaojie. Efectos del cumquatoside sobre la neuralgia periférica diabética y su mecanismo [J]. Farmacología y clínica de la medicina tradicional China, 2013, 29(5): 39.
[23] Qi FY, Yang L, Tian Z, et al. Efectos neuroprotectores de Asiaticoside [J]. Neural Regen Res, 2014, 9(13) : 1275.
[24] Xu CL,Wang QZ, Sun LM, et al. Asiaticoside: atenude la neurotoxicidad indupor MPTP en un modelo de rata de parkinsonismo a través de mantener el equilibrio redox y la regulación de la relación de Bcl-2 / Bax [J]. Pharmacol Biochem Behav, 2012, 100(3) : 413.
[25] Kumar A, Dogra S, Prakash A. efectos neuroprotectores de Centella asi- ática contra la disfunción cognitiva Intracerebroventricular inducida por colchicina y el estrés oxidativo [J]. Int J Alzheimers Dis, 2009, 2009:1.
[26] Chen Yao, Qin Luping, Zheng Hanchen, et al. Efectos de los asiaticosidos sobre las funciones neuroendocrinas en ratas deprimi[J]. Journal of Second Military Medical University, 2002, 23 (11): 1224.
[27] Luo L, Liu XL, Mu RH, et al. BDNF hipocampal señalización restaurada con el tratamiento crónico asiaticoside en ratones similares a la depresión [J]. Brain Res Bull, 2015, 114 :62.
[28] Wan J, Gong X, Jiang R, et al. Efectos antipiréticos y antiinflamatorios de asiaticoside en ratas tratadas con lipopolisacáridos a través de la regulación de la heme oxigenas-1 [J]. Phytother Res, 2013, 27 (8) :1136.
[29] Zhang Zhuo, Qin Dalian, Wan Jingmian, et al. Influencia de los glucósidos de centella asiática en el balance de factores inflamatorios en la lesión pulmonar aguda indupor LPS en ratones [J]. China Materia Medica, 2008, 31 (4) : 547.
[30] Qiu J, Yu L, Zhang X, Wu Q, et al. Asiaticoside atenúa la lesión pulmonar aguda indupor lipopo- lisacárido a través de la regulación descendente de NF- − B. Regulación de la vía de señalización NF - − B [J]. Int Immunopharmacol, 2015, 26(1) : 181.
[31] Zhang L, Li HZ, Gong X, et al. Efectos protectores de los asiaticosidos sobre la lesión hepática aguda inducida por lipopolisacárido/D - galactosamina en ratones [J]. Phytomedicine, 2010, 17 (10) : 811.
[32] Lin X, Huang R, Zhang S, et al. Efectos beneficiosos de asiaticoside sobre déficit cognoscien senescence - ratones acelerados [J]. Fitoterapia, 2013, 87 :69.
[33] Cheng CL, Guo JS, Luk J, et al. Los efectos curativos del extracto de Centella y asiaticoside sobre el ácido acético indujeron úlceras gástrien ratas [J]. 2004, 74(18) : 2237.
-
anterior
¿Cuál es el ingrediente activo de Centella Asiatica Extract?
-
siguiente
¿Cuál es el beneficio del Gotu Kola en bengalí?


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




