Estudio sobre polvo de licopeno sintético
Lycopene (C40H56) is a natural fat-soluble pigment of plant and microbial origin. Chemically, it is a carotenoid composed of a straight-chain hydrocarbon with 11 conjugated double bonds and 2 non-conjugated double bonds [1]. Lycopene can effectively scavenge free radicals in the body and quench singlet oxygen. Its ability to quench singlet oxygen is 2 times that of β-carotene and 10 times that of α-tocopherol[2]. It can be used as an effective antioxidant to reduce the damaging effects of oxidative stress on cells. More and more studies have shown that lycopene has a protective or intervention effect on chronic diseases such as type 2 diabetes, malignant tumors and Alzheimer's enfermedad, y por lo tanto atrae mucha atención en los campos de la alimentación, la industria química y la medicina. La organización de las naciones Unidas para la alimentación y la agricultura (FAO), el comité del Codex sobre aditivos alimentarios (CCFA) y la organización mundial de la salud (OMS) han identificado al licopencomo nutriente de clase a [3].
Con el creciente reconocimiento de los productos funcionales naturales, la investigación sobre el licopencomo aditivo alimentario funcional también se está profundizando. Sin embargo, el cuerpo humano no puede sintetizar el licopendirectamente y sólo puede obtenerlo de vegetales y frutas naturales o de la flora intestinal, y sus fuentes y cantidades son bastante limitadas. Este artículo se centra en la relación entre la estructura principal del polvo de licopeno, la biodisponibilidad y los factores influyentes, la vía de síntesis microbiana, las estrategias de síntesis de tres cepas de levadura para producir licopeno, y la relación y el papel de la aplicación de licopeno en la prevención de enfermedades crónicas. Proporciona una base teórica para la producción, utilización y exploración funcional del licopeno.

Estructura química y biodisponibilidad del licopeny sus análogos
La estructura molecular de la molécula de licopencontiene 13 enlaces dobles, 11 de los cuales se conju, lo que hace que el licopensea inestable y propenso a la isomeribajo la influencia de la luz, oxígeno, ácidos, catalizadores u otros cambios ambientales. El licopeno existe principalmente en dos conformaciones: el isótodo e (isótodo trans) y el isóz (isócis-trans) (figura 1). Más del 90% del licopennatural en frutas y verduras existe en la forma termodinámicamente más estable del isótodo e [4]; Sin embargo, los estudios han encontrado que más del 50% del licopenen el suero y los tejidos humanos se metaboliza en forma del isómero z [4]. Los isómeros z comunes son principalmente 5-cis, 9-cis, 13-cis y 15-cis licopeno. Estudios han mostrado que el 5-cis licopentiene mayor capacidad antioxidante y mayor biodisponibilidad que otros análogos [5].
Por lo tanto, la ingesta de 5-cis licopeno puede ser más beneficiosa para la salud humana que la ingesta de todo-e-licopeno y tiene un mayor potencial de aplicación en las industrias alimentaria y farmacéutica. En los últimos años, los investigadores han estado trabajando arduamente en el desarrollo de métodos para obtener altas concentraciones de z-licopeno, como el tratamiento térmico, el tratamiento con microondas, la irradiación de la luz, el tratamiento de electrólisis y el tratamiento catalítico. Sin embargo, estos métodos todavía pueden mejorarse. Por ejemplo, el calentamiento y el tratamiento por microondas pueden causar degradación debido a las altas temperaturas; El tratamiento fotoquímico también puede causar degradación debido a la conversión del isómero todo-e. Aunque el uso de fotosensibilizadores puede prevenir eficazmente la fotodegradación del licopeno, trae el reto de la eliminación de fotosensibilizador. Del mismo modo, si se utilizan reactivos químicos como electrolitos y catalizadores, la eliminación de sustancias tóxicas también es un gran reto.
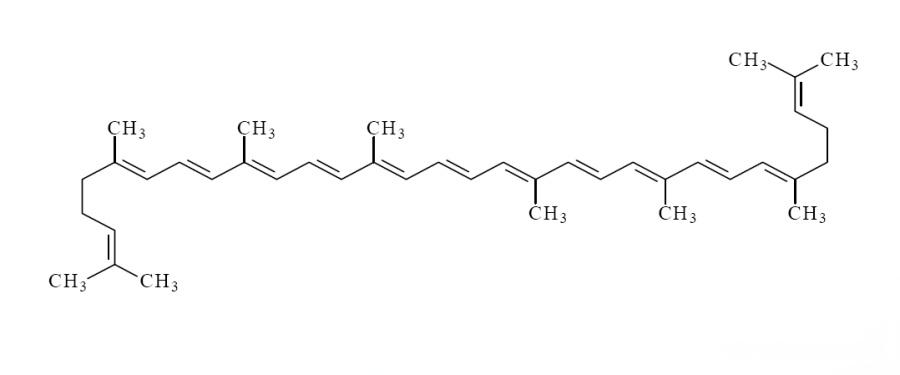
Hay dos razones principales que afectan la biodisponibilidad del licopenen polvo: si el licopense libera completamente de la matriz alimentaria y la fuerza de la emulsificación lipídependiente del licopeny y la formación de micelas [6] (figura 2).debido a la estructura química extremadamente hidrófoba del licopeno, la absorción directa y la tasa de utilización del licopenen las frutas y verduras por el cuerpo humano es muy baja [7]. Sin embargo, procesos como el tratamiento térmico durante el procesamiento de alimentos pueden dañar las membranas celulares y promover la liberación de licopendesde la matriz tisul, aumentando así la biodisponibilidad de licopeno. La biodisponibilidad del licopeno varía considerablemente según el método de tratamiento, siendo el orden de magnitud: Procesamiento suave > Tomates crudos [8]. Con el fin de mejorar aún más la utilización efectiva del licopeno, los investigadores han desarrollado con éxito sistemas de administración de licopencomo las emulsiones tradicionales, los portadores de nanoemulsión y los portadores de lípidos nanoestructurbasados en sus propiedades fisicoquímicas y características, como la estructura de las células del cuerpo (figura 3). Protegiéndolos de las condiciones adversas del tracto digestivo, y liberándolos en el sitio de absorción para una mejor absorción.
2 biosíntesis de licopeno
Natural lycopene is mainly derived from tomatoes and fruits such as grapefruit, melons, red guava, red carrots, and wolfberries. In addition, studies have confirmed that some microorganisms, including bacteria, fungi and algae, can accumulate lycopene under specific physiological conditions [9]. For example, the inactivation of lycopene cyclase leads to the interruption of the carotenoid pathway, which helps lycopene accumulate in Blakeslea trispora [10]. The Codex Alimentarius Commission (CAC) has approved three sources of lycopene: tomato extract, chemical synthesis, and Blakeslea trispora extract.
Among them, the tomato extraction method mainly uses vegetable and fruit raw materials rich in lycopene, which are extracted efficiently using various extractants. The advantage of this method is that it can achieve high-quality natural lycopene production in batches, but this method is susceptible to external factors such as the species, origin, and harvest season of the raw materials, which can affect the yield. In addition, large amounts of waste residue, waste liquid, and waste gas are generated during industrial production, which results in high comprehensive treatment costs. The chemical synthesis method is relatively mature, with mild reaction conditions, high recovery rates and low costs. It is currently the main technology for the industrial production of lycopene. However, lycopene has many C=C double bonds, making it difficult to control stereoselectivity. The reaction process is complex and has high technical requirements. There is also the safety issue of organic solvent pollution from the chemical reagents left over from the reaction. In recent years, with the analysis by scientists of the biosynthetic pathway of natural Polvo de licopeno and the great progress in modern microbial genetic engineering, other microorganisms (such as Saccharomyces cerevisiae, Pichia pastoris and Yarrowia lipolytica) can also be used as hosts for lycopene production. Because they have the incomparable advantages of no seasonal restrictions, high yield and a single product, they provide a new way of thinking for the large-scale industrial production of lycopene and have attracted the attention of researchers and the food and pharmaceutical industries.

2.1 vía biosintética del licopeno
En los organismos vivos, el licopense sintetiza principalmente a través de dos vías biosintéticas: la vía del mevalon(mevalon, MVA) y la vía del 2-metil-d-eritritol-4-fosfato (2-metil-d-eritritol-4-fosfato, MEP). Entre ellos, los eucariotas sintetizan principalmente licopeno y sus derivados a través de la vía MVA, mientras que los procariotas a menudo los sintetizan a través de la vía MEP. Ambas vías biosintéticas utilizan gliceraldehí3-fosfato (G3P), que es producido por el cuerpo#39;s metabolismo del azúcar, para catalizar una serie de enzimas metabólicas secundarias para sintetizar moléculas intermedias como el pirofosfato de isopentenilo (pirofosfato de isopentenilo, IPP) y su isómero 3,3-dimetilalilo difosfato (DMAPP) y otras moléculas intermedias. Posteriormente, la IPP y el DMAPP son condensados, modificados y alargpor enzimas para finalmente sintetizar licopeno (figura 4).
2.2 ingeniería metabólica de la levadura para la síntesis de licopeno
En la naturaleza, las levaduras como Rhodotorula glutinis, Rhodotorula graminis y Phaffia rhodozyma pueden sintetizar productos naturales carotenoides de forma autónoma, pero la cantidad y la actividad biológica de los productos sintetizados a menudo no pueden satisfacer las necesidades de la producción industrial [11]. Sin embargo, las levaduras de fermentación industrial comúnmente usadas como Saccharomyces cerevisiae, Pichia pastoris y Yarrowia lipolytica son altamente seguras, tienen herramientas de modificación genética maduras y han sido modificadas genéticamente para la investigación y producción de licopeno [12]. En respuesta a la falta de un sistema metabólico completo en S. cerevisiae y Y. lipolytica, y al hecho de que el proceso metabólico de la síntesis de carotenoides se detiene en el paso del difosfato de gerangeranilo (GGPP) [13], los investigadores han propuesto varias estrategias para construir cepas de levadura productoras de licopen(tabla 1); sin embargo, la mejora del título final de licopeny y el rendimiento sigue siendo un reto importante. Hay más estrategias reportadas para S. cerevisiae que para P. pastoris y Y. lipolytica, pero hay menos estudios sistemáticos de ingeniería sobre S. cerevisiae para lograr una alta producción de licopeno. La fuente de los componentes de la vía heteróloga y la eficiencia de la vía son factores clave para la producción de licopeno en S. cerevisiae [14]; el bajo rendimiento probablemente se deba a la falta de coordinación entre la vía endógena y la vía heteróloga.
Por lo tanto, con el fin de seguir explorando la adaptabilidad de la propia S. cerevisiae y la vía heteróloga, SHI B et al. [6] proporcionuna solución eficaz mediante la detección de genes de diferentes fuentes, como bacterias, levaduras, hongos, algas y plantas que participan en la biosíntesis de licopeno, como crtE (que codifica GGPP sintasa), crtB (que codifica octahidrolicopeno sintasa) y crtI (que codifica octahidrolicopeno deshidrogenasa) para mejorar la actividad catalítica; La combinación de los genes examinados evita la pérdida de pasos clave debido a un desequilibrio entre las vías metabólicas endógenas y exógenas; La eliminación de genes de derivendaumenta el suministro de la precursor acetil coenzima A (acetil coenzima A, acetil-CoA) y la utilización equilibrada de NADPH, se logró un sistema de inducde glucosa pura, y se construyó una cepa con el mayor rendimiento, BS106 (rendimiento de licopende 3,28 g/L). Esta cepa proporciona una referencia para mejorar la compatibilidad de S. cerevisiae's vía heteróloga para producir sustancias valiosas con antecedentes endógenos. En la actualidad, la producción microbiana de compuestos isoprenoides, incluido el licopeno, se enfrenta a dos desafíos potenciales: la vía natural de MVA o MEP está limitada por cofactores; La mayoría de los compuestos isoprenoides de cadena larga se almacenan principalmente en un espacio limitado debido a su hidrofobicidad, lo que evitará su acumulación a gran escala [15].
Para resolver ambos problemas, LUO Z S et al. [16] introdujeron la vía de utilización de isopentenol (IUP), que convierte isopentenol directamente a IPP, mejora la vía MVA, y aumenta el flujo de IPP y productos aguas abajo [14]. La combinación de IUP con alta hidrofobicidad convierte a Y. lipolyen un organismo productor de lípidos que es más propicio para la acumulación de compuestos isopentenilo soluen lípidos. Estas estrategias pueden ser ampliamente utilizadas con fines comerciales. P. pastoris fue seleccionado como productor de sustancias carotenoides porque también tiene importantes ventajas comerciales. P. pastoris tiene una alta calidad celular y puede crecer hasta densidades más altas que otras levaduras como S. cerevisiae sin acumular etanol y usando varios tipos de materia orgánica como fuentes de carbono. Por lo tanto, BHATAYA A et al. [17] aplicó por primera vez tecnología de ingeniería metabólica A P. pastoris, diseñy construyendo dos plásmido: el plásmido pGAPZB-EpBPI*P codifica la superóxido dismutasa objetivo, mientras que el plásmido pGAPZB-EBI* codifica la enzima no objetivo. Después de que estos dos plásmidos se transformen en P. pastoris, una cepa productora de licopende alto rendimiento del clde tipo v de P. pastoris que contiene el plásmido pGAPZB-EpBPI*P pudo ser seleccionada, sentando las bases para el desarrollo de la producción de licopenusando P. pastoris.
Con el rápido desarrollo de la biología sintética, la ingeniería de proteínas y la ingeniería metabólica, la levadura genéticamente modificada no sólo ha mejorado la eficiencia de producción de licopeno, sino que también ha aumentado la utilización de sustrde bajo costo, reduciendo aún más los costos de producción. Los microorganismos sintéticos sin duda ofrecerán nuevas opciones para la síntesis heteróloga de productos naturales.
3 bioactividad antioxidante del licopeno
Los estudios han demostrado que existe una relación entre el desarrollo y la progresión de enfermedades crónicas como los tumores malignos y el estrés oxidativo. El licopen, como un antioxidante natural, tiene el efecto de reducir el daño causado por el estrés oxidativo. La principal actividad antioxidante del polvo de licopenes actuar sobre los radicales libres como el peróxido de hidrógeno, dióxido de nitrógeno y los radicales hidroxilo para combatir la oxidde proteínas, lípidos y ADN. Cuando el licopeno se expone a oxidantes o radicales libres, los enlaces dobles se pueden romper o aumentar, destruyendo la cadena del polieno. Las posibles reacciones del licopeno con sustancias activas son [32]: la formación de aductos, la transferencia de electrones a radicales libres y la extracción de hidrógeno de los alelos (figura 5).la siguiente descripción se centra en la relación entre varias enfermedades crónicas y el estrés oxidativo y cómo el licopeninhilas mutaciones que conducen a enfermedades crónicas.
Las células tumorales suelen tener concentraciones excesivamente altas de especies reactivas del oxígeno (ROS) [33] y experimentan estrés oxidativo. Las ROS son productos metabólicos normales de las células que juegan un papel clave en la transducción de señales. Niveles altos de ROS en las células tumorales están involucrados en varias etapas de la tumorigénesis, tales como crecimiento de células tumorales, proliferación, invasión, angiogénesis y metástasis [34]. Se ha encontrado que el licopeny el cisplatino tienen un efecto sinérgico al inhibir el crecimiento de las células del carcinoma cervical humano (HeLa). Las tasas de supervivencia a 72 horas de las células HeLa tratadas con licopen(10 μmol/L) y cisplatino (1 μmol/L) solas fueron de 65,6 y 71,1%, respectivamente, y la viabilidad celular disminuyó a 37,4% después de la combinación. Además, en comparación con el grupo de control, el grupo de células tratadas con licopenmostró un aumento en la expresión del factor nuclear relacionado con el factor E2 (NRF2) y la concentración de NRF2 en el grupo combinado fue significativamente más alta que en el grupo de células tratadas con cisplatino solo. Estos resultados indican que es probable que el licopenejerza un efecto contra el cáncer al activar el NRF2 para mediar la tensión oxid[35] (figura 6).
La regulación anormal de la señal de NRF2 se asocia con muchas enfermedades relacionadas con el estrés oxidativo. La activación de NRF2 se considera una forma de inducir la capacidad antioxidante y aliviar la patología, principalmente a través de la inducde enzimas antioxidantes mediada por la señal NRF2. En otro estudio, se encontró que el licopenpuede inhibir la activación del potencide la cadena del factor nuclear − -luz de las células B activadas (NF- − B) y la expresión de los genes diana NF- − B (cIAP1, cIAP2 y supervivencia) al reducir las concentraciones de ROS intracelular y mitocondrial, induciendo la apoptosis de las células de cáncer de páncreas PANC-1. Estos hallazgos indican que la administración de suplementos de licopenpodría prevenir el cáncer de páncreas [36].
La inflamación es el cuerpo ' respuesta de la propia defensa. En el equilibrio normal del cuerpo, la inflamación sirve para eliminar los factores iniciales que causan daño celular, disponer de las células necróticas y tejido dañado causado por el daño y la inflamación, y llevar a cabo la reparación de tejidos. Esta respuesta natural, la inflamación aguda, es un mecanismo clave de supervivencia utilizado por todos los vertebrados superiores [37-38]. Sin embargo, si la inflamación aguda no se puede resolver, puede conducir a la inflamación crónica y puede ser un proceso destructivo. El tejido dañado libera citoquinas pro-inflamy otros mediadores inflambiológicos en el cuerpo#39;s, transformando así la inflamación tisular de bajo grado en inflamación sistémica [39]. Además, las enfermedades autoinmuny la exposición a largo plazo a los irritantes también puede conducir a un estado inflamsistémico. Una respuesta inflamatoria excesiva afectará negativamente al cuerpo 's reparación, y las células pueden volverse cancerosas bajo estimulación prolongada de la infiltración inflam[40]. Estudios han reportado que el licopenpuede mejorar el trastorno mitocondrial inducido por el lipopolisacárido en el cerebro y el hígado de ratones, reducir los niveles de expresión de citocinas pro-inflamatorias TNF-a, IL-1β y IL-6, y aliviar la neuroinflamación y la hepatitis [41].
4 conclusiones y perspectivas
This paper provides a systematic review of recent research progress on the structure, bioavailability, heterologous microbial synthesis strategies, and protection against oxidative stress in chronic diseases of lycopene powder. El licopenes un miembro de la familia de los carotenoides y su capacidad antioxidante tiene importantes beneficios para la salud. Esta propiedad ha generado un gran interés en su uso en formulaciones alimentarias. Para utilizar este compuesto, es necesario asegurar que los procesos de extracción y retención consideren plenamente los factores que afectan a la estabilidad y biodisponibilidad del licopen, con el fin de obtener un producto funcional altamente efectivo y de fácil uso.
Hay muchas técnicas tradicionales de extracción de sustancias bioactivas, incluyendo la extracción mecánica y ultrasónica, y la extracción con solventes orgánicos seguros. Sin embargo, debido a los avances en diversos campos, han surgido nuevos métodos alternativos, como la mezcla de alta cizadura, la homogeneia alta presión y el procesamiento microfluídico, que tienen un gran potencial para la extracción de licopeno. Además, la molienda ultrafina es una nueva opción que no sólo mejora la tasa de extracción de licopeno, sino que también es una buena opción para disolventes de calidad alimentaria. En términos de protección del licopeno, los sistemas de administración de licopense han convertido en un método alternativo para proteger y mejorar la utilización del licopenen el cuerpo. El desarrollo de portadores de nanoemulsión, portadores de lípidos nanoestructurados, hidrogeles y liposomas es una buena opción para mejorar la protección del licopeno.
In addition, the use of industrial yeast as a host cell to produce lycopene is also a brand new idea. Yeast that does not have a lycopene powder synthesis pathway can become a lycopene-producing strain by introducing genes from an external source. This strategy improves the production efficiency of lycopene and reduces production costs. Under the premise of achieving high lycopene yields, scholars can also develop other effective methods to synthesize other high-value carotenoids.
Referencia:
[1]SOUKOULIS C, BOHN T. A comprehensive overview on the micro- and nano-technological encapsulation advances for enhancing the Chemical stability and bioavailability of carotenoids[J]. Critical Reviews in Food Science and Nutrition,2018,58(1):1-36.
[2]PRZYBYLSKA S. lycopen— un carotenobioque ofrece múltiples beneficios para la salud: una revisión [J]. International Journal of Food Science & Tecnología,2020,55(1):11-32.
[3]LIANG X P, MA C C, YAN X J, et al. Avances en la investigación sobre bioactividad, metabolismo, estabilidad y sistemas de administración del licopeno [J]. Tendencias en ciencia alimentaria & Tecnología, 2019,93:185-196.
[4]CLINTON S K, EMENHISER C, SCHWARTZ S J, et al. Isómeros de licopencis-trans, carotenoides y retinolina en la próstata humana [J]. Biomarcadores de epidemiología del cáncer y Prevención,1996,5(10):823-833.
[5]HONDA M, KAGEYAMA H, HIBINO T, et al. Método eficiente y respetuoso con el medio ambiente para la extracción de carotenoides de Paracoccus carotinifaciutilizando catalizadores acelerde z-isomeriz[J]. Process Biochemistry,2020,89:146-154.
[6] el SHI B, MA T, YE Z L, et al. Ingeniería metabólica sistemática de Saccharomyces cerevisiae para la sobreproducción de licopeno [J]. Journal of Agricultural and Food Che- Mistry,2019,67(40):11148-11157.
[7]SHARIFFA Y N, TAN T B, ABAS F, et al. Producir una nanodispersión de licopen: los efectos de los emulsionantes [J]. Food and Bioproducts Processing,2016,98:210-216.
[8] honesto K N, ZHANG H W, ZHANG L. licopeno: efectos de isomerisobre la biodisponibilidad y las propiedades de bioactividad [J]. Food Reviews International,2011,27(3):248 — 258.
[9]FENG L R, QIANG W, YU X B, et al. Efectos de lípidos exógenos y aclial frío sobre la producción de licopeno y la composición de ácidos grasos en Blakesleatrispora[J]. AMB Express,2019,9(1).
[10]MEHTA B J, CERDAOLMEDO E. mutantes de producción de carotenen Blakesleatrispora[J]. Applied Microbiology and Biotechnology,1995,42(6):836-838.
[11]LI C J, ZHANG N, SONG J, et al. Un solo gen desaturasa de la levadura roja Sporidiobolus pararoseus es responsable de cuatro y cinco pasos de deshidrogendel fitoeno [J]. Gene,2016,590(1):169-176.
[12] Sun Ling, Wang Junhua, Jiang Wei, et al. Construcción de una cepa de levadura licopeno sintética de alta eficiencia [J]. Chinese Journal of Bioengineering, 2020, 36(7): 1334-1345.
[13]VERWAAL R, WANG J, MEIJNEN J P, et al. Alto nivel Producción de betacaroteno en Saccharomyces cerevisiae por transformación sucecon genes carotenogénicos Xanthophyllomyces dendrorhous[J]. Applied and Microbiología ambiental,2007,73(13):4342-4350.
[14]MA T, SHI B, YE Z L, et al. La ingeniería lipícombinada con la ingeniería metabólica sistemática de Saccharomyces cerevisiae para la producción de alto rendimiento de licopeno [J]. Ingeniería metabólica,2019,52:134-142.
[15]JING Y W, GUO F, ZHANG S J, et al. Avances recientes en la síntesis biológica del licopeno mediante el uso de levadura industrial [J]. Industrial & Engineering Chemistry Research,2021, 60(9):3485-3494.
[16]LUO Z S, LIU N, LAZAR Z, et al. Mejora la síntesis de isoprenoides en Yarrowialipolytica por Expresando la vía de utilización del isopentenol y modulando la hidrofobicidad intrac[J]. Ingeniería metabólica,2020,61:344-351.
[17]BHATAYAA, SCHMIDT-DANNERT C, LEE P C. Meta- bolic Engineering of Pichia pastoris X-33 for lycopeno production[J]. Process Biochemistry,2009,44(10):1095-1102.
[18]LI X, WANG Z X, ZHANG G L, et al. Mejorar la producción de licopenen Saccharomyces cerevisiae a través de la vía de optimización y el metabolismo del chasis [J]. Ciencia de ingeniería química,2019,193:364-369.
[19]HONG J, PARK S H, KIM S, et al. Producción eficiente de licopenen Saccharomyces cerevisiae mediante ingeniería enzimy aumento de la flexibilidad de la membrana y producción de NAPDH [J]. Applied Microbiology and Bio- Technology,2019,103(1):211-223.
[20]ALSHEHRI WA, GADALLAN O, EDRIS S, et al. Ingeniería metabólica de la vía mep para la sobreproducción de lvcopeno en Saccharomyces cerevisiae usando vectores pESC-LEU y pTEF1/Zeo [J]. Applied Ecology and Environmental Sesearch,2020,18(4):5279-5292.
[21]ZHANG Y, CHIU T Y, ZHANG J T, et al. Ingeniería sistemática de levaduras sintéticas para mejorar la producción de licopeno [J]. Bioengineering,2021,8(1):14.
[22]XU X, LIU J, LU Y L, et al. Ingeniería de caminos de Saccharomyces cerevisiae for eficiente Producción de licopeno [J]. Bioprocess and Biosystems Engineering, 2021,44(6):1033-1047.
[23]BIAN Q, ZHOU PP, YAO Z, et al. La biosíntesis heteróloga de la luteína en S. cerevisiae es posible gracias al control de la vía de producción de la misma [J]. Ingeniería metabólica,2021,67:19-28.
[24]SU B L, YANG F, LI A Z, et al. La secuencia de activación aguas arriba puede funcionar como un aislpara la regulación cromosómica de las vías heterólogas contra los efectos de posición en Saccharomyces cerevisiae[J]. Applied Biochemistry and Biotechnology,2022,194(4):1841-1849.
[25]SU B L, LAI P X, YANG F, et al. Ingeniería de un metabolismo balancede acetil coenzima a en Saccharomyces cerevisiae para la producción de licopeno mediante ingeniería racional y evolutiva [J]. Journal of Agricultural and Food Chemistry, 2022,70(13):4019-4029.
[26]ARAYA-GARAY J M, FEIJOO-SIOTA L, ROSA-DOS- SANTOS F, et al. Construcción de nuevas cepas de PichiapastorisX-33 para producción de licopeny betacaroteno [J]. Applied Microbiology and Biotechnology,2012,93(6):2483-2492.
[27]ZHANG X, WANG D, DUAN Y, et al. Producción de licopenmediante la ingeniería metabólica de Pichiapastoris[J]. Bioscience,Biotechnology, and Biochemistry,2020,84(3):463-470.
[28]LIU D, LIU H, QI H, et al. Construcción de vías quiméricas de levadura para impulsar la síntesis de terpenlipofílico [J]. ACS Synthetic Biology,2019,8(4):724-733.
[29]ZHANG XK, NIE MY, CHEN J, et al. Los integrales multicopia de los genes CRT y la coexpresión de la AMP deaminasa mejoran la producción de licopenen Yarrowia lipolytica[J]. Journal of Biotechnology,2019,289:46-54.
[30]XIE Y X, CHEN S L, XIONG X C. ingeniería metabólica de la levadura no productora de carotenoiyarrowialipolytica para la biosíntesis de zeaxantina [J]. Frente Microbiol,2021, 12:699235.
[31]LIU X Q, CUI Z Y, SU T Y, et al. Identificación de sitios de integración genópara el desarrollo de un kit de herramientas de expresión gébasado en crisp en Yarrowialipolytica[J]. Bio- tecnología microbiana,2022,15(8):2223-2234.
[32]MAGNE T M, BARROS A O D S D, FECHINE P BA, et al. El licopencomo plataforma multifuncional para el tratamiento del cáncer y la inflamación [J]. Revista Brasileira De farmacognosia — Brazilian Journal of Pharmacognosy,2022, 32(3):321-330.
[33]LIBBY P, BURING J E, BADIMON L, et al. Athero- la esclerosis [J]. Nat RevDis Primers,2019,5(1):56.
[34]GALADARI S, RAHMAN A, PALLICHANKANDY S, et al. Especies reactivas de oxígeno y la paradoja del cáncer: para promover o suprimir?[J]. Biología y medicina Radical libre, 2017,104:144-164.
[35]AKTEPE O H, SAHIN T K, GUNER G, et al. El licopensensibililas células de cáncer de cuello uterino al cisplatino por medio de la vía del factor nuclear Kappa B (NF-kappaB) [J]. Diario turco de ciencias médicas,2021,51(1):368-374.
[36]JEONG Y, LIM J W, KIM H. el licopeninhila la señalización NF-kappaB mediada por especies reactivas de oxígeno e induce apoptosis en células cancerosas de páncreas [J]. Nutrientes,2019, 11(4):762.
[37]TODORIC J, ANTONUCCI L, KARIN M. dirigido a la inflamación en la prevención y el tratamiento del cáncer [J]. Cancer Prevention Research,2016,9(12):895-905.
[38]MEDZHITOV R. origen y funciones fisiológicas de la inflación [J]. Nature,2008,454(7203):428-435.
[39]ARULSELVAN P, FARD M T, TAN W S, et al. Papel de los antioxidantes y productos naturales en la inflamación [J]. Medicina oxidy longecelular,2016,(13): 5276130.
[40]SINGH N, BABY D, RAJGURU JP, et al. Inflamación y cáncer [J]. Anales de la medicina africana,2019,18(3):121-126.
[41]WANG J, ZOU Q H, SUO Y, et al. El licopeno mejora la disfunción sináptica inducida por la inflamación sistmediante la mejora de la resistencia a la insulina y la disfunción mitocondrial en el eje hígado-cerebro [J]. Comida y comida Función,2019,10(4):2125-2137.


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés



