Natural Colorant Lutein Supports Clean Label Formulations
En hoy y#39;s global food industry, “clean labeling” is no longer an option but an imperative. Consumers are scrutinizing ingredient lists with unprecedented vigilance, demanding not just “no artificial colors” but expecting to see a roster of familiar, simple, and beneficial components. This marks the market's transition from the 1.0 phase of “removing negative ingredients” to a new 2.0 era of “enhancing product value through positive ingredients.”
However, this evolution presents new challenges for food brands: After removing synthetic dyes like Yellow No. 5 and Sunset Yellow, how can we simultaneously achieve these three objectives?
✨ Maintain or even enhance the product's visual appeal?
✨ Ensure the formulation's technical stability and reliability throughout its shelf life?
✨ Infuse the product with core value that consumers can clearly perceive?
If brands merely achieve “exclusion” without delivering “empowerment,” so-called clean-label products risk becoming bland in color and ambiguous in value, ultimately fading into obscurity amid fierce market competition.
It is precisely at this critical juncture that the value of Luteína natural comes to the fore. Far more than a direct substitute for synthetic colorants, it serves as a strategic ingredient capable of simultaneously fulfilling the triple roles of “natural coloring,” “clean labeling,” and “functional empowerment.” Choosing natural lutein means your product upgrade journey shifts from passively meeting market demands to proactively leading trends, building irreplicable core competitiveness for your brand.

I. How Natural Lutein Becomes the “Key Puzzle Piece” for Clean Label Formulations
On the path to clean label transformation, food companies require not just a simple pigment substitute, but a multifunctional solution that seamlessly integrates into modern food production systems. Green Spring Technology's natural lutein was developed precisely with this philosophy in mind, providing comprehensive support across three dimensions.
1.Label Purity: Ensuring Formulation Transparency from the Source
Ingredient List Optimization Solutions
·Can be labeled as “Marigold Extract” or “Natural Colorant (Lutein)”
·Complies with U.S. FDA 21 CFR 73.350 regulations
· Certified organic by USDA Organic and EU Organic
· Halal and Kosher certified to meet specific dietary requirements
2. Technical Stability: Performance Assurance for Clean Labels
Innovative Encapsulation Technology
Utilizes a patented triple-layer microencapsulation system:
· Inner protective layer: pH-responsive wall material maintains stability during processing
· Intermediate buffer layer: Plant-based protein matrix with heat denaturation temperature of 125°C
· Outer freshness-locking layer: Nanoscale lipid coating blocks moisture and oxygen permeation
Key Performance Data
· 98.2% pigment retention after 30 minutes at 95°C
· >96% activity retention after 6 months storage at 40°C/75% RH
· Suitable for broad pH range (3.0-8.0) in food systems
3. Dual Value Proposition: Functional Empowerment Beyond Coloration
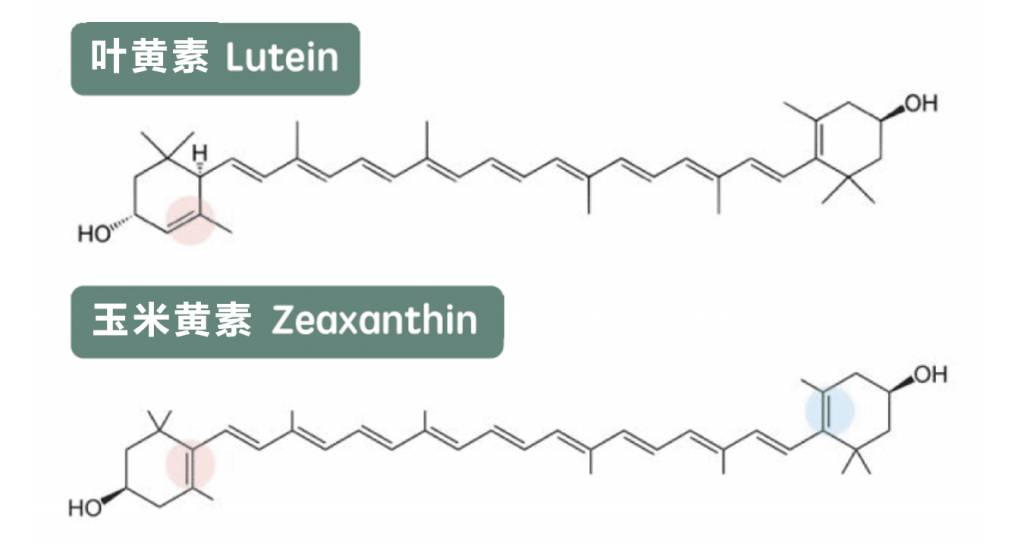
Visual Health Benefits
· Clinically proven: Daily intake of 10mg lutein effectively increases macular pigment density
· Helps filter harmful blue light, reducing eye strain from digital screens
· Exhibits antioxidant activity with ORAC value of 6,800 μmol TE/g
Market Differentiation Advantages
· Upgrades ordinary foods into functional foods
· “Eye protection” functionality has broad consumer recognition
· Synergizes with other nutrients for enhanced efficacy
Technical Director's In-Depth Analysis
“Our clean label solution must fulfill three criteria: label purity, production feasibility, and perceived value. Through technological innovation, Green Spring Technology's natural lutein unifies these demands into one solution, making clean labeling a competitive edge in the market.”
Quality & Safety Certifications
· Certified under BRC and IFS international food standards
· ISO 9001 Quality Management System and ISO 22000 Food Safety Management System certified
· Compliant with relevant U.S. FDA requirements
II. From “Clean Label” to “Brand Trust”
In the increasingly competitive food industry, clean labeling has evolved from a differentiator to a market entry requirement. Green Spring Technology's natural lutein solution empowers businesses to transform this “requirement” into tangible commercial value, building sustainable market competitiveness.
1. Establishing the Foundation of Brand Trust
Consumer perception studies reveal:
· 83% of consumers are willing to pay more for products with transparent ingredients
· 76% of buyers directly associate clean labels with “safer and healthier” products
· Over 90% of consumers show stronger purchase intent for products with clear functional claims
Pathways to Elevate Brand Value:
· Visualizing Trust: Establish formulation transparency through straightforward ingredient statements like “marigold extract”
· Value Perception: Transform clean labels from abstract concepts into tangible benefits by integrating “eye care functionality”
· Quality Traceability: Build comprehensive quality trust through certifications like BRC and IFS

2. Breaking Through Market Competition
Differentiated Competitive Advantages:
· Functional Differentiation: Only 17% of clean label products offer distinct visual health benefits, creating significant market opportunity
· Ingredient Differentiation: USDA Organic and EU Organic certified natural lutein meets premium market demands for stringent raw material standards
· Certification Differentiation: Halal and Kosher certifications serve as market access credentials for specific consumer segments
Market Expansion Proof:
After a partner company adopted our solution in their gummy products:
· Product premium increased by 25%, with repurchase rate rising 40%
· Successfully entered North American organic food retail chains
· Market share among Muslim consumers increased by 30%
3. Optimizing Product Value Structure
Cost-Benefit Analysis:
Tracking studies of partner companies reveal the following return on investment for Green Spring Technology's natural lutein:
Direct Economic Benefits
· Every RMB 1 invested in raw material upgrades yields RMB 3-5 in sales premium returns
· Shelf-life stability improved, reducing related losses by 15%
· New product development cycles shortened by 30%
Indirect Value Contribution
· Enhanced brand reputation drives organic traffic growth
· Premium channel penetration increased to 2.5 times that of traditional products
· Consumer loyalty index rose by 35 percentage points
III. Market Outcomes of Clean Label Transformation
Green Spring Technology's natural lutein solutions have been successfully validated across multiple global food brands. Below are three representative cases demonstrating how clean label transformation creates significant market value for enterprises.
Case 1: Quality Breakthrough for a Functional Gummy Brand
Background Challenge
An emerging functional gummy brand sought to establish a premium product line while facing dual challenges: achieving clean label transformation in formulations and establishing clear product differentiation.
Solution
The brand adopted Green Spring Technology's natural lutein solution:
1. Utilized ingredients certified by USDA Organic and EU Organic
2. Expanded into Middle Eastern and Southeast Asian markets through Halal certification
3. Established core product selling points centered on visual health benefits
Transformation Outcomes
· Achieved 180% sales growth within 6 months
· Successfully entered North American Whole Foods Market and European organic food chains
· Increased product repurchase rate to 52%
· Awarded the 2023 “Best Clean Label Innovation Award”
Case 2: Brand Upgrade for a Traditional Beverage Company
Background Challenge
A 50-year-old juice beverage company faced brand aging, needing to attract younger consumers through product upgrades while retaining its existing customer base.
Innovative Measures
The company implemented phased product innovation:
1. Replaced synthetic dyes with natural lutein using clean label ingredients
2. Obtained ISO 22000 and BRC certifications to strengthen quality reputation
3. Developed “Eye Care Juice” series emphasizing functional benefits

Market Response
· Brand recognition among 25-35 year-olds increased by 45%
· Average selling price rose by 20%, market share grew by 15%
· 92% customer retention rate achieved while expanding customer base
· Secured premium shelf space in major supermarket chains
Case 3: International Breakthrough in Infant Formula
Background Challenge
An infant formula company planned international expansion but faced product formulation issues that failed to meet target market certifications and consumer preferences.
Upgrade Solution
Leveraging Green Spring Technology's comprehensive certification support:
1. Adopted Kosher-certified ingredient formulations
2. Established an international quality image through IFS certification
3. Developed a clean-label eye-care nutrition series
Significant Outcomes
· Successfully entered premium maternal and infant markets in the EU and North America
· Achieved 320% annual export growth
· Became the top seller in its niche category on international e-commerce platforms
· Earned recommendations from pediatric nutrition experts in multiple countries
Client Testimonial
"Choosing Green Spring Technology marked a pivotal turning point for our brand. Their natural lutein not only enabled our clean label transformation but, more importantly, provided us with a passport to global markets. Today, ‘clean label + eye care functionality’ has become our most core brand asset."
IV. Take Action Now to Launch Your Clean Label Upgrade!
Get Your Customized Solution & Samples
· Free Download: Clean Label Solutions White Paper
· Request Samples for Effectiveness Verification
· Schedule a One-on-One Expert Consultation
Información de contacto
· Technical Support: +86 29 88313578
· Sample Requests: helen@greenspringtech.com
· Online Consultation: WhatsApp: +86 13649243917
(Please include your company name and product category for tailored assistance)
Contact us now to make clean labels your competitive edge!
referencias
[1] Shi Gaofeng, Li Ganggang, Li Na, et al. Investigación del proceso de extracción de ésteres de luteína en caléngoldos [J]. Food Science and Technology, 2010, 35(9): 254-257.
[2] Chen Zhiwen. Debate sobre el desarrollo de la industria del caléndula en el condado de Qiubei [J]. Yunnan Agriculture, 2017(8): 70-71.
[3] Zhang Hui, Li Tao, Xu Gongshi. Un coloralimentario natural con un futuro prometedor: la luteína [J]. China Food Additives, 2004(5): 45-48.
-
anterior
Highly Bioavailable Lutein for Enhanced Eye Care Formulas
-
siguiente
Say Goodbye to Synthetic Dyes? Marigold-Derived Lutein Offers a Natural Coloring Solution


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




