Estudio en ginsenósido raro Rg1 Rb1
Ginseng (PanaxGinseng C. A. Meyer) is a perennial herb enelfamily Araliaceae yis a traditional precious Chinese medicine. ginsenósidosare one deelmaenactive ingredients deginseng. They belong to the group detriterpenoid glycosides yare formed porthe condensatieldea sugar ya glycoside precursor. Studies have shown that ginsenósidoshave a variety depharmacological effects [1-3]. After oral administration, most protopanaxadiol-type ginsenósidosare hydrolyzed by intestinal flora to ginsenosideC-K, Rg3, Rh2and PPD[4-5], and protopanaxatriol-type ginsenosides are mainly degraded to ginsenoside F1 and 20(S)-PPT[6- 7]. The metabolite C-K deprotopanaxadiol-type ginsenosides has significant antitumor activity in vitro and in vivo, and suactivity is enhanced compared to the precursor[8]. Rg1, Re and 20(S)-PPT have a strong anti-tumor célulametastasis effect after oral administration, while only 20(S)-PPT has an anti-tumor effect when administered intravenously, indicating that the anti-tumor metastasis effect of Rg1 and Re after oral administratielis produced by their metabolite 20(S)-PPT [9].
Un gran número de estudios han demostrado que el ginsenósido es deglucosilado por bacterias intestinales para producir ginsenósidos raros con dos o un solo enlace glicosídico, que tienen una actividad biológica más fuerte [10].

La biotransformación puede cambiar la estructura química de los ginsenósidos, mejorar efectivamente la utilización in vivo de los ginsenósidos, optimizar la eficacia clínica del fármaco y reducir las reacciones adversas [11]. La biotransformación de los ginsenósidos incluye cambios en la glicosilación, hidroxilación, y enlaces dobles. La glicosilación de los ginsenósidos se produce principalmente en C-3, C-6 y C-21, incluyendo la hidrólidel glucósido y glicosilación; También se producen algunas transformaciones en las cadenas laterales C-3, C-12 y C-17, conectando grupos metilo y grupos hidroxilo; La modificación de dobles enlaces implica principalmente la adición u oxiddel doble enlace C-24/C-25. Este artículo revisa el desarrollo de la biotransformación microbiana de ginsenósidos raros en los últimos años, los cambios estructurales del núcleo de origen y la aplicación de sus derivados, con la esperanza de proporcionar una base teórica para la investigación estructural y la aplicación de los ginsenósidos y sus derivados.
1 estructura y aplicación de ginsenósidos raros
1.1 estructura de ginsenósidos raros
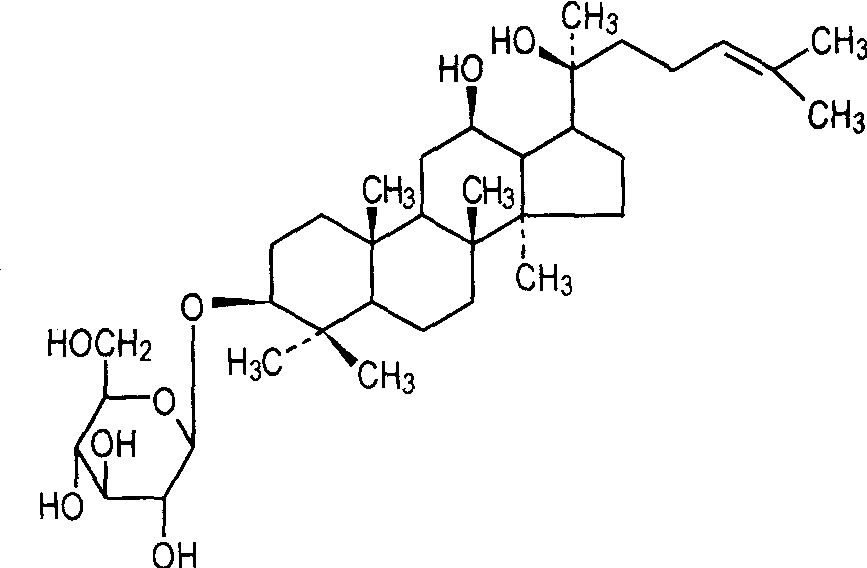
Los ginsenósidos se dividen en triterpenoides tetracíclicos y triterpenoides pentacíclicos de acuerdo con la estructura de la aglicona. Los ginsenósidos de tipo protopanaxadiol (Fig. 1a) y los ginsenósidos de tipo protopanaxatriol (Fig. 1b) son de tipo dammarano triterpenoide tetracíclic, las saponinas de tipo oxitirone (figura 1c) son un tipo de saponde triterpénico tetracícliccon una cadena lateral que contiene un anillo furano; Las saponinas tipo oleanano con ácido oleanólico como núcleo parental pertenecen a las saponinas triterpenpentacíclic(figura 1).
El nombre "ginsenósiraro" se deriva del hecho de que están presentes de forma natural en cantidades bajas o casi inexistentes. Los ginsenosidos raros son principalmente saponinas tipo Damasco, con no más de tres fracciones de azúcar Unidas a las posiciones C-3, C-6 y C-20 de la aglicona, ycon no más de dos fracciones de azúcar Unidas a una sola posición. Ginsenósidos raros se obtienen principalmente por deglicosilación o deshidratde ginsenósidos. En la actualidad, los principales ginsenósidos identificados son Rg3, Rg1, Rh1, Rh2, Rh3, RT3, F1, F2, C-K, PPD,PPT, etc., como se muestra en la tabla 1.
1.2 aplicación de saponinas raras de ginseng
raroginseng saponins are mainly found in red ginseng and black ginseng, and are the basis of the physiological activity of red ginseng and black ginseng, which is different desdethat of ginseng. Polvo de Ginseng en polvo and ginseng tablets sold on the marketonly grind the raw materials (ginseng, American ginseng, etc.) from which ginseng saponins are extracted intopowder, or add excipients and then press into tablets. Ginseng saponin tablets and capsules only extract the total ginsenosides from the medicinal herb, without further separation or transformation. This directly extracted ginsenoside needs to be broken down by specific enzymes before it can be absorbed by the body. However, these enzymes are either rare or absent in the human body. This results in low bioavailability and weak pharmacological effects in the human body.
En la actualidad, la mayoría de las raras preparaciones de ginsenósido en China contienen los componentes monoméricos Rh2 o Rg3. En el cuadro 2 se muestran los preparados que contienen un solo tipo de monómero ginsenósido.
Common rare ginsenosides such as ginsenoside C-K, Rg3 and Rh2 have been used in clinical applications to improve the body's en combinación con otros fármacos para terapia adyuvante. Mientras tanto, la investigación de aplicación de ginsenósidos raros sigue siendo una parte importante del desarrollo de ginsenósidos. Usando 20(R) -ginsenósido como materia prima, los investigadores sintetizaron un nuevo derivado del glicato de ginsenósido a través de una reacción de esterificación entre la posición C-3 y la glicina tert-butoxilcarbonilo. Y determinó que la actividad antitumoral de este derivado es más de 100 veces la de 20(R) -ginsenósido (IC50 > 30 mmol/L). El efecto inhibidor in vivo de A11 es más significativo que el de 20(R) -ginsenósido (P < 0,01). Al mismo tiempo, el A11 inhila la proliferación, migración e invasión de las células HeLa de forma dosidependiente y promueve la apoptosis [12]. Ginsenósido Rg4 es un ginsenósido raro que se encuentra en las hojas de ginseng y ginseng negro. Rg4 inhila la inflamación y exhibe efectos protectores contra la sepsis inducida por CLP [13]. Rg5 forma un complejo estable con el receptor purinérgico humano 12 (P2RY12) a través de interacciones alostéricos, reduciendo su actividad a través de los residuos E188 y R265, resultando en una disminución en la liberación de interleucina (IL)-6, IL-1 - y factor de necrosis tumoral - - en el plasma sanguíneo, mejorando la respuesta inflamatoria al tiempo que inhila la formación de trombvenosos [14]. El ginsenósido Rk1 tiene antitumoral [15], regula el azúcar en la sangre [16-17], protege el sistema nervioso [18-19], y cuando se utiliza en combinación con el ginsenósido Rk5, promueve la diferenciación de osteoblay el crecimiento mediante el aumento de la actividad de la fosfatasa alcalina, por lo tanto el tratamiento de la osteoporosis [20]. unmedida que avanza la investigación, se descubrirán más actividades biológicas de ginsenósidos raros y sus derivados.

2 estado de investigación de la biotransformación de ginsenósidos raros
Los principales métodos de transformación de ginsenósido son la transformación química y la biotransformación. La transformación química utiliza principalmente reacciones tales como hidróliácibase de enlaces glicosídicos, adición oxidy acetilpara cambiar sustitusustitu. La biotransformación utiliza células microbipara modificar la estructura de los sustratos exógenos, y utiliza una o más enzimas producidas durante el metabolismo para catalizar reacciones en partes específicas (grupos) del sustr, aumentando así el contenido y las propiedades medicinales de los principios activos [21]. Los métodos de bioconversión incluyen la transformación bacteriana, la transformación de la flora intestinal, la transformación fúny la catálisis enzimin vitro, que compenlas las deficiencias de los métodos de transformación química, como las condiciones de reacción drásticas, la contaminación ambiental y la generación de subproductos. Son ampliamente utilizados en investigación y producción. Los principales tipos de reacción de biotransformación incluyen reacciones de hidrólisis del glicósido y reacciones redox [22], entre las cuales las reacciones de hidrólidel glicósido son las más utilizadas [23]. En los últimos años, la reacción de adición en las posiciones C-24 y C-25 también se ha aplicado gradualmente en la producción práctica.
2.1 glucoside hidróliof Rare ginseng saponins
2.1.1 hidrólide glucósido microbiana de las saponinas de ginseng
The metabolic pathway of ginseng saponins in vivo is an importantepart of the research on the structure-activity relationship of ginseng saponins. Stepwise deglycosylation is the main metabolic pathway of ginseng saponins in vivo. The rare ginseng saponins and aglycones produced by metabolism have significant pharmacological effects in the body. The main transformation products of ginsenoside Rd were found to be F2, Rg3, C-K, Rh2 and PPD; the main transformation products of ginsenoside F2 were C-K and PPD; the main transformation products of ginsenoside Rg3 are Rh2 and PPD[24]; and C-K and Rh2 can be converted to PPD[25]. Through the analysis of the transformation products of protopanaxatriol-type saponins Re, Rg1, Rh1, Rf, F1 and R1 in the human intestinal flora, their metabolites and transformation pathways were determined i.e., the conversion pathway of ginsenoside Re is Re →Rg1/Rg2 →Rh1/F1 →PPT; the conversion pathway of ginsenoside Rg1 is Rg1 →Rh1/F1 →PPT; the conversion pathway of ginsenoside Rf is Rf→Rh1 →PPT; and the metabolic pathway of notoginsenoside R1 is R1 →Rg1/Rg2 →Rh 1 →PPT[26].
La vía metabólica del ginsenósido Rb1por bacterias intestinales in vitro es un proceso de deglucosilación, yla hidrólisis del ginsenósido Rb1 por bacterias intestinales in vitro es también un proceso de deglucosilación por etapas [27]. Lo mismo es cierto para el metabolismo ginsenósido por las bacterias intestinales in vivo. GUO etAl.[28] usaron antibióticos de amplio espectro para construir un modelo de ratas libres de gérmenes y verificaron la conversión de saponinas de notoginseng (1,535 g/kg) por la microbiota intestinal en ratas. Los resultados mostraron que los cuatro metabolitos ginsenósido F1, Rh2, C-K y PPT fueron detectados en el plasma de las ratas libres de germenes, pero no en el plasma de las ratas con germenes positivos. Por lo tanto, se infique la ley básica del metabolismo ginsenósido in vivo es tetraglycoside → trisacárido → disaccharide → monosaccharide → aglicone.
Hay muchos tipos de enzimas presentes en los microorganismos, que tienen el potencial de convertir glucósidos [29]. Al mismo tiempo, los azúcares eliminados después de la fermentación se pueden utilizar como una fuente de carbono para el crecimiento y la reproducción de hongos, metabolizando así para producir más enzimas [30]. Por lo tanto, diferentes microorganismos pueden ser utilizados como biocatalizadores para jugar un papel importante en la biotransformación de productos naturales. Académicos en el país y en el extranjero han utilizado bacterias y hongos para llevar a cabo investigaciones de biotransformación en ginsenósidos (figura 2).
Los estudios han demostrado que algunos hongos y bacterias como Aspergillus niger, Fusarium sp., Penicillium sp., Cordyceps sinensis y Armillaria mellea, Bifidobacterium breve, Bacillus sp., Lactococcus lactis y Lactobacillus plantarum sub sp., Terrabacter sp., Cellulosimicrobium cellulans sp., Y Thermotoga thermarum puede metabolizar los grupos de azúcar en el ginsenósido C-3 o C-20 para producir ginsenósidos raros o ageconas (tabla 3). Aspergilniger puede metabolizar el ginsenósido Rb1 y Rb3 a los ginsenósidos Rd, F2 y C-K, respectivamente [31, 38]; También puede hidrolizar el 3-O-Glc de los ginsenósidos Rb2 y Rc primero, y luego hidrolizar el 20-O-Ara para producir una única vía de hidrólisis: Rb2 − C-O − C-Y − C-K, Rc − C-Mc1 − C-Mc − C-K, y principalmente a través de la vía de Rb3 − C-Mx1 − C-Mx − C-K para hidrolizar el 3-O-Glc de Rb3, y lentamente hidroliza Rb3 20-O-Xly a través de la vía Rb3 − Rd − F2 − CK [38]. Penicillium hidroliza ginsenósidos y monómeros ginsenósia través de la vía Rb1 → Rd → F2 → C-K, produciendo ginsenósidos raros [32-33,52]; Fusarium convierte las saponinas totales ginsenósidas a ginsenósido raro C-K a través de un cultivo de fermentación [47]; Bifidobacterium fermentum puede convertir ginsenósido F2 a ginsenósido C-K [39]; Bacillus subtilis hidroliza las posiciones C-3 y C-20 del ginsenósido Rb1 en las posiciones C-3 y C-20 de la aglycone, respectivamente, para generar ginsenósidos Rd, Rg3[39] y Gyp-xⅦ, F2[40]. Los genesde glucosidasa clonados de Lactococcus lactis[36] y Thermus thermophilus[42-43] fueron expresados en Escherichia coli para producir glucosidasas que pueden hidrolizar gradualmente las partes externas e internas de glucosa de las posiciones C-20 y C-3 del ginsenósido Rb1. La reacción es la siguiente: Rb1 − Rd − Rg3 (S) y F2 − C-K.
In recent years, edible fungi have also been used in the study of the glycosidase hydrolysis of ginseng saponins. For example, Cordyceps militaris can convert ginseng saponin Rb1 to the rare ginseng saponin F2, with the conversion pathway being Rb1→Rd→F2 [44]. The honey ring fungus can convert ginsenoside Rb2 into the rare ginsenosides C-Y and C-K, with the conversion pathway being Rb2→C-Y→C-K [45]. This is the first time in the literature that a basidiomycete has been used to convert ginsenoside Rb2 into the rare ginsenoside C-K.
La transformación microbiana tiene sus propias ventajas únicas. Las condiciones de reacción son suaves, y en comparación con los métodos de transformación física y química, no requiere altas temperaturas y presiones, lo que reduce los costos. Durante la reacción, casi no se utilizan reactivos orgánicos, lo que puede asegurar la actividad de los ginsenósidos en mayor medida. Las enzimas secretadas por los microorganismos pueden descomponer y consumir impurezas como azúcares y proteínas, aumentar la concentración de ginsenósidos, y aumentar la tasa de conversión. El método de conversión microbiana tiene una alta eficiencia de utilización de materias primas y una alta eficiencia de conversión, que no sólo ahorra materias primas, sino que también aumenta la producción [46].
2.1.2 hidrólienzimdel grupo de azúcares de los ginsenósidos
La especificidad de la conversión microbiana es menor que la de la conversión enzimdirecta, por lo que la actividad de la glicosidasa necesita ser ajustada para limitar la producción de subproductos y mejorar la especificidad de la conversión.
Las saponinas tienen diferencias estructurales y diversidad funcionAl.La estructura de la saponina del Ginseng incluye de 1 a 4 enlaces glicosídicos. Los azúcares comunes incluyen − -glucosa, l-arabinosa, d-xilosa y l-rinosa, que requieren la acción sinérgica de diferentes enzimas para lograr la bioconversión. Las enzimas comunes incluyen glucosidasa, mannosidasa, arabinosidasa y xilosidasa, que son principalmente aisladas y puride microorganismos o animales y plantas. En el estudio de la conversión enzimde los ginsenósidos, los investigadores utilizaron por primera vez enzimas producidas por microorganismos naturales para hidrolizar los enlaces glicosídicos de los ginsenósidos. Por ejemplo, utilizando Monascus purpureus, que puede producir − -glucosidasa extracelularmente, al fermentar los ginsenósidos lograron un incremento de 2,3 veces en la fracción másica de Rg3 en los ginsenósidos [57]. A medida que avanla la investigación, los investigadores extrarelativamente pura − -glucosidasa de hongos, animales y plantas para hidrolizar ginsenósidos. Jin etAl.[58] usaron − -glucosidasa para convertir los ginsenósidos Rb1, Rb2, Rc y Rd se convirtieron en la rara saponina Rh2 usando − -glucosidasa. Sin embargo, las enzimas aisladas de microorganismos y animales y plantas son en su mayoría enzimas mixtas, que son difíciles de convertir de una manera específica y tienen muchos productos de reacción secundarios, lo que aumenta la dificultad de aislar y purificar los productos de conversión.
Con el desarrollo de la biología molecular yla tecnología de ingeniería genética, el uso de la tecnología de recombinación genética para construir bacterias genéticamente modificadas para llevar a cabo la glicosilación de saponde ginseng es una manera eficaz para mejorar la eficiencia de conversión. Las células de Escherichia coli y de levadura, como huéspedes maduros de expresión, se utilizan a menudo como vectores de expresión preferidos para proteínas enzimbiológicas recombinantes. La introducción del gen glicosiltransferasa en la célula del vector produce eficientemente ginsenósido Rh2 [59]. En los últimos años, el gen xilosidasa xln-DT de una bacteria termófila se ha recombinado en el plásmido pET-20b aguas abajo del péptido señal pelB utilizando tecnología de empalme genético. El plásmido recombinpelb-xln-dt se transformó en el hospede expresión de E. coli E. coli BL21 (DE3), y la enzima se utilizó como catalizador para hidrolizar el enlace glicosídico de la saponr1 de notoginseng. Y produjo con éxito ginsenoside Rg1[44]. Jeon etAl.usaron glucosidasa recombin(MT619) para convertir el ginsenósido Re, y la vía de conversión fue Re →Rg1 →F1 →MT1[60]. MT1 es un nuevo tipo de ginsenósido PPT. El gen que codifica -glucosidasa de dos cepas de bacifue clonado y altamente expresado en E. coli BL21 (DE3). Usando extracto crudo BL21 (DE3) para hidrolizar el ginsenósido Rb1 para producir ginsenósido F2[40]; La enzima recombinexpresada en tándem en E. coli es de mayor pureza y puede convertir los ginsenósidos de tipo ppen el raro ginsenósido Rh2(S)[61].
Actualmente, la mayoría de los estudios utilizan una sola enzima para convertir ginsenósidos. Por lo tanto, estudios futuros pueden utilizar la tecnología de recombinación genética para expresar enzimas con diferentes funciones en el mismo huésped. A través del efecto sinérgico de diferentes enzimas, se puede lograr el objetivo de producir ginsenósidos raros y sus derivados que satisfnecesidades específicas, mejorando así la tasa de utilización de los recursos de ginseng.
2.2 modificación microbiana de la estructura aglicona de los ginsenósidos
La investigación sobre la modificación estructural de las agliconas ginsenósise ha centrado principalmente en los ginsenósidos de tipo pp, y se han obtenido derivados como 25-OH-PPD y 25-OCH3-PPD. Los métodos de derivatización son generalmente métodos químicos y físicos, y ha habido pocos estudios sobre el cambio de la estructura aglicona por métodos biológicos. Los principales métodos que se han reportado son la hidratdel doble enlace en la posición C24-C25, en ratas. La principal vía metabólica de 20S-dammar-24-en-2 −, 3 −, 12 −, 20-tetrol (GP) observada es la oxiddel enlace 24,25-doble para formar el 24,25-epóxido, seguido por hidróliy rearreglo para formar el 20,24-epóxido (figura 3) [62]. Los investigadores han utilizado el co-cultivo de saponinas de ginseng y Cordyceps militaris para convertir ginsenósido Rg1 a 25-OH-(S/R)-Rh1 y panaxósido R1 a 25-OH-20(S/R)-R2. El contenido de derivados de 25-OH en los productos de conversión es mucho más alto que el de ginsenoside Rh1 y panaxoside R2 por lo que es fácil de aislar y puriel derivado [63-64]. Usando Mucor spinosus en cocultivo con 20(S)-protopanaxatriol, se obtuvieron seis derivados. Los resultados del estudio demostraron que los derivados de ginsenósiproducidos por deshidrogenación en la posición C-12 seguida de hidroxilación adicional en la posición C-7 o C-11 y carbonilación en la posición C-15, así como el rearreglo de doble enlace en la posición C-26, tienen una actividad inhibitoria significativa contra las células cancerosas [65].
De acuerdo con la investigación nacional y extranjera, se especula que este puede ser el sistema biocatalítico más eficaz para la hidroxilregionalmente selectiva de los ginsenósidos. Estudios experimentales han encontrado que estos derivados ejercen diferentes efectos in vivo e in vitro a través de diferentes mecanismos, y su actividad biológica es mayor que la de los ginsenósidos comunes [66]. Por ejemplo, Rb1 experimenta una reacción de deshidrogenación para formar dihidroginsenósido Dg-Rb1, que puede reparar neurondañadas sin afectar los parámetros sistémicos, y la dosis efectiva de Dg-Rb1 es 10 veces menor que la de Rb1 [67]. El derivado de éster de octilo Rh2-O del ginsenósido Rh2 tiene una actividad anticancermás alta que el Rh2 al activar la vía intrínseca de la apoptosis [68]. Los derivados acetil de PPD tienen importantes actividades de inducantiproliferativa y apoptótica y algunos derivados tienen una actividad anticancermás alta que PPD [69]. El anillo de pirazina se introdujo en el 25-OH-PPD para mejorar su actividad antitumorAl.La 2-pirazina-ppd puede inhibir significativamente la proliferación de células de cáncer gástrico y tiene poca toxicidad para las células normales (línea celular epiteligástrico humano GES-1) [70]. El derivado 25-OH-PPD de la aglicona PPD tiene mejor actividad anticancerque los fármacos existentes en el mercado como el ginsenósido Rg3, paclitaxel y ácido aminolevulínico [71].
Por lo tanto, mientras se mantiene la estructura activa original del ginsenósido, la estructura aglicona del ginsenósido puede ser modificada mediante la introducción de grupos polares y grupos farmacóforos para mejorar la solubilidad en agua, la orientación y la eficacia del ginsenósido, y mejorar la biodisponibilidad del ginsenósido.
2.3 glicosilación de ginsenósidos
A partir de 2,3-oxidosqualene, elBiosynthesis of ginsenosides (en inglés)Se puede dividir en tres pasos: 2,3-oxidosqualene ciclas(OSC) cícliz2,3-oxidosqualene; Las reacciones de hidroxilación y glicosilación son llevadas a cabo por citocromo (Cyt) y glicosiltransferasa (GT), en última instancia produciendo ginsenósidos [72]. La enzima UGT es una de las enzimas más críticas en la síntesis de ginsenósidos raros en organismos vivos [73] y es también el paso final en la biosíntesis de ginsenósidos. El gen UGT fue clonado a partir de Lactobacillus rhamnosus y expresado en E. coli BL21 (DE3). La proteína UGT recombinpuede convertir Rh2 en dos ginsenósidos nuevos, el ginsenósido glucosilado Rh2 y el ginsenósido diglucosilado Rh2 [74].
El triterpenoide aglycon es catalizado por UGT para formar ginsenósidos con diferentes estructuras. El protopanaxadiol tipo aglicon se glicosilado en las posiciones C-3 y C-20, y el protopanaxatriol tipo aglicon se glicosilado en las posiciones C-6 y C-20 [80]. La rara vía de glicosilación ginsenósido se muestra en la figura 4. La glicosiltransferasa 73C5 (UGT 73C5) fue aislada de Arabidopsis thaliana y añadipaso a paso a PPD. Esta glicosiltransferasa puede transferir selectivamente glucosa al grupo hidroxilo C-3 de PPD para sintetizar ginsenósido Rh2, logrando el mayor rendimiento reportado de ginsenósido Rh2 (3,2 mg/mL) [75]. La glicosiltransferasa 74AE2 (UGT 74AE2) cataliza la transferencia de glucosa a los grupos hidroxilo C-3 de PPD y C-K para formar Rh2 y F2, respectivamente [76]. La glucosiltransferasa 94Q2 (UGT 94Q2) puede transferir glucosa a Rh2 y F2 para formar Rg3 y Rd, respectivamente [77]. UGT51 es una de las glicosiltransferasas en Saccharomyces cerevisiae S288c [78], que puede transferir glucosa al grupo hidroxilo C-3 de PPD para formar Rh2 [79]. La investigación futura sobre UGTs puede proporcionar conocimientos sobre el mecanismo regulador de la glucosilación ginsenósido y ofrecer nuevas formas de modificar la producción de ginsenósido.
Como el factor directo que cataliza la formación de ginsenósidos, los UGTs juegan un papel vital en la producción de ginsenósidos por biocatálisis. La mayoría de los UGTs derivados de plantas tienen baja actividad catalítica, mientras que los UGTs microbirecombintienen propiedades biocatalíticas especiales, como la promiscuidel sustry altos niveles de expresión en células de sustrmicrobi, que los hacen herramientas eficaces para la producción de ginsenósidos. Por lo tanto, es necesario mejorar la actividad catalítica de UGTs con el fin de aumentar el rendimiento y la producción de los ginsenósidos raros objetivo.
3 conclusión y perspectivas
Studies have shown that rare ginsenosides have higher medicinal value. Al mismo tiempo, la baja solubilidad en agua y el bajo contenido de ginsenósidos raros han limitado su aplicación. La hidrólisis o glicosilación de los ginsenósidos por enzimas intra o extracelulares de diferentes microorganismos convierte efectivamente los ginsenósidos polisacchridos y las agliconas inactivas en ginsenósidos raros, mejorando así la biodisponibilidad de los ginsenósidos.
Los estudios han encontrado que los cambios en algunos grupos funcionales pueden cambiar la estructura molecular y las propiedades, lo que afecta la Unión de los fármacos a los receptores y afecta la eficacia. Por ejemplo, los grupos alquilo pueden aumentar la solubilidad lipíde un compuesto, reducir la disoci, aumentar la estabilidad y prolongar la duración de la acción del fármaco; Los grupos sulfhidrilo aumentan la solubilidad lipídica y facilitan la absorción del fármaco; Los enlaces amida pueden formar fácilmente enlaces de hidrógeno con macromoléculas biológicas y unirse a receptores, mostrando una especificidad estructural especial; Y la ruptura de un grupo hidroxilo para formar un enlace de hidrógeno aumenta la solubilidad en agua del compuesto, aumentando así la actividad del fármaco.

Basado en la estructura de los ginsenósidos, se especula que las reacciones de hidroxilación pueden ocurrir en las posiciones C-2, C-11, C-15, C-24, y C-30 pueden sufrir reacciones de hidroxilación; Los dobles enlaces carbono-carbono en las posiciones C-12 y C-13 pueden sufrir reacciones de adición y reacciones de oxid; Al mismo tiempo, los ginsenósidos de tipo diol pueden ser oxidados en las posiciones C-12 y C-24 para formar los ginsenósidos de tipo orictol. Por lo tanto, si las enzimas que pueden modificar la estructura de los ginsenósidos se pueden encontrar a través de la detección de diferentes microorganismos y enzimas, y algunos grupos pueden ser agregados o eliminados sobre la base de la estructura activa existente de los ginsenósidos raros, la actividad farmacológica y el objetivo de los ginsenósidos se puede mejorar, y la biodisponibilidad de los ginsenósidos se puede aumentar, proporcionando una nueva dirección para la modificación estructural de los ginsenósidos.
At the same time, with the continuous development of technology in the fields of food, medicine, the continuous development of technology in the fields of food, medicine, and biochemistry, researchers can use genetics, molecular cytology, and other interdisciplinary integration, as well as high-throughput screening and genomics technology to select or design enzymes or strains with high selectivity and conversion rates. Biological means can be used to achieve the industrial producciónof highly active rare ginseng saponins and their derivatives, further increasing the yield of rare ginseng saponins and their highly active derivatives. This is of great significance paramaking full use of ginseng resources for the benefit of the public.
Referencia:
[1] Jin Hee Kim,Miseon Kim, Sun-Mi Yun, etAl.El ginsenósido Rh2 induce apoptosis e inhila la transición epitelial-mesenquimal en células de cáncer de endometride HEC1A e Ishikawa [J]. Biomedicina & Farmacoterapia,2017,96. 871 — 876.
[2] Jiang Z, Yang Y, Yang Y, et al. El ginsenósido Rg3 atenúa la resistencia al cisplatino en el cáncer de pulmón al disminuir la regulación de la PD-L1 y reanudar el sistema inmunitario [J]. Biomed. Pharm. 2017.96.378-383.
[3] Yao W, Guan Y. Ginsenosides in Cáncer: A enfoque on the reglamento of célula Metabolismo. Biomed Farmacother. 2022 10 de octubre;156:113756. Doi: 10.1016/j.biopha.2022.113756.
[4] Yu H, Wang WangY, Liu C, et al. Conversión del ginsenósido Rb1 en seis tipos de ginsenósido altamente biobiorg3 y sus derivados por catálisis FeCl3. Chem Pharm Bull (Tokio). 2018;66(9):901-906.
[5] Zhang J,Ai Z, Hu Y, et al. Notable impacto de la esterilización comercial en la transformación de ginsenósidos en pulpa fresca de ginseng basada en análisis metabolómicos ampliamente dirigidos. Food Chem X. 2022 Aug 9;15:100415.
[6] Hasegawa, Hideo,Sung, et al. Principales metabolide saponde de Ginseng formados por bacterias intestinales. Planta médica, 1998, 62(5), 453-457.
[7] Hasegawa, Hideo, Sung, et al. Papel del Prevotella Oris Intestinal humano en la hidrolización del Ginseng Saponinas. Planta médica, 1997,63(5), 436-440.
[8]SHANGGUAN Lihua, LIU: Guoquan. Progreso de la investigación en el metabolismo de los componentes del ginseng [J]. China tradicional and Herbal Drugs, 1999(11):865-870.
[9] Lee Byung-Hoon, Lee, Sang-Jun Hui, et al. Actividad antigenotóxica In vitro de Novel Metabolide saponde Ginseng formados por bacterias intestinales. Planta médica, 1998, 64(6), 500 -503.
[10] Yoshimasa Yamaguchi, masnicaragua Higashi, Hideshi Kobayashi. efectos of ginsenosides on El deterioro rendimiento causado Byscopolamine in rats[J]. European Journal of Pharmacology, 1996, 312(2): 149-151.
[11] Kim WY, Kim JM, Han SB, et al. Al vapor de ginseng a alta temperatura aumenta la actividad biológica [J]. J Nat Prod, 2000, 63(12):1702-1704.
[12] Guo HY, Xing Y, Sun YQ, et al. Derivados de ginsengenina sintetiza partir de 20(R)-panaxotriol: síntesis, caracterización y actividad antitumoral dirigida a la vía HIF-1. J Ginseng Res. 2022 Nov;46(6):738-749.
[13] Kim GO, Kim N, Song GY, et al. Actividad inhibide la rara Ginsenoside Rg4 sobre la ligación cecy Sepsis inducida por punción. IntJ Mol Sci. 2022 16; 23(18):10836. Doi: 10.3390/ijms231810836.
[14] Chen Z, Wang G, Xie X, et al. El ginsenósido Rg5 interactúa alopéricon P2RY12 y mejora la trombovenosa profunda al contrarrestar la NETosis de neutrófilos y la respuesta inflam. Inmunol frontal. 2022 Aug 12;13:918476.
[15] Yannan. Preparación del ginsenósido Rg5 y su actividad contra el cáncer gástrico y de mama [D]. Shaanxi: universidad del noroeste, 2019.
[16] DENG J J, LIU Y, DUAN Z G, et al. El Protopanaxadioly las saponinas tipo protopanaxatriol mejoran el metabolismo de la glucosa y los lípidos en la diabetes mellitus tipo 2 en ratones inducidos por dieta alta en grasas/estreptozocina [J]. Front Pharmacol,2017, 8: 506.
[17] MAENG Y S, MAHARJAN S, KIM J H, et al. Rk1, un ginsenósido, es un nuevo bloqueador de la fuga vascular que actúa a través de la remodelde la estructura de actina [J], PLoSOne, 2013, 8(7) : e68659.
[18] RYOO N, RAHMAN MA, HWANG H, et al. El ginsenósido Rk1 es un nuevo inhibidor de los receptores NMDA en las neuronhipocampde cultivadas en ratas [J]. J Ginseng Res, 2020, 44 (3) :490-495.
[19] OH J M, LEE J, IM W T, et al. El ginsenósido Rk1 induce apoptosis en células de neuroblastoma a través de la pérdida del potencial de la membrana mitocondrial y la activación de caspasas [J]. Int J Mol Sci, 2019, 20(5) : 1213.
[20] SIDDIQI M H, SIDDIQI M Z, AHN S,et al. Efecto estimulante de los ginsenósirg5: Rk1 en las células osteoblasticMC3T3-E1 murina [J]. Phytother Res, 2014, 28(10) : 1447-1455.
[21] Krishika Sambyal, Rahul Vikram Singh. Aspectos de producción de testosterona por biotransformación microbiana y perspectivas de futuro [J]. Esteroides, 2020, 159(C).
[22]NAN bo,YOU ying,WANG yushan, et al.Research Progress on Microbial transformaciónof Ginsenosides[J]. Food Research And Development, 2017, 38(14): 196-199
[23]ZHOU Zhong-liu, LIChun-Yan,CHEN Lin-hao1, et al. Biotransformación de los Saponins[J]. Chinese Journal of Experimental Traditional Medical formulas, 2019, 25(16): 173-192.
[24] M. J. H, Eun-Ah BAE, Min-Kyung, et al. Metabolismo de 20(S)- y 20(R) -ginsenósido Rg3 por bacterias intestinales humanas y su relación con actividades biológicas in Vitro [J]. Biol. Pharm Bull, 2002, 25(1): 58-63.
[25] HAN Mingxin, LI Fangtong, ZHANG ZHANG yan, et al. biotransformación of Rare Protopanaxadiol Saponinby humana Microflora Intestinal [J]. Chemical Journal of Chinese Universities, 2019, 40(07): 1390-1396.
[26] ZHANG yan, LI fangtong, HAN mingxin, et al.Analysis of metaboliof Protopanaxatriol saponinasin Human Intestinal Flora by RRLC-Q-TOF MS and UPLC-QQQ MS[J]. Journal of Chinese Mass spectrosociety, 2020, 41(01): 66-75.
[27] TANG lan1, FU Lulu,, SHEN liting, et al.degradación de saponinas totales de Panax notoginseng por flora intestinal de ratas in vitro[J]. Chinese Traditional and Herbal Drugs, 2018, 49(02): 396-399.
[28] Guo Y P, Chen M Y, Shao L, et al. Cuantide metabolide saponinas de Panax notoginseng en plasma de rata con biotransformación mediada por microbioin vivo por HPLC-MS/MS[J]. Chinese Journal of Natural Medicines, 2019, 17(3): 231-240.
[29]CHEN sijian, WU dongxue, LIU suying, et al. Avances en la transformación química y biológica de ginsenoside[J] Chinese Traditional Patent Medicine,2022, 44(5): 1539-1545.
[30] WANG shanshan,HU ping,YU shaowen. Avances en la investigación de biotransformación de productos naturales [J]. Chinese Journal of New Drugs, 2016, 25(1): 71-75.
[31]GAO Juan, ZHOU Andong, YUAN ye, et al. Degradación enzimdel ginsenósido Rb1 para la preparación del compuesto K por Aspergillus niger sp. J7[J]. Current Biotechnology, 2016, 6(02): 98-104.
[32] Song X L, Wu H, Piao X C, et al. Transformación microbiana de ginsenósiextraído de raíces adventide Panax ginseng en un biorreactor de airlift [J]. Electronic Journal of Biotechnology, 2017, 26:20-26.
[33] Yan Q, Zhou W, Shi X L, et al. Vías de biotransformación del ginsenósido Rb1 a compuesto K by Paecilomyces Bainier sp. 229[J], Process Biochemistry, 2010, 45(9): 1550-1556.
[34] Hu Y B, Wang N, Yan X C, et al. Ginsenósido Re impactos en los productos de biotransformación de ginsenósido Rb1 por Cellulosimicrobium cellulans sp. 21 and ITS mechanisms[J], Process Biochemistry, 2019, 77: 57-62.
[35] Jitendra Upadhyaya, Min-Ji Kim, Young-Hoi Kim, et al. Formación enzimde compode k a partir de ginsenósido Rb1 por preparación enzimde micelios cultivados de Armillaria mellea[J]. Journal of Ginseng Research, 2016, 40(2): 105-112.
[36] Li Ling, Lee Soo Jin, Yuan Qiu Ping, et Al. Producción de bioactivos Ginsenósido Rg3(S) y compuesto K usando Lactococcus lactis recombin[J]. Journal of Ginseng Research, 2017, 42(4): 412-418.
[37] Hyojin Lee, Seung Il Ahn, Byung Wook Yang, et al. Biotransformación de ginsenósidos por bacterias de ácido lácderivadas de eoyukjang en Ginseng cultivado en montaña [J]. Microbiology and Biotechnology Letters, 2019, 47(2): 201-210.
[38] Liu C Y, Zuo K Z, Yu H S, et al. Preparación de ginsenósidos menores C-Mx y C-K de ginsenósidos de hoja de notoginseng por una ginsenosidasa especial tipo i [J]. Process Biochemistry, 2015, 50(12): 2158-2167.
[39] Zhang R, Huang X M, Yan H J, et al. Producción altamente selectiva del compuesto K del ginsenósido Rd hidrolizando glucosa en glucósido C-3 usando Bifidobacterium breve ATCC 15700[J]. Journal of Microbiology and Biotechnology, 2019, 29(3): 410-418.
[40] Almando Geraldi, Ni Matuzahrohabet, Fatimahab, al. enzimenzimenzim biotransformación of ginsenoside Rb1 by Glucosidasa recombinante de cepas bacterianas aisladas de Indonesia[J]. Biocatysis and Agricultural Biotechnology. 2020, 23(C): 101449-101449.
[41] Li L, Lee S J,Yuan Q P, et al. La producción de bioactivos ginsenósirg3 (S) Y compuesto K usando Lactococcus lactis recombinante [J]. Journal of Ginseng Research, 2017, 42(4): 412-418.
[42] Pei J J, Xie J C, Yin R, et al. Transformación enzimdel ginsenósido Rb1 a ginsenósido 20(S)-Rg3 por GH3 -glucosidasa de thermotomardsm 5069 T[J]. Journal of Molecular Catalysis B: enzim, 2015, 113:104-109.
[43] Zhang S H, Xie J C, ZhaoL G. clonación, sobreexpresión y caracterización de un termoestable Xilosidasa de Thermotoga Petrophila y la transformación cooperada del extracto de ginsenósido a ginsenósido 20(S)-Rg3 con a -glucosidasa [J]. Bioorganic Chemistry, 2019, 85:159-167.
[44]114-120. [LI Qi, TONG Xinyi, China Yujie, et al. construcción of todo cell Catalizador catalizador pelB-Xln-DT and its aplicación En biotransformación de Panax notoginsenoside R1[J]. Journal of Forestry Engineering, 2020, 5(04): 114-120.
[45] Min-Ji Kim, Jitendra Upadh ya ya, Min-SunYoon, et al. Biotransformación altamente regioselectiva del ginsenósido Rb2 en compuesto Y Y compuesto K by − -glicosidasa puride Armillaria mellea mycelia[J]. Journal of Ginseng Research. 2017, 42(4) : 504-511.
[46]ZHONG yating. Exámenes de exámenes de detección de Ginseng saponina transformación cepa GsBt3 and su Transformation Total Saponins De Panax Quinquefolium [D]. Shanghai: Shanghai Normal University, 2012.
[47] YANG yuanchao, WANG yingping, YAN meixia, et al. Selección de hongos fitopatógenos por producción de K compuesto ginsenósido [J]. China Journal of Chinese Materia Medica, 2011, 36(12): 1596-1598.
[48] CHEN yang,ZHANG mmeiping, WANG Yi, et al. Ginsenoside transformado microbiano Rg3 de saponinas totales de Panax ginseng por Bacillus subtilis [J]. Lishizhen Medicine and Materia Medica Research, 2014, 25(11):2676-2678.
[49] JIN yan, JIN xiangmei, YIN chengriBiotransformation of major ginsenoside Re to minor ginsenoside Rh1by Sphingomonas sp.2-F2[J]. Agricultural Science Journal of Yanbian University, 2011, 33(02): 103-107.
[50] LIANG zhiqi, ZHANG jinglou, JING haizhu, et al. Transformación microbimicrobide ginsenósido Rg3 en Rh2[J]. Ginseng Research, 2018, 30(03): 6-10.
[51] Yan Q, Zhou W, Shi X L, et al. Vías de biotransformación del ginsenósido Rb1 a compuesto K by Glucosidasas en el hongo Paecilomyces Bainier sp. 229[J]. Process Biochemistry, 2010, 45(9): 1550-1556.
[52] Ye L, Zhou C Q, Zhou W, et al. Biotransformación del ginsenósido Rb1 a ginsenósido Rd por Paecilomyces bainier 229-7[J] altamente tolerante al sustrato. Bioresource Technology, 2010, 101(20):7872-7876
[53] CHEN Xiaochun, DAI Zhu, FU rongzhao. Síntesis biocatalítica de raro ginsenósido Rh2[J]. Jiangxi Chemical Industry, 2019(02): 55-57.
[54] Su J H, Xu J H, Lu W Y, et al. Transformación enzimdel ginsenósido Rg3 a Rh2 usando el nuevo aislado de Fusarium proliferatum ECU2042[J]. Journal of Molecular Catalysis B, 2006, 38(2):113-118.
[55] Su J H, Xu J H, Yu H L, et al. Las propiedades de la novela -glucosidasede Fusarium proliferatum ECU2042 que convierte el ginsenósido Rg3 en Rh2[J]. Journal of Molecular Catalysis B, 2009, 57(1-4):278-283.
[56] WU Xiuli, WANG yan, ZHAO wenqian, et al. Biotransformación fúndel ginsenósido Rg3[J]. Acta Microbiologica Sinica, 2008(09): 1181-1185.
[57] CONG yueyi, SUN Jia, YU en, et al. Estudio sobre la transformación del ginsenósido Rg3 fermentpor Monascus purpureus[J]. Chinese Traditional and Herbal Drugs, 2018,49(06): 1298-1303.
[58] Jin F.X. En el II simposio internacional de medicina Natural y Microflora[M]. Tokio, Japón 1998, Oct, 24-26:1-15.
[59] Zhuang Y, Yang G Y, Chen X H, et al. Biosíntesis de la planta derivada de ginsenósido Rh2 en la levadura a través de la reutilización de una enzima microbiana promiscua clave [J]. Ingeniería metabólica, 2017, 42:25-32.
[60] Byeong-Min Jeon, Jong-In Baek,Min-Sung Kim, et al. Caracterización de un nuevo ginsenósido MT1 producido por una transramnosilación enzimde protopanaxatriol tipo ginsenósire [J]. Biomoléculas. 2020, 10(4): 525-525.
[61] Muhammad Zubair Siddiqi, hipóamaral Ximenes, Bong-Kyu Song, et al. Aumento de la producción de ginsenósido Rh2(S) a partir de ginsenósidos mayores tipo ppusando BglSk clonado de sacáribacikuerlensis junto con dos glicosidasa en serie [J]. Saudi Journal of Biological Sciences. 2021, 04, 079.
[62] Chen H, Dong, Zhi F, et al. Descubrimiento, síntesis y relaciones estructura-actividad de 20S-dammar-24-en-2 −, 3 −, 12 −,20-tetrol (GP) derivados como una nueva clase de AMPK − 2 − 1 − 1 activadores [J]. Bioorgánica y Química medicinal, 2016, 24(12): 2688-96.
[63] Xin S, Jl A, Yu X A, et al. Biotransformación altamente regioselectiva de ginsenósido Rg1 a derivados 25-OH de 20(S/R)-Rh1 por Cordyceps Sinensis-ScienceDirect[J]. Bioorgánica y Cartas de química Medicinal. 2020, 30(21): 127-504.
[64] Liu J S, Yu X N, Qiu Z D, et al.biotransformación de notoginsenósido R1 mediada por cordyceps sinensien 25-OH-20(S/R)-R2 con un efecto cardioprotector elevado contra la lesión celular indupor dox[J]. RSC Advances, 2022, 12, 129-38.
[65] Chen G T, Ge H J, Song Y, et al. Biotransformación de 20(S)-protopanaxatriol por Mucor racemosus y las actividades anticancerígenas de algunos productos [J]. Biotechnology Letters, 2015, 37(10): 2005-2009.
[66] Kim M Y, Cho J Y. 20s-dihidroprotopanaxadiol, un derivado del ginsenósido, aumenta las respuestas inmunitarias innde monocitos Y macrófagos [J]. Journal of Ginseng Research, 2013, Jul, 37(3): 293-9.
[67] akanaka M, Zhu P, Bo Z, et al. La infusión intravenosa de dihidroginsenoside Rb1 previene la lesión compresiva de la médula espinal y el daño cerebral isquémico a través de la regulación de VEGF y Bcl-XL.[J]. J Neurotrauma, 2007, 24(6): 1037-1054.
[68] Chen F, Zheng S L, Hu J N,et al. El éster octílico de ginsenósido Rh2 induce Apoptosis y detención del ciclo celular G1 en células humanas hepg2activando la vía apoptótica extrínseca y modulando la vía de señalización Akt/ P38 MAPK [J]. Journal of Agricultural &Food Chemistry, 2016, acs.jafc. 6b03519.
[69] Du G J, Dai Q, Williams S, et al. Síntesis de derivados del protopanaxadiol y evaluación de sus actividades contra el cáncer [J]. Medicamentos contra el cáncer, 2011, 22(1):35.
[70] Xu D, Tao L, Yan L, et al. 2-pirazina-ppd, un nuevo derivado del dammarano, mostró actividad anticancermediante especies reactivas de oxigenoapoptosis mediada y tensión del retículo endoplasmático en células de cáncer gástrico [J]. European Journal of Pharmacology, 2020, 881.
[71] Xu D, Yuan Y, Fan Z, et al. 4-XL-PPD, un nuevo derivado ginsenósido, como posibles agentes terapéuticos para el cáncer gástrico muestra actividad anticancerosa mediante la inducde la apoptosis celular generación medicada de especies reactivas de oxígeno e inhibide especies migratorias e invasi[J]. Biomedicina & Pharmacotherapy, 2019, (118): 108.
[72] Li Y, Baldauf S, Lim E K, et al. Análisis filogenético de la UDP-glucosiltransferasaMultigene Family of Arabidopsis thaliana[J]. Journal of Biological Chemistry, 2001, 276(6):4338.
[73] Christensen L P. Ginsenósidos: química, biosíntesis, análisis y efectos potenciales sobre la salud (capítulo 1)[J]. Adv Food Nutr Res, 2008, 55(55):1-99.
[74] Wang D D, Yeon-Ju Kim, Nam Baek, et al. Glycosyltransformation of ginsenoside (en inglés) Rh2 into dos Novela novela ginsenosides Utilizando glicosiltransferasa recombinde Lactobacillus rhamnosus y sus aplicaciones in vitro [J]. Journal of Ginseng Research. 2021 45(1): 48-57.
[75] Hu Y, Xue J, Min J, et al. Síntesis biocatalítica de ginsenósido Rh2 usando Arabidopsis thaliana glucosiltransferasa catalizada por reacciones acopladas [J]. Journal of Biotechnology, 2020, 309: 107-112.
[76] Jung S C, Kim W, Park S C, et al. Dos ginseng udp-glicosiltransferasas sintetizginsenósido Rg3 y Rd.[J]. Planta & Cell physiology, 2014, 55(12): 2177-88.
[77] jorolragchaa, Altanzul, Kim, et al. agrupación and Caracterización caracterización caracterización de glycosyltransferase genes from Panax Ginseng Meyer[J]. Gene, 536(1): 186-192.
[78] Warnecke D, Erdmann R, Fahl A, et al. Clonación y expresión funcional de genes UGT que codifican esterglucosiltransferasas de Saccharomyces cerevisiae, Candida albicans, pichiapastoris y Dictyostelium discoideum[J]. J Biol Chem, 1999, 274(19): 13048-13059. [79] Zhuang Y, Yang G Y, Chen X H, et al. Biosíntesis de planta de ginsenósido Rh2 en levadura a través de la reposición de una enzima microbiana promiscua clave [J]. Metab Eng, 2017, 42: 25-32.
[80] Zhao J N, Wang R F, Zhao S J, et al. Advance in Glicosiltransferasas, the important bioparts for production of Ginsenósidos diversificados [J]. Chinese Journal of Natural Medicines, 2020, 18(9): 643-658.
-
anterior
Natural Black Rice Extract Anthocyanins: Antioxidant Product Solutions
-
siguiente
Estudio en ginsenósido raro Rg1 Rb1 Rg3


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




