Estudio sobre Nanoginsenoside Preparion
El Ginseng. has an important place entraditional Chinese medicine, yits medicinal value was recorded as early as enShennong's clásico de Materia médica [1]. Los ginsenósidos son uno de los ingredientes farmacológicamente activos más importantes en el ginseng. Tienen diversos efectos farmacológicos, como la regulación del azúcar en la sangre [2], antitumoral [3], antiinflamatorio [4], neuroprotección [5], antifatiga [6], etc., pero debido a su pobre solubilidad en agua, baja biodisponibilidad y mala absorción, tienen ciertas deficiencias en su aplicación clínica [7]. En los últimos años, con el desarrollo de la tecnología de la nanomedicina, los ginsenósidos, como uno de los representantes de las medicinas naturales en el siglo 21, han atraído la atención de los investigadores en el desarrollo de sistemas de administración de nanomedicina relacionados con los ginsenósidos. Por lo tanto, el autor revisa la investigación actual sobre las nanomedicinas ginsenósidas, con la esperanza de proporcionar una referencia para el desarrollo de preparaciones relacionadas en el futuro.
1 introducción
1.1Ginseng saponins
Desde la década de 1960, los investigadores han aislado más de 100 tipos de saponginseng del ginseng. Sus estructuras químicas están compuestas principalmente por agliconas y sustituazúcares [8]. Las saponinas de Ginseng se pueden dividir en tipo de dammarano y tipo de oleanano de acuerdo con las diferencias en aglicones y azúcares. De acuerdo con la posición del grupo de azúcar, los ginsenósidos de tipo dammarano se pueden dividir en dos tipos: aquellos con el grupo de azúcar unido a las posiciones C-3 y C-20 del anillo de dammarano se conocen como tipo protopanaxadiol, y el tipo protopanaxatriol, en el que los grupos de azúcar se unen a las posiciones C-6 y C-20 del anillo de damarano. Las estructuras químicas de los distintos tipos de ginsenósidos se muestran en la figura 1 [9-11].
The ginsenosides that have been widely studied are mainly of the damarane type, such as ginsenosides CK,Rb1, Rg3, Rh2, Re, Rh1 yRg1, etc. The specific chemical structures are shown enTable 1 [11-12]. However, due to the poor membrane permeability of ginsenosides, the oral bioavailability is usually less than 5%, and the efficacy of direct application is not good [7]. Exploring suitable La drogaentregasistemasis an important means of enhancing their medicinal value.
1.2 sistemas de administración de nanomedicina
El desarrollo de la nanotecnología ha promovido el desarrollo de muchas nanomedicinas. Las nanomedicinas han sido ampliamente estudidebido a sus efectos farmacodinámicos únicos, tales como área de superficie específica grande, estabilidad fuerte, y carga alta del fármaco. Se ha encontrado que los sistemas de administración de nanomedicina pueden mejorar la eficacia de los fármacos al aumentar la solubilidad, mejorar la estabilidad de los fármacos, promover la absorción de fármacos, regular la liberación de fármacos y evitar el reconocimiento inmunológico [13-15]. La modificación dirigida de las nanomedicinas puede administrar medicamentos más precisamente a sitios patológicos [16-17], y la co-carga de múltiples fármacos con diferentes efectos farmacológicos puede mejorar el efecto terapéutico y reducir las reacciones adversas [18-19]. Además, las nanodrogas han sido ampliamente estudiadas para el tratamiento de tumores [20]. Muchos estudiosos han propuesto teorías de apoyo para la focalización tumoral de los nanofármacos, como el efecto EPR (Enhanced permeand retención effect), es decir, el tejido tumoral sólido tiene las propiedades de alta densidad vascular, integridad estructural pobre, trastornos de reflinfá, y altas concentraciones de medios de permevascular local, lo que facilita que las nanopartículas, liposomas y algunas sustancias macromoleculares entren y permanezcan en el tejido tumoral [21-22]. Preparación de ginsenósidos como una nano-formulación es una manera eficaz para mejorar su efecto terapéutico.
2 ginsenósidos como fármacos terapéuticos
2.1 mic
Las micelas son agregados ordenados de macromoléculas a nanoescala formadas por el autoensambde moléculas anfifílicas [23]. La parte hidrofóbica de la cadena molecular forma el núcleo de la micela, mientras que la parte hidrofílica forma la concha [24]. Las moléculas anfifílicas pueden ser utilizadas para encapsular fármacos poco solubles para mejorar la solubilidad del fármaco en agua, mejorar la estabilidad del fármaco, prolongar su tiempo de circulación en la sangre, alterar su distribución en los tejidos y 5 potenciar el efecto terapéutico [25].
Ginsenoside CK is the main metabolite of protopanaxadiol-type saponins and has a significant inhibitory effect on a variety of tumor cells [26]. However, CK has poor water solubility and low bioavailability, which limits its clinical application. Zhang etAl.[17] prepared a ginseng saponin CK polymer micelle APD-CK with deoxycholic acid-O-carboxymethylchitosan as the carrier modified with a liver cancer-specific targeting peptide A54.
La modificación del péptido A54 permite que la APD-CK se dirija de forma selectiva a las células cancerosas de hígado. El valor de IC50 de APD-CK después de 48 h de acción en células HepG2 es 16,32 μg·mL-1, que es mucho menor que el de CK libre (28,19 μg·mL-1). Además, la liberación de medicamentos en APD-CK es ph resistente, y es más fácil de liberar en condiciones ácidas. Esta micela también puede tener alguna habilidad de apuntar lisosoma. Además de la integración física, las drogas que enlazquímicamente a la portadora es también un medio común de preparar micelas cargadas de droga. Li etAl.[27] usaron ginsenósido Rh2 y triptólido para terminar la esterify PEG, preparcon éxito un polímero triblock "hidrofóbic-hidrofílic-hidrofóbico". Este polímero puede autoensamben en micelas y ser utilizado para la entrega de drogas hidrofóbic. Libera medicamentos bajo condiciones de pH bajo y la acción de las hidrolasas del suero sanguíneo, y puede usarse como un sistema de administración de fármacos combinado estable en el tratamiento del cáncer de pulmón.
2.2 liposomas
Liposomes are tiny double-layered vesicles composed of amphiphilic phospholipids. Cholesterol is embedded in the membrane to enhance stability. Hydrophobic drugs can be encapsulated inside the lipid bilayer, while hydrophilic drugs can be embedded in the hydrophilic layer of the lipid membrane [28]. Compared with polymericnanoparticles, they have fewer adverse reactions and are biocompatible. At present, the few FDA-approved nanoformulations are mainly Los liposomasparaintravenous injection [29-30].
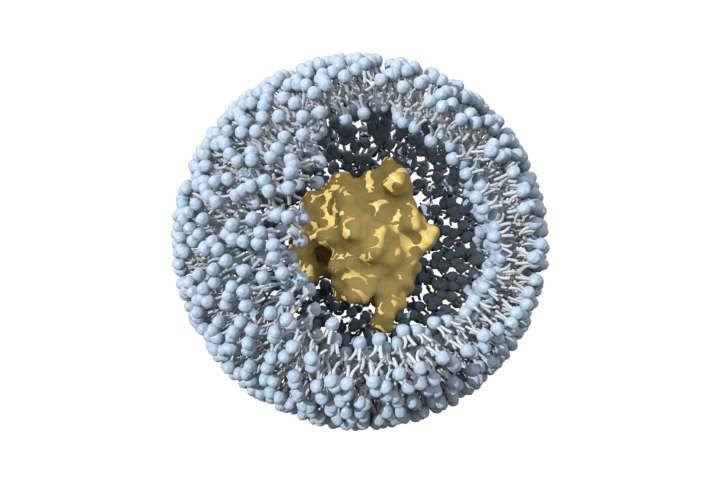
Ginsenoside Rh2 has a good Contra el cáncereffect in Vitro vitroand in vivo, but due to its hydrophobicity and significant efflux mediated by ABCtransporters, its bioavailability is very low [31]. Xu etAl.[32] prepared mPEG-PLA modified long circulating liposomes Rh2-PLPand and an octadecylamine-modified cationic liposome (Rh2-CLP). Compared with conventional liposome Rh2-LP,both have better physicochemical and biological properties in vitro and in vivo. PLP can targetdrug entregato tumor tissue. The fluorescence intensity of DiR-labeled PLP in mouse tumor tissue was 1.3 times that of CLP and 1.6 times that of LP. In vivo anti-tumor studies have shown that Rh2-PLP has the strongest tumor inhibitory effect. This property may be attributed to the PEG modification, which can shield the recognition of liposomes by the reticuloendothelial system (RES), prolong the circulation time of liposomes in the blood, and thus achieve passive targeting of tumors. In addition, other studies have found that the affinity of saponins paracholesterol and phospholipids can affect the structure and formation of liposomes. When the interaction between cholesterol and phospholipids is stronger than that between cholesterol and saponins, it is more conducive to the stability of liposomes [33-34].
2,3 nanoleche
Las nanoemulsiones son sistemas termodinámicamente estables compuestos por una fase de aceite, una fase de agua y un surfaco coemulsificador. Normalmente se requieren fuertes fuerzas mecánicas para disperel fármaco y excipientes uniformemente [35]. Sin embargo, el proceso de preparación requiere menos surfac, el tamaño de la gota es pequeño, y la absorción del fármaco puede ser aumentada [36]. Se ha estudiado para la liberación controlada de sustancias bioactivas cuando se administra por vía oral, por inyección, y por vía tópica en la piel [37-39].
Ginsenoside Rg1 has low membrane permeability and is not effective when taken orally [40]. In order to improve the oral bioavailability of Rg1, Khattab etAl.[41] used Caproyl 90, IPMand Labrafil M1944 as the oil phase, Tween 80, Cremophor EL and Tween 20 as the surfactants, Transcutol HP and propylene glycol as co-surfactants, prepared a Rg1-loaded nanoemulsion SNES. SNEShas an ultra-small particle size of 10.05–13.32 nm, which effectively avoids the phagocytosis of RES. The lipid components in the preparation enhance the ability of Rg1 to penetrate the blood-brain barrier, thereby providing higher brain targeting. After oral administration, the metabolites of the lipid components in SNES,such as diacylglycerides, monoglycerides and fatty acids, form mixed micwith bile acids, which promote the absorption of Rg1 into the blood circulation through the lymphatic system, thereby avoiding the first-pass effect. This nanomilky solution may be an alternative treatment for obese patients with orlistat metabolic disorders.

2,4 nanopartículas de albúmina
Albumin is abundant in serum and has the advantages of being non-toxic, non-immunogenic, biocompatible, and easily chemically modified. Based on these properties, albumin nanoparticles have been widely studied for the entregaof various types of molecules, including chemical drugs, proteins/peptides, and oligonucleotides [42-44].
Zhang etAl.[45] seleccionmpeg-sa para esterificar los grupos hidroxil libres en el ginsenósido Rg3 y preparó nanopartículas de albúmina mPEG-Rg3-BSA usando albúmina de suero bovino (BSA) como el portador. La introducción de mPEG hidrófilo puede prolongar significativamente la circulación sanguínea de la droga, que es propicio para el mPEG-Rg3-BSA NPs lograr el efecto EPR. La intensidad de fluorescde las NPs mPEG-Rg3-BSA marcadas con DiR en el sitio del tumor es 5,4 veces mayor que la de la DiR libre. En comparación con Rg3 libre, mPEG-Rg3-BSA NPs mejorar el efecto terapéutico. El ginsenósido Rg5 tiene baja solubilidad en agua y pobre biodisponibilidad. Dong et al. [46] usaron un método de dessolvatación para preparar nanopartículas de albúmina sérica bovina diana modificada de ácido fólico (FA) cargadas con Rg5 (FA-Rg5-BSA NPs). Estas nanopartículas se dirigen específicamente a las células tumorales debido a la gran cantidad de FA en la superficie, el aumento de la captación de nanopartículas y la internalización a través de la endocitosis mediada por el receptor, induciendo la apoptosis de las células tumorales. En un modelo de tratamiento de cáncer de mama humano MCF-7 en ratones, se observó que el Rg5 podía acumularse efectivamente en el sitio del tumor rápidamente (8 h), y la tasa de inhibición del peso tumoral en ratones alcanzó (79,25 ± 6,36 %) %, significativamente mayor que la de Rg5 libre (48,84 ± 9,74%) y Rg5-BSA NPs sin modificación de la FA (69,91 ± 11,77%).
Nanopartículas de 2,5 metales
Cuando las partículas de Metal metal metal metalse utilizan como portadores de fármacos, el fármaco puede ser cargado en la superficie del portador de metal a través de interacciones tales como fuerzas electrostáticas, enlaces de hidrógeno y fuerzas de van der Waals. En los últimos años, las nanopartículas metálicas han atraído mucha atención debido a su gran área de superficie específica, facilidad de modificación funcional, alta estabilidad y alta capacidad de carga del fármaco. Se han estudiado ampliamente en imaginología tumoral, terapia dirigida y terapia fototérmica [47-49].
Due to the good biocompatibility and automatic liver targeting function of iron-based nanoparticles, Ren et al. [50] prepared Fe@Fe3O4 nanoparticles Np Rg3 coupled with ginsenosideRg3Lo que puede inhibir significativamente el desarrollo de carcinoma hepatocelular (CHC), eliminar la metástasis pulmonar de CHC y prolongar eficazmente la supervivencia de ratones con cáncer de hígado. Las nanopartículas también pueden remodela la red desequilibrentre los microorganismos intestinales y el metabolismo, retraslos cambios microbiintestindupor el HCC durante al menos 12 semanas, proporcionando una nueva estrategia para el tratamiento del CHC. Además, la combinación de terapia fototérmica y quimioterapia es también un medio importante para el tratamiento del cáncer. Kim et al. [51] prepararon nanopartículas de CK-Au de ginsenósido usando Lactobacillus acidophilus DCY51T. Que tienen una carga catiónica en la superficie. Cuando llegan al tejido tumoral utilizando el efecto EPR,pueden unirse a la superficie aniónica de las células tumorales e invadir las células tumorales a través de endocitosis, promoviendo la lisis de las células tumorales. Cuando se combina con el tratamiento con luz infrarroja de 635 nm, el efecto inhibitsobre la proliferación de las células del cáncer gástrico humano se mejora aún más, y es un agente terapéutico sinérgico eficaz para la fototérmica y la quimioterapia.

3 Ginseng saponinas como portadores de drogas
3.1 Ginseng saponinsComo portador de drogas
La estructura química única de los ginsenósidos los hace valiosos como un nuevo tipo de portador de fármacos, la combinación de las funciones de un portador y un tratamiento.
(1) Los ginsenósidos tienen una estructura hidrofóbica de dammarano o oleanano y una fracción hidrofílica de glucosa [8], que puede formar nanopartículas autoensambl, micelas o actuar como surfacactivos en nanoemulsiones [19,52-54]. (2) las saponinas de Ginseng tienen una estructura de estery pueden reemplazar al colesterol como un nuevo tipo de estabilide membrana de liposomas. Tienen las características de buena estabilidad y fuerte orientación tumoral [55-56]. (3) las saponinas de Ginseng pueden interactuar con los fosfolípidos en las membranas celulares. Cuando se utilizan como portadores de fármacos, pueden generar brechas transitorias al entrar en contacto con las membranas celulares, aumentando la captación celular de fármacos, y la integridad de la membrana celular puede ser restaurada en un período de tiempo relativamente corto [53]. (4) el grupo glicosil en la estructura de los ginsenósidos es un sustrpara el transportador de glucosa 1 (GLUT1). La GLUT1 se expresa específicamente en algunas células tumorales, por lo que los ginsenósidos también tienen ciertas propiedades dirigidas al tumor [57-58]. (5) GLUT1 es también el principal transportador de la barrera hematoencefálica. Las saponinas de Ginseng que contienen grupos glicosilos también pueden cruzar la barrera hematoencefálica, y tienen cierto potencial para la administración dirigida de fármacos en el cerebro [56,59].
(2)
3.2 aplicación de ginsenósidos como portadores de fármacos
3.2.1 formación directa de nanopartículas autoensambladas
Based on the amphiphilic molecular Estructura de ginsenósidosPueden formar nanopartículas por sí mismas y recubrir otros fármacos como portadores. Dai et al. [52] usaron micelas automontadas de ginsenósido Rb1 para producir compuestos anticancerosos naturales de baja solubilidad (ácido betulínico, dihidroartemisinina e hidrocamptotecina). Las nanopartículas preparadas tenían una alta capacidad de carga del fármaco (20%-35%), fuerte foctumoral y prolongada semivida del fármaco. Li et al. [19] prepararon con éxito micelas de saponrb1 de ginseng microemulcargada con Diclofenac con un tamaño de partícula menor de 10 nm usando el método de dispersión de película delgada. Estudios de penetración corneal ocular In vivo en conejos mostraron que las micelas podían entregar altas concentraciones de diclofenaco a la córnea. Después de una dosis única, los niveles de diclofenaco en el grupo de administración de Rb1-Dic fueron 137,54%, 74,93% y 255,43% más altos que los del grupo de solución oftálmica de diclofenaco disponible comercialmente en los puntos de tiempo de 0,5, 1 y 2 h, respectivamente, proporcionando una nueva estrategia para el tratamiento de enfermedades inflamoculares. Zou et al. [53] usaron el extracto de saponde de ginseng como un material de membrana preparado con insulina cargada con ginsenosi(INS) y nanopartículas de ginsenósipor dispersión de película delgada, que puede proteger a las INS de ser destruidas por las hidrolasas de la piel. Las nanopartículas también pueden penetrar rápidamente en las células en 15 minutos mediante la destrucción reversible de la barrera lipíintercelular, y basado en la piel#39;s efecto reserv, la eficacia hipoglicémica de la formulación en un modelo del tratamiento diabético en rata se mantuvo en cerca del 50% del nivel inicial para 48 h.
3.2.2 estabilide membrana para liposomas
El ginsenósido tiene una estructura química similar al colesterol y se puede utilizar como estabilide membrana para los liposomas en lugar de colesterol. Hong et al. [55] prepararon liposomas que contienen paclitaxel usando ginsenoside Rh2 y fosfolípidos y confirmaron que el Rh2 tiene las excelentes propiedades de aumentar la estabilidad de los liposomas, prolongar el tiempo de circulación del fármaco en la sangre, promover la acumulación del fármaco en los tumores e invertir el microambiente inmunosupres. Chen et al. [58] además, encontraron que los ginsenósidos con un grupo de azúcar C-3 sustituido (como los ginsenósidos Rg3 y Rh2) pueden prolongar el tiempo de circulación sanguínea de los liposomas y unirse específicamente a GLUT1 expresado en la superficie de las células 4T1, aumentando la capacidad de dirigir el tumor. Los residuos de azúcar en la estructura ginsenósido son sustratos para el transportador de glucosa de la barrera hematoencefá. [59]. Zhu et al. [56] usaron el ginsenósido Rg3 como material de membrana para preparar los liposomas cargados con paclitaxel Rg3-PTX-LPs, que también pueden cruzar la barrera hematoencefálica para el tratamiento dirigido de los tumores cerebrales. La IC 50 de Rg3-PTX-LPs para células de glioma C6 de rata es 0.045 μg·mL-1, que es mucho más baja que la de los liposomas de colesterol C-PTX-LPs (0.149 μg·mL-1). Las imágenes de fluorescencia In vivo mostraron que la intensidad de la señal DiR detectada en la región de glioma de Rg3-LPs era cerca de 3 veces la de C-LPs, y se detectó que la eliminación de Rg3-LPs en ratones era más lenta que la de C-LPs, e incluso cerca de PEG-C-LPs. Este tipo de liposoma también tiene un cierto efecto de circulación prolongada.
3.2.3 surfaccomo nanomulsión
Los ginsenósidos son también un surfacnatural [60] porque su estructura química contiene tanto grupos hidrofóbicos como hidrófilos. Actualmente se están estudiando para su uso en el diseño y desarrollo de nuevos alimentos funcionales. Shu et al.[54] disperastaxantina en aceite de soja como la fase de aceite y ginsenosidos en agua de alta pureza como la fase acuosa. Prepararon con éxito nanoemulque contienen astaxantina por homogeneia alta presión. Incluso a un nivel relativamente bajo, el ginsenósido puede reducir eficazmente la tensión interfacial entre las interfaces de aceite y agua. Dentro de un cierto rango de concentración, a medida que la concentración de ginsenósido aumenta, el tamaño de la gota se hace más y más pequeño. Sin embargo, vale la pena señalar que cuando esta emulsión nanolechosa se almacena a temperaturas más altas, la tasa de degradación de astaxantina es demasiado rápida, y el impacto específico de ginsenosida como surfacen la estabilidad de la emulsión debe ser estudiado más a profundidad.
4 conclusión y perspectivas
Los ginsenósidos tienen una variedad de actividades farmacológicas y son medicamentos naturales con gran potencial de desarrollo. Sin embargo, son altamente hidrofóbicy tienen baja biodisponibilidad oral, lo que limita su aplicación clínica. El desarrollo de formas nanofarmacéuticas proporciona un medio de aplicación práctica para muchos fármacos poco solubles. Los ginsenósidos pueden ser encapsulados directamente en nanoportadores como micelas, liposomas, nanoleches, nanopartículas de albúmina y nanopartículas de metal, y su biodisponibilidad puede ser mejorada de manera efectiva. Además, el grupo de azúcar hidrofílico en la estructura hidrofóbica del ginsenósido le da ciertas propiedades surfac, y puede ser utilizado para formar nanopartículas o actuar como un surfacpara nanoemulsiones. Además, el ginsenósido tiene una estructura similar al colesterol, y también se puede utilizar como un estabilide membrana para los liposomas para mejorar su estabilidad. En general, preparar los ginsenósidos como una nanoformulación puede mejorar su biodisponibilidad. Los ginsenósidos también se pueden utilizar como un material portador para mejorar las propiedades de la nano-formulación. Cuando se utiliza para encapsular otros fármacos, también puede lograr un efecto terapéutico sinérgico, y tiene un gran valor de desarrollo y potencial de aplicación. Sin embargo, en esta etapa, la investigación sobre los ginsenósidos como un portador de fármacos está todavía en su infancia, y el desarrollo de formulrelacionadas requiere más investigación.

Referencias:
[1] Sun Xingyan, Sun Fengyi, comp. Shennong's clásico de Materia médica [M]. Beijing: The Commercial Press, 1955: 9.
[2] SABA, E KIM KIM KIMS H,KIM S D, et al. Alivio de las complicaciones diabéticas por ginsenoside rg3 enriquecido con extracto de ginseng rojo en ratones LDL - / - alimentados con dieta occidental [J]. JGinseng Res, 2018,42(3): 352-355.
[3] ROSA M T M G, SILVA E K, SANTOS D T, et al. Obtención de miniemulsiones de aceite de semilla de achipor ultrasonización utilizando extracto acuoso de raíces de ginseng brasileño como biosurfac[J]. JFood Eng, 2016,168: 382-390.
[4] Qi B, Zhang S, Guo D, et al. Efecto protector y mecanismo del ginsenósido Rg1 sobre el tetracloruro de carbono inducido por lesión hepática aguda [J]. Mol Med Rep, 2017, 16(3): 2814-2822.
[5] WANG R, LI Y N, WANG G J,et al. Efectos neuroprotectores y transporte cerebral de ginsenósido Rg1[J]. Chin J Nat Medicines, 2009,7(4): 315-320.
[6] YANG Q Y,LAI X D, JING O Y, et al. Efectos de ginsenoside Rg3 sobre la resistencia a la fatiga y SIRT1 en ratas envejecidas [J]. Toxicology, 2018,409: 144-151.
[7] KIM H, LEE J H, KIM J E, et Al. Micro-/nano-size delivery sistemas De ginsenósidos Para mejorar Biodisponibilidad sistémica [J]. J Ginseng Res, 2018,42(3): 361-369.
[8] CHEN W, BALAN P,POPOVICH D G. capítulo 6 - comparación de la composición ginsenósidel ginseng asiático (Panax ginseng) y ginseng americano (Panax quinquefolius L.) y sus vías de transformación [J]. Stud Nat Prod Chem, 2019,63: 161-195.
[9] MOHANAN P,SUBRAMANIYAM S, MATHIYALAGAN R, et al. Señalización Molecularde los ginsenósidos Rb1, Rg1 y Rg3 y su modo de acción [J]. J Ginseng Res, 2018,42(2): 123-132.
[10] XU X H, LI T, FONG CM V, et al. Saponinas de medicinas chinas como agentes anticancerosos [J]. Moléculas, 2016,21(10): 1326.
[11] WANG H, ZHENG Y, SUN Q, et al. Los ginsenósidos emergen como fármacos bifuncionales y nanoportadores para terapias antitumorales mejor[J]. J Nanobiotechnol, 2021,19(1): 322.
[12] PIAO X M, ZHANG H, KANG J P, et al. Avances en la diversidad de saponina de Panax ginseng[J]. Moléculas, 2020,25(15): 3452.
[13] BISWAS S, KUMARI P, LAKHANI P M, et al. reciente Avances avances in polymeric micelles for anti-cancer Administración de drogas [J]. Eur J Pharm Sci, 2016,83: 184-202.
[14] SHISHIR M R I, XIE L H, SUN C D, et al. Avances en micro y nanoencapsulación de compuestos bioactivos utilizando biopolímeros y transportadores basados en lípidos [J]. Food Sci Tech, 2018,78: 34-60.
[15] DEY T K, KOLEY H, GHOSH M, et al. Efectos de la nanosización sobre la bioaccesibilidad lipíy la biodisponibilidad ex vivo de aceite rico en EPA-DHA en nanoemulsión de agua [J]. Food Chemistry, 2018,275: 135-142.
[16] HOON H, HO P M, GAYOUNG J, et al. Hidrogel inyectable de glicol quitosán que contiene ácido fólico complejo de ciclodextrina-paclitaxel funcionalizado para el tratamiento del cáncer de mama [J]. Nanomateriales, 2021,11(2): 317.
[17] ZHANG J M, JIANG YY, LI YP. Micelas modificadas con el péptido homing derivado de achitosan para la entrega intracdirigida del compuesto ginsenósido K a las células cancerosas del hígado [J]. Carbohydr Polym, 2020,230: 115576.
[18] SUN J J, LIU Y H, CHEN Y C, et al. Doxorrubicina administrada por un profármaco polipolique contiene dasatinique responde a redox para tratamiento combinado [J]. J Controlled Release, 2017,258: 43-55.
[19] LI M S, LAN J, LI X F,et al. Nuevas micelas ultra-pequeñas basadas en el ginsenósido Rb1: una nanoplataforma potencial para la administración de fármacos oculares [J]. Drug Delivery, 2019,26(1): 481-489.
[20] GABIZON A A, ROSALES R T M D, LA-BECK N M. Translational considerations in nanomedicine: the Oncology perspective[J]. Adv Drug Deliver Rev, 2020,158: 140-157.
[21] GOLOMBEK S K, MAY J N, THEEK B, et al. Tumor targeting vía EPR: estrategias para mejorar las respuestas de los pacientes [J]. Adv Drug Deliver Rev, 2018,130: 17-38.
[22] PARK J, CHOI Y, CHANGH, et al. Alianza con el efecto EPR: estrategias combinadas para mejorar el efecto de EPR en el microambiente tumoral [J]. Theranostics, 2019,9(26): 8073-8090.
[23] DESHMUKH A S, CHAUHAN P N, NOOLVI M N, et al. Micelas poliméricas: investigación básica para la práctica clínica [J]. Int J Pharm, 2017,532(1): 249-268.
[24] JHAVERI A M, TORCHILIN V P. micelas polimérimultifuncionales para la administración de fármacos y SiRNA [J]. Front Pharmacol, 2014,5: 77.
[25] AHMAD Z, SHAH A, SIDDIQ M, et al. Micelas poliméricas como vehículos de liberación de fármacos [J]. RSC Advances, 2014,4(33): 17028-17038.
[26] SHARMA A, LEEH J. Ginsenoside Compound K: insights into recent studies on pharmacokinetics and Health - promoting activities[J]. Biomoléculas, 2020,10(7): 1028.
[27] LI P, ZHOU X Y, QU D, et al. Estudio preliminar sobre la fabricación, caracterización y efectos sinérgicos anticáncer de pulmón de micelas autoensamblde celastrol polietilenglicol ginsenósido covalconjugrh2 [J]. Drug Delivery, 2017,24(1): 834-845.
[28] DIANA G, ARTUR C P, EUGENIAN. Diseño de liposomas como sistema de administración de fármacos para aplicaciones terapéu[J]. Int J Pharm, 2021,601: 120571.
[29] DE L V, MILANO F, AGOSTIANOA, et al. Avances recientes en el ensamblaje de polímeros/liposomas para la administración de fármacos: desde modificaciones superficiales hasta vesículas híbri[J]. Polímeros, 2021,13(7): 1027.
[30] ALMEIDA B, NAG O K, ROGERS K E, et al. Avances recientes en estrategias de bioconjugación para la administración de fármacos mediada por liposomas [J]. Moléculas, 2020,25(23): 5672.
[31] GU Y, WANG G J, WU X L, et al. Mecanismos de absorción Intestinal del ginsenósido Rh2:estereoselectividad e implicación de los transportadores ABC [J]. Xenobiotica, 2010,40(9): 602-612.
[32] XU L Q, YU H, YIN S P, et al. A base de liposomas delivery systems for ginsenoside Rh2: in vitro and in Comparaciones de vivo [J]. J Nanopart Res, 2015,17(10): 415.
[33] HAO F, HEY X, SUNY T, et al. Mejora de la disponibilidad oral de saponinas de la fruta de ginseng mediante un sistema de administración prolífico que contiene desoxicolato de sodio [J]. Saudi J Biol Sci, 2016,23(1): S113-S125.
[34] GROOT C D, MUSKEN M, müller-goymann C C. el triterpenbidesmosídico saponinshederacoside C y el ginsenósido Rb1 exhibaja afinidad al colesterol en las membranas liposómicas [J]. J drogas drogas Sci Tec, 2019,53: 101127.
[35] ANTON N, VANDAMME T F. Nano-emulsions and micro-emulsions: clarifications of the critical differences[J]. Pharm Res, 2011,28(5): 978-985.
[36] MCCLEMENTS D J. avances en nanoemulsiones comestibles: digestión, biodisponibilidad, y toxicidad potencial [J]. Prog Lipid Res, 2021,81: 101081.
[37] MASKARE R G, INDURWADE N H, DESHMUKH RA, et al. Nanoemulsiones: aumento de las posibilidades de administración de fármacos por vía oral [J]. Asian J Chem Tec, 2021,11(1): 53-58.
[38] SEGUY L, GROO A C, GOUX D, et al. Diseño de nanoemulsiones no hemolípara administración intravenosa de APIs hidrofóbic[J]. Pharmaceutics, 2020,12(12): 1141.
[39] BASHIR M, AHMAD J, ASIF M, et al. Nanoemulgel, un portador innovador para la administración tópica de diflunisal con profundo efecto antiinflamatorio: evaluación in vitro e in vivo [J]. Int J Nanomed, 2021,16: 1457-1472.
[40] HE C Y, FENG R, SUN Y P, et al. Cuantisimultánea de ginsenósido Rg1 y sus metabolipor HPLC - MS/MS: excreción de Rg1 en la bilide de rata, orina y heces [J]. Acta Pharm Sin B, 2016,6(6): 593 -599.
[41] KHATTAB A, AHMED-FARID O A, NASR S A. Enhanced brain biodistribution of Ginsenoside Rg1 based (en inglés) Autonanoemulsificante sistema de administración de fármacos para mejorar los síndromes metabólicos y mantener el equilibrio homeost[J]. J Drug Deliv Sci Tec, 2021,61: 1002276.
[42] YHEE J Y, LEE J, CHANG H, et al. Molecular Imágenes por imágenes and targeted drug delivery usando Nanopartículas a base de albúmina [J]. Curr Pharm Design, 2015,21(14):1889-1898.
[43] LIU Z B, CHEN X Y. la química bioconjugsimple sirve a grandes avances clínicos: la albúmina como una plataforma versátil para el diagnóstico y la terapia de precisión [J]. Chem Soc Rev, 2016,45(5):1432-1456.
[44] JAIN A, SINGH S K, ARYA S K, et al. Nanopartículas de proteínas: plataformas prometedoras para aplicaciones de administración de fármacos [J]. ACS Biomater Sci Eng, 2018,4(12):3939-3961.
[45] ZHANG L J, HUI J F, MA P, et al. PEGylation of ginsenoside rg3 entrapped beef serum albúmina nanopartículas: preparación, caracterización, y estudios biológicos in vitro [J]. J Nanomater, 2019: 3959037.
[46] DONG YN, FU R Z, YANG J, et al. Nanopartículas de albúmina de suero bovino cargadas con ácido fólico modificado con ácido fólico para terapia dirigida contra el cáncer in vitro e in vivo[J]. Int J Nanomed, 2019,14: 6971-6988.
[47] RAI M, INGLE A P, GUPTA I, et al. Bioactividad de nanopartículas de metales nobles decoradas con biopolímeros y su aplicación en la administración de fármacos [J]. Int J Pharm, 2015,496(2): 159-172.
[48] GOKUL P, Namibia K, ARUL M R, et al. anisotrópico Noble noble metal Nanopartículas: Síntesis, Funcionalización de superficies y aplicaciones en biosensores, bioimágenes, administración de fármacos y teranosticos [J]. Acta Biomater, 2017, 49: 45-65.
[49] NOOR NA R, BASMA AA, NATHEER H A R, et al. Magnetism in Drug delivery: the Marvels of Iron oxide and ferrites nanopartículas [J] (en inglés). Saudi Pharm J, 2020,28(7): 876-887.
[50] REN Z G, CHEN X M, HONG L J, et al. La conjugde nanopartículas de ginsenósido Rg3 inhiel desarrollo de carcinoma hepatocelular y metástasis [J]. Small, 2020,16(2): e1905233.
[51] KIM YJ, PERUMALSAMY H, MARKUS J, et al. Desarrollo de nanopartículas de oro mediadas por Lactobacillus kimchicus dcy51t para la entrega del compuesto ginsenósido K: efectos fototérmicos in vitro y detección de apoptosis en células cancerosas [J]. Artif Cell, Nanomed, Biotechnol, 2019,47(1): 30-44.
[52] DAI L, LIU K F, SI C L, et al. Ginsenoside nanopartícula: un nuevo sistema de administración de fármacos verdes [J]. J Mater Chem B, 2015,4(3): 529-538.
[53] ZOU J J, LE J Q, ZHANG B C, et al. Acelerar la entrega transdérmica de insulina por nanopartículas de ginsenósido con permeúnica [J]. Int J Pharm, 2021,605: 120784.
[54] SHU G F, KHALID N, CHEN Z, et al. Formulación y caracterización de nanoemulde enriqucon astaxantina estabilizadas usando saponde ginseng como emulsificantes naturales [J]. Food Chem, 2018,255: 67 — 74.
[55] HONG C, LIANG J M, XIA J X, et al. One Stone Four Birds: a novel liposomal delivery system multi-functionalized with ginsenoside Rh2 for tumor targeting therapy[J] (en inglés). Nano-Micro Lett, 2020,12(10): 73-90.
[56] ZHU Y, LIANG J M, GAO C F, et al. multifuncional Ginsenoside rg3 basado en liposomes Para la terapia dirigida a glioma [J]. J Controlled Release, 2020,330: 641-657.
[57] RAMANI P, HEADFORD A, MAY M T. la expresión de la proteína GLUT1 se correlaciona con la categoría histológica desfavorable y el riesgo alto en pacientes con tumores neuroblásticos [J]. Virchows Arch, 2013,462: 203 -209.
[58] CHEN C, XIA J X, REN H W, et al. Efecto de la estructura de los ginsenósidos sobre el destino in vivo de sus liposomas [J]. Asia J Pharm Sci, 2022, 2022,17(2): 219-229.
[59] WANG Y Z, XU Q, WU W, et al. Perfiles de transporte cerebral de ginsenósido Rb1 por transportador de glucosa 1: In vitro e in vivo[J]. Front Pharmacol, 2018,9: 398.
[60] ROSA M T M G, SILVA E K, SANTOS D T, et al. Obtención de miniemulsiones de aceite de semilla de achipor ultrasonización utilizando extracto acuoso de raíces de ginseng brasileño como biosurfac[J]. J Food Eng, 2016,168: 68 -78.
-
anterior
Estudio sobre la síntesis de ginsenósido
-
siguiente
Extracto de Ginseng Ginsenoside y la regulación inmune


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés





