Estudio sobre la tecnología de preparación del ingrediente activo del extracto de Centella Asiatica
Centella asiatica (L.) Urban. is the dried whole herb of the plant Centella asiatica (L.) Urban. in the family Apiaceae. Its active ingredients are mainly triterpene saponins and their derivatives [1], such as asiaticoside, madecassoside and madecassic acid, of which asiaticoside has the highest content. Asiaticoside has various pharmacological effects, such as promoting wound healing, treating scars, inhibiting breast hyperplasia, anti-tumor, anti-depression, and treating Alzheimer&#Enfermedad de 39;s [2]. Las actividades farmacológicas del ácido asiático y la madecassoside son similares a las del asiaticoside, mientras que la madecassoside también tiene el efecto de proteger los sistemas cardiovascular y cerebrovascular [3]. Con el fin de aplicar mejor los principios activos de Centella asiatica en la práctica clínica, investigadores nacionales y extranjeros han preparado diversos preparados seguros, estables y eficaces para sus diversas actividades farmacológicas. Este documento resume la investigación de preparación, resume las tecnologías clave en el proceso de preparación y las características de los preparados obtenidos, y analiza y resume la eficacia correspondiente.

1 inyección
El extracto titulado de la inyección de Centella asiática (TECA) se puede usar para tratar la esclerosis sistémica. Sin embargo, en una solución acuosa común, la solubilidad de TECA es baja, y debido aque el componente principal es una saponpentriterpen, la inyección directa puede causar hemólisis y una fuerte sensación dolorosa. Para resolver los problemas anteriores, Chong-Kook et al. prepararon una nueva inyección de TECA mediante la adición de Tween-20 y Tween-85 a la solución para mejorar la solubilidad de asiaticoside y reducir sus efectos secundarios tóxicos [4]. Los estudios han demostrado que cuanto mayor es la proporción de Tween-20 en el surfac, mayor es la solubilidad de TECA, hasta 18 mg/ml. Cuando la proporción de Tween-20 a Tween-85 es 6:4, el tamaño de partícula de la fase dispersa en la emulsión preparada es el más pequeño. En comparación con la inyección ordinaria de TECA propilglicol, después de que la inyección se administró a ratones mediante inyección intramuscular, el número de torcetas de los ratones se redujo significativamente, lo que indica que la inyección produjo menos dolor, lo que es beneficioso para aumentar la conformidad del paciente y es más adecuado para la aplicación clínica.
2 preparaciones orales
2.1 comprimidos
2.1.1 comprimidos de liberación prolongada
Con el fin de resolver los problemas de la existenteCentella asiatica tablets (en inglés)Como la gran dosis por porción y el gran número de dosis diarias, Gan Kelin y otros aumentaron la dosis en 3 veces sobre la base de las tabletas disponibles comercialmente de Centella asiatica, y añadihidroxipropimetilcelul(HPMC) como un material de liberación sostenida para preparar las tabletas de liberación sostenida de glucósido total de Centella asiatica [5]. Usando 20% K100M HPMC como portador de liberación sostenida y añadiendo 10% solución de etanol de celulde etilo como agente de adhesión, se prepararon tabletas de liberación sostenida, cada una con un peso de aproximadamente 1,5 g y conteniendo 18 mg de glucósido total de Centella asiatica. Los resultados del estudio de liberación in vitro mostraron que las tabletas normales de Centella asiatica total saponins habían básicamente completamente desintegrado y liberado todo el fármaco después de aproximadamente 1 hora, mientras que las tabletas de liberación sostenida de Centella asiatica total saponins podrían liberar efectivamente el fármaco durante 12 horas, logrando el propósito de liberación lenta y controlada. Zheng Xiaochun et al. usaron K15M hidroxipropil metilcelulcomo un portador de liberación sostenida, celulmicrocristalina como un regulador de liberación, y una solución de etanol povidona como un aglutinpara también producir una tableta de liberación sostenida total de glucósido de Centella asiatica que puede liberar efectivamente el fármaco durante un máximo de 12 horas [6].
2.1.2 comprimidos de desintegración Oral
Con el fin de resolver el problema de las dificultades de deglución de algunos pacientes, Song Xuyin et al. prepararon tabletas desintegrantes orales de asiaticoside [7]. Mediante la adición de celulmicrocristalina, carboximetilcelulde sodio reticuly manitol, y el uso de un diseño de prueba ortogonal para optimizar la prescripción, los comprimidos finales de desintegración oral pueden desintegrarse completamente en 1 min. Al mismo tiempo, el proceso de tableting es sencillo y fácil de llevar a cabo, lo que facilita la producción industrial.

2.1.3 comprimidos flotantes gástricos
Estudios han demostrado que asiaticoside tiene un buen efecto terapéutico sobre las úlceras gástri[8]. Con base en esto, Shi et al. prepararon tabletas flotantes de estómago asiático que pueden permanecer en el estómago y prolongar el tiempo de administración del fármaco [9]. Mediante el uso de carboximetil sódico almidón como ayuda para el blanqueamiento, polietilenglicol 20 000 como un pore-formador, y un método de diseño de mezcla para optimizar la prescripción, Centella asiatica total glucoside tabletas flotantes que pueden flotar efectivamente hasta 12 horas fueron finalmente obtenidos. Tableting tiene un impacto significativo en la apariencia, el rendimiento flotante y el rendimiento de liberación de fármacos de la tableta. El aumento de la presión puede prolongar el tiempo de flotación, ralentizar la tasa de liberación del fármaco y reducir la cantidad de fármaco liberado.
2.2 suspensión
Centella asiatica total glucoside has poor solubility in water, so it is often prepared as a suspension for oral administration. Literature shows that when used as a suspending agent with hydroxypropyl methylcellulose, it is administered to mice by gavage (30 mg/kg), and the degree of anxiety in mice is reduced in the elevated plus-maze experiment, the black box experiment, and the open field experiment. The anxiolytic effect of the drug becomes more pronounced with increasing dose [10]. At the same time, the preparation had a certain effect on the body weight of mice and the adrenaline content in the serum, but when the same dose of asiaticoside (10 mg/kg) or madecassoside (16 mg/kg) was used alone, there was no significant effect, indicating that the two may have a synergistic effect when used together, but it is also possible that the single use of a component is not sufficient in terms of dosage to produce an effect.

3 preparados tópicos
3.1 geles
Xia et al. utilizaron la tasa de absorción transdérmica y la penetración acumulativa como indicadores para mejorar la absorción transdérmica de asiaticoside mediante la adición de lauricina y geraniol a la prescripción en diferentes concentraciones [11]. Los resultados mostraron que la permeación acumulada y la tasa de absorción transdérmica podrían incrementarse de 3 a 12 veces después de agregar un potenciador de perme, y el efecto fue mejor cuando se usó 1% de laurazona sola. Wang Shuping et al. también utilizaron borneol, mentol, etc como potencide la permepara mejorar la absorción transdérmica de asiaticoside [12].
Los surfacno sólo pueden usarse para aumentar la solubilidad de sustancias poco solubles, sino también para promover la absorción transdérmica de sustancias poco solubles. Soon-Sun et al. investigaron el efecto solubilizante de una serie de surfacno oniónicos y aniónicos en TECA, y seleccionel éster caprílico de poliglicerol cácrrico y desoxicolato de sodio como solubilizadores para preparar geles TECA [13]. Una gran cantidad de cristales aparecieron en el gel preparado con PEG polioxietileno glicercaprilato y caprato después de 24 horas, mientras que no aparecieron cristales obvien el gel preparado con desoxicolato de sodio después de un mes, lo que indica que la adición de desoxicolde de sodio tiene un efecto más estable en la mejora de la solubilidad de asiaticoside. Los experimentos con animales han demostrado que en comparación con el gel blanco, la tasa de curación de las heridas de ratones es significativamente más rápida y la eficacia es notable después de usar el gel de desoxicolato sódico TECA.
Emulsiones 3.2
Laugel et al. prepararon una emulsión compuesta de agua en aceite con asiaticoside, madecassoside y ácido asiático (en una relación de masa de 4:3:3) como el fármaco principal [14]. Los experimentos reológicos mostraron que la emulsión compuesta preparada era estable, y que la presencia del fármaco casi no tenía efecto sobre la estabilidad de la emulsión en comparación con la emulen blanco. Los experimentos transdérmicos In vitro mostraron que en comparación con las emulsiones ordinde aceite en agua, las emulsiones complejas tenían una tasa de retención en la epidery la dermis que era tres veces y dos veces más alta, respectivamente. Cuando se añade dimeticona a la fase exterior del aceite, también puede mejorar la tasa de absorción del fármaco y producir un cierto efecto de liberación sostenida [15]. Al mismo tiempo, la dimeticona con un menor peso molecular puede mejorar la solubilidad del fármaco en el estrato córneo, haciendo que los fármacos triterpenoides tengan más probabilidades de penetrar en el estrato córneo y llegar a la epidermis, y aumentando la cantidad de fármaco retenido en el estrato córneo. Sin embargo, la dimeticona con un mayor peso molecular tendrá el efecto opuesto.

3.3 agente de recubrimiento
Las preparaciones tópicas existentes de asiaticoside son principalmente preparaciones de crema, que tienen una estabilidad pobre, una sensación grasa, y son propensas a manchar la ropa. Con el fin de superar estos problemas, Jiang Ping et al. utilizaron una solución acuosa de quitosano como base, complementcon alcanfor, borneol y mentol, para preparar un agente de recubrimiento asiaticoside fácil de usar [16]. El contenido de asiaticoside y madecassoside en el agente de recubrimiento de película fue del 95% al 105% de la cantidad etiquetada, lo que indica que el agente de recubrimiento de película preparado tenía un contenido estable de fármaco.
Agente de la membrana 3.4
Xin Tian et al. usaron quitosano deacetilcomo material formador de película para preparar un 6% de agente de película asiaticoside. El fármaco fue distribuido uniformemente en el agente film, y el rendimiento de liberación in vitro fue bueno, con 90% del fármaco liberado después de 14 h [17]. La película preparada se utilizó para tratar trauma uterino en conejos. En comparación con el grupo control, el trauma uterino se curó significativamente después del tratamiento con la película de Centella asiática y no hubo adherencia a la pared intestinal.
Panprung et al. used sodium alginate, a natural polysaccharide, as a raw material and prepared the centella asiatica film-forming agent by forming calcium alginate salt through complexation with Ca2+ as the matrix of the film-forming agent based on the traditional preparation method [18]. In this study, a high concentration of CaCl2 solution was used to carry out a secondary cross-linking reaction on the initially prepared film-forming agent to improve the stability of the film-forming agent. Mechanical property studies showed that the addition of asiaticoside could make the membrane withstand greater tensile stress, but it would make the membrane less flexible. In PBS containing 10% methanol, the membrane could effectively release the drug for up to 24 hours, and the cumulative release rate of asiaticoside could reach 92%. At the same time, toxicological studies showed that the membrane had no significant toxicity to fibroblasts in human dermis.
En contraste con el proceso de preparación anterior, el proceso de preparar directamente un agente de película de alginato de sodio, secándolo, y luego sumergiéndolo en una solución de CaCl2 que contiene etanol de diferentes concentraciones para reticulpara obtener un agente de película asiaticoside es más simple. En comparación con una solución CaCl2 pura, la adición del disolvente etanol latente puede reducir la velocidad de reticul, resultando en una película con una apariencia más transparente y un espesor reducido. Observado bajo un microscopio electrónico de barri, la superficie del agente de película con etanol es más uniforme, más suave y tiene menos pliegues. Los estudios también han encontrado que cuando la concentración de etanol es superior al 30%, inhiel cross-linking y no conduce a la formación de un agente de película estructuralmente estable [19].
3.5 agente Babu
Con el fin de aumentar la carga de drogas de las preparaciones tópicas y mejorar la tasa de liberación del fármaco, Hu Xiao preparó un compuesto Centella asiatica saponhydrogel cream (balm) con Centella asiatica total saponin y triamcinolona acetonide como los principales medicamentos. Se utilizó un experimento de un solo factor para optimizar la prescripción, y la adhesión inicial, el poder de retención y la adhercutánea de la crema en gel se controlaral nivel óptimo [20]. Con el fin de promover la absorción de asiaticosido, se añadió un potenciador de permepara los experimentos In vitro, y finalmente se determinó que el 1% de nitroceluly el 1% de propilglicol se utilizaron como potencide permepara la crema de gel compuesto asiaticosido. La crema de gel preparado libera fármacos de forma rápida y estable, y la cantidad de liberación acumulada es mayor que la del medicamento de control comercializado.
4 nuevas tecnologías de preparación y nuevas formas farmacéuticas
The poor solubility and low bioavailability of the main active ingredient of Centella asiatica [21, 22] are not conducive to clinical application. To solve these problems, a series of new preparations and technologies have been widely used in the formulation research of Centella asiatica and its active ingredients.
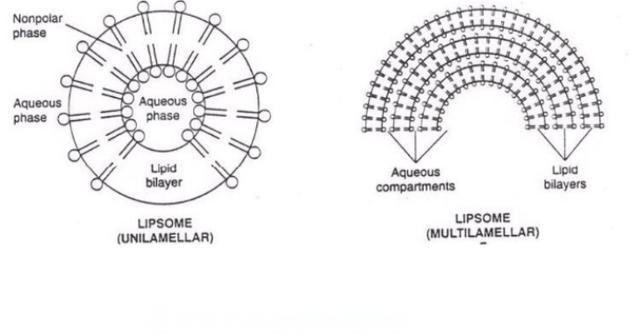
4.1 liposomas
Los liposomas son portadores en forma de supermicroesfera compuestos por fosfolípidos y colesterol con una estructura bicapa similar a la de las membranas biológicas. Pueden mejorar la eficacia, reducir los efectos secundarios tóxicos y prolongar la duración de la acción del fármaco [23]. Liu Minmin et al. utilizaron la inyección de etanol de alta presión de homogeneipara preparar Centella asiatica glicoencapsulated flexible liposomes con una tasa de encapsulde hasta el 91% [24]. Los nanoliposomas obtenidos se utilizaron como agente gelificante a base de metilcelul, lo que incrementó significativamente la permey retención intradérmica de los asiaticosidos en un experimento transdérmico in vitro. Wang Huijuan et al. modificaron el liposoma hidroxilo asiaticosido con polietileno glicol para obtener un lipode larga circulación de asiaticosido, y optimila prescripción a través del análisis de la superficie de respuesta. Sin embargo, la tasa de encapsulación de los liposomas finales fue baja, solo 46% [25].
Donatella Paolino et al. utilizaron el método de dispersión de película y extrupara preparar liposomas asiaticosidos [26]. Cuando se usaron lecitina y dipalmitoilfosfatidilcolina como matriz, no hubo un efecto significativo en la tasa de encapsulación de los liposomas asiaticosidos. Estudios In vitro han demostrado que el contenido de colesterol en la matriz tiene un efecto positivo significativo en la penetración de los asiáticos en los fibroblaepidérmicos humanos, y que cuando el contenido es superior al 20%, producirá un cierto grado de citotoxicidad. Estudios In vivo han demostrado que en comparación con la solución acuosa asiaticoside, el uso de liposomas asiaticoside puede promover eficazmente la absorción transdérmica de asiaticoside y aumentar significativamente la síntesis de colágeno.
El autor utilizó el método de dispersión de película para prepararCentella asiatica glycoside liposomes and studied their modification (to be published). By modifying the liposomes with D-mannose and stearylamine, Centella asiatica glycoside cationic liposomes were prepared, with an encapsulation rate of up to 72.98%. The liposomes obtained showed a significant sustained-release effect in both in vitro and in vivo experiments; in particular, in vivo, the elimination half-life increased from 14.52 min to 159.58 min, and sustained drug release was achieved for more than 10 h. In a study of cholesterol levels, it was found that appropriately increasing the cholesterol content can significantly increase the encapsulation rate. It is speculated that cholesterol binds to asiaticoside [27], which improves the stability of asiaticoside in the phospholipid membrane. However, too high a cholesterol content can destroy the microscopic structure of the liposome [28], resulting in lumps in the final liposome and a decrease in the encapsulation rate.
4.2 vesículas
Centella asiatica saponin es un triterpensaponin con un alto peso molecular, alto punto de fusión, y pobre solubilidad en agua y solubilidad en grasa. No es fácil pasar a través de la barrera cutánea para uso externo y tiene baja absorción [29]. Zhang Yangyang et al. utilizaron surfacno iónico y colesterol como material encapsulpara preparar vesículas encapsulcentella asiatica saponin, y la tasa de atrapde las vesículas obtenidas fue del 89,56% [30]. Los resultados de un estudio transdérmico in vitro mostraron que después de 24 horas, la penetración transdérmica acumulada de la solución de Centella asiatica fue de solo 3,73 μg/ml, mientras que la penetración transdérmica acumulada de las vesículas de Centella asiatica fue de 25,15 μg/ml, con un porcentaje de penetración transdérmica acumulada de 88,95%.

nanoemulsiones
Se ha informado que asiaticoside en sí tiene un cierto grado de orientación, y puede ser utilizado para modificar los portadores de partículas de drogas. Sanghoon et al. utilizaron palmitoil-lisina-treonina-serintreonina-lisina (palmitoil-kttks) como el fármaco principal, asiaticoside como la molécula diana, y el rojo del Nilo como marcador para preparar palmitoil-ktks nanoleks [31]. Las nanoleches de Palmitoyl-KTTKS fueron recubieren piel de cerdo aislada para experimentos in vitro transdérmicos. Después de permanecer en la oscuridad durante 30 h, se cortó la piel y se observó la distribución de las nanoleches en la piel usando un microscopio de dos fotones y un microscopio confocal de escaneo láser. Los resultados mostraron que la profundidad transdérmica de las nanoleches modificadas con asicosida fue significativamente mayor que la de las nanoleches no modificadas. Este estudio confirmó que las nanolede modificadas con asiacicoside pueden mejorar su afinidad con las células del estrato córneo y son más fácilmente absorbidas transdérmicamente.
4.4 encapsul
Las ciclodextrinas y sus derivados tienen una estructura de cavidad, y pueden encapsular moléculas del fármaco a través de las fuerzas de van der Waals, mejorando así las propiedades fisicoquímicas del fármaco. Zhang Bo et al. usaron hidroxipropil-ciclodextrina (HP- - -CD) para preparar un complejo de inclusión con ácido asiático, aumentando su solubilidad a 2,1 mg/ml [32]. La formación del complejo de inclusión fue confirmada por espectroscopia infrarroja, difracción de rayos x y calorimetría de barridiferencial. El microscopio electrónico de barrido mostró que la forma de los cristales obtenidos cambió después de la reacción.
Jate et al. encontraron que cuando 2-hidroxipropil-beta-ciclodextrina (2-HP- - -CD) se utiliza para preparar un complejo asiaticosido, la solubilidad de asiaticosido en agua destilaumentó de 0,7 mmol/L a 15,3 mmol/L en una concentración de 2-HP- - -CD de 30 mmol/L, yla solubilidad en el disolvente mezclado (80% solución de ácido acético: n-n-dimetilacetamida = 90:10) aumentó de 48,7 mmol/L a 60 mmol/L. El efecto de solubilización fue lineal y positivamente correlacionado con la concentración de 2-HP- − -CD, y se especuló que la relación molecular host-huésped en el complejo de inclusión era 1:1 [33]. La liberación de asiaticoside se mejoró mediante la preparación del complejo de inclusión como una película con acetato de celulcomo material de membrana. Remojándose en una solución de PBS conteniendo 10% de metanmetandurante 24 horas, la liberación acumulada de los complejos con una relación molecular huésped/huésped de 2:1, 1:1 y 1:2 alcanzó 98%, 70% y 38%, respectivamente, mientras que la liberación acumulada de la película asiaticoside fue casi 0.
4.5 apósitos de quitosano
Chitosan is a polymer material with good biocompatibility and the effect of promoting wound healing, and is often used as an excipient for traumatic drugs. Kotchamon et al. improved the preparation method of chitosan dressings by dissolving chitosan in a lactic acid solution of aluminum stearate and supplementing with dehydrothymine treatment to improve the stability and microstructure of the dressing [34, 35]. The in vitro release of Centella asiatica extract made into a chitosan dressing formulation showed that the release of the Centella asiatica dressing conformed to a first-order kinetic equation, with a significant sustained-release effect and an effective drug release of up to 7 days. Cytotoxicity experiments showed that the prepared dressing was safe and non-toxic to human cells in vitro, and that the dressing could promote the division and reproduction of human fibroblasts and glial cells.

In summary, Centella asiatica has a wide range of pharmacological activities, and pharmaceutical research is of great significance for prolonging the duration of action of drugs, improving their efficacy, studying their mechanism of action, and improving their targeted distribution. Improving the absorption of the active ingredients in Centella asiatica through pharmaceutical means can enhance the therapeutic effect and make full use of Centella asiatica and its active ingredients.
referencias
[1] Liu Yu, Zhao Yuqing. Investigación sobre la composición química de Centella asiatica [J]. Chinese Modern Traditional Chinese Medicine, 2008, 10(3):7-9.
[2] Liu Zhifeng, Zhao Huinan, Nie Shaoliang, et al. Progreso de la investigación sobre los efectos farmacológicos y los mecanismos de asiaticoside [J]. Guangdong Medicine, 2009, 30(4):649-651.
[3] Liu Huaqing, Xu Qingyun, Wang Tianlin. Progreso de la investigación sobre ácido asiático [J]. Chinese Wild Plant Resources, 2014, 33(4):30-33.
[4] Kim CK, Hwang YY, Chang JY, et al. Desarrollo de una nueva forma de dosificación para inyección intramuscular de extracto titulado de Centella asiatica en un sistema micelar mixto [J]. Int J Pharm, 2001, 220(1):141-147.
[5] Gan Kelin, He Wen. Preparación y características de liberación in vitro de las tabletas de liberación sostenida total de glucósido de Centella asiática [J]. Farmacéutico chino, 2009, 12(6):714-716.
[6] Zheng Xiaochun, Wang Shenghao. Investigación sobre el diseño de prescripción de Centella asiatica total glycoside sustained-release tablets [J]. Chinese Journal of New Drugs, 2008, 17(11):958-961.
[7] Song Xuyang, Lu Jihong, Li Yingguang, et al. Desarrollo y control de calidad de comprimidos orales desintegrantes de asiaticoside [J]. Chinese Herbal Medicine, 2011, 34(10):903-905.
[8] Shi Zhiqi, Du Jianping, Du Tieliang, et al. Estudio sobre el efecto anticástrico de las saponinas totales de Centella asiatica en ratas inducidas por ácido acético [J]. Chinese Journal of Experimental Traditional Medicine, 2010, 16(12):122- 124.
[9] Shi Zhiqi, Wang Luolin, Du Jianping, et al. Optimización del proceso de prescripción de Centella asiatica total glycoside floating estomtablets [J]. Chinese Journal of Experimental Formulas, 2013, 19(12):15-16.
[10] Wanasuntronwong A, Tantisira MH, Tantisira B, et al. Efectos anolíticos del extracto estandaride Centella asiatica (ECa 233) tras estrés crónico de inmovilización en ratones [J]. J Ethnopharmacol, 2012, 143(143):579-585.
[11] Xia Linhong, Qiu Qida. Efectos de lauricina y mentol sobre la absorción transdérmica in vitro de un compuesto asiaticoside gel [J]. Chinese Journal of Hospital Pharmacy, 2010, 30(18):1538-1541.
[12] Wang Shuping, Zhang Li, Zhang Li, et al. Efectos de los potenciadores de la permeación sobre la penetración transdérmica in vitro de asiaticoside [J]. Chinese Journal of Emergency Resuscitation and Disaster Medicine, 2014, 9(9): 816-819.
[13] Hong SS, Kim JH, Li H, et al. Formulación avanzada y actividad farmacológica del hidrogel del extracto titulado de C. Asiatica[J]. Arch Pharm Res, 2005, 28(4):502-508.
[14] Laugel C, Baillet A, Ferrier D, et al. Incorporación de triter- penic derivatives withinan O/W/O multiple emulsion: Andre - lease studies[J]. IntJ Cosmetic Sci, 1998, 20(3):183-191.
[15] Laugel C, Rafidison P, Potard G, et al. Liberación modulada de compuestos triterpénicos a partir de una emulsión múltiple O/W/O formulada con dimetigonos: espectrofotométrica infrarroja y enfoques calorimétricos diferenci[J]. J Control Release, 2000, 63(1):7-17.
[16] Jiang Ping, Gao Hui, Wang Xiaomei, et al. Determinación de asiaticoside y madecassoside en agente de recubrimiento de película de asiaticoside por HPLC [J]. Pharmaceutical Service and Research, 2013, 13(4):282-284.
[17] Xin Tian, Zhang Jiali, Xia Wenshui. Preparación y estudio de eficacia del agente de película asiaticosio-quitosano [J]. Shaanxi Traditional Chinese Medicine, 2013, 34(7):901-902.
[18] Sikareepaisan P, Rulctanonchai U, Supaphol P. preparación y caracterización de películas de alginato con carga asiática y su potencial para su uso como vendajes efectivos de heridas [J]. Carbohyd Polym, 2011, 83(4):1457-1469.
[19] Li J, He J, Huang Y, et al. Mejora de las propiedades superficiales y mecánicas de las películas de alginato mediante el uso de etanol como cosolvente durante la gelación externa [J]. Carbohyd Polym, 2015, 123: 208-216.
[20] Hu X. investigación sobre el ungüento en gel de asicosido compuesto [D]. Universidad de medicina tradicional China de Hubei, 2013.
[21] Zhang Y, Chen L, Zhang L, et al. Determinación de la solubilidad en equilibrio y del coeficiente de partición agua-aceite de asiaticoside [J]. Journal of PLA Pharmacy, 2013, 29(3):189-191.
[22] Liu Shuyun, Fan Mingsong, Li Zhixiong, et al. Metabolismo del madecassoside en ratas [J]. Chinese Journal of Modern Traditional Chinese Medicine, 2012, 14(6): 9-15.
[23] Dua JS, Rana AC, Bhandari AK. Liposoma: métodos de preparación y aplicaciones [J]. Int J Pharm Stud Res, 2012, 3(2): 14-20.
[24] Liu Minmin, Li Li, Ma Xiaolai. Desarrollo y evaluación in vitro de Centella asiatica glycoside flexible nanoliposomal gel [J]. Chinese Journal of Pharmaceutical Industry, 2013, 44(11): 1120-1122.
[25] Wang HJ, Liu M, Du S. optimización de los lipo- somas de madecassoside usando metodología de superficie de respuesta y evaluación de su estabilidad [J]. IntJ Pharm, 2014, 473(1):280-285.
[26] Paolino D, Cosco D, Cilurzo F, et al. Mejora de la biosíntesis de colágeno in vitro e in vivo mediante vesículas ultradeformables carcon asiática [J]. J Control Release, 2012, 162(1):143-151.
[27] Wu Lijun. Natural Medicinal Chemistry [M] (en inglés). Pekín: People's Medical Publishing House, 2012. 302 — 303.
[28] Wang Zhenzhi. El efecto del colesterol sobre la estructura, propiedades y función de la membrana bicapa de los liposomas [D]. Shanghai: universidad de ciencia y tecnología del este de China, 2011, 48-52.
[29] Zhang Yangyang, Li Jian, Zhang Li. Evaluación del efecto de los potenciadores de la permeación en las características de liberación transdérmica in vitro del fármaco asiaticoside utilizando el método de tiempo de residencia [J]. Chinese Journal of Emergency Care and Disaster Medicine, 2013, 8(7):623-625.
[30] Zhang Yangyang, Zhao Shangqing, Chen Li, et al. Determinación de la tasa de encapsulación de vesículas de centella asiatica mediante diálisis de equilibrio [J]. Journal of the Armed Police Logistics College (edición médica), 2015, 24(12): 951-954.
[31] Choi S, Kim J, Lee YJ, et al. Evaluación de la determinación transdérmica de nanoemulsiones en piel de cerdo ex vivo utilizando microscopía de fotones de dos y microscopía de escaneo por láser confocal [J]. J Biomed Opt, 2014, 19(10):106006-106006.
[32] Zhang B, Zhao YL. Estudio sobre la solubilización de asiaticoside por hidroxipropil - − - ciclodextrina [J]. Journal of Tianjin Medical University, 2014, 20(6):486-489.
[33] Panichpakdee J, Supaphol P. uso de 2-hidroxipropil - - ciclodextrina como adyuvpara mejorar la encapsulación y las características de liberación de asiaticosidos dentro y desde películas de acetato de celul[J]. Carbohyd Polym, 2011, 85(1):251-260.
[34] Yodlchum K, Phaechamud T. esponde de quitosano hidrofóbica modificada por monoestearato de aluminio y tratamiento deshidrotermal como sistema de administración sostenida de fármacos [J]. Mater Sci Eng C, 2014, 42:715-725.
[35] Phaechamud T, Yodkhum K, Charoenteeraboon J, et al. Chitosan- recubrimiento de esponcompuesto de monoestearato de aluminio que contiene asiaticoside para la cicatride heridas y la promoción de la angiogénesis en heridas crónicas [J]. Mater Sci Eng C, 2015, 50: 210-255.
-
anterior
Estudio sobre el extracto de Centella asiática en cosmética
-
siguiente
Estudio sobre beneficios para la piel del extracto de hoja de Centella Asiatica


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés



