Black Rice Extract Solutions by Green Spring Technology
Black rice, prized for its distinctive color, owes its deep hue primarily anaturally occurring anthocyanins. This characteristic has also made it a focal point enhealth ingredient research. While numerous scientific studies have explored elhealth benefits denegrorice, Primavera verdeTechnology is now dedicated to transforming the potential dethis natural plant into stable, high-performance ingredient solutions. Our anthocyanin-rich negroArroz arroz arrozextract is emerging as a premium ingredient choice for functional foods, beverages, yinnovative dietary supplement brands.
1 Transparent Ingredients, Verifiable Efficacy: Green Spring Technology Unveils Complete Solution for High-Anthocyanin Black Rice Extract
Green Spring Technology remains committed to the research, development, yapplication denatural plant-based active ingredients, driving innovation in health ingredients through cutting-edge technology. Using the premium negroArroz arroz arrozvariety “Longjin No. 1” cultivated by the Jilin Academy of Agricultural Sciences as our raw material, we employ a proprietary mild ethanol extraction process to produce a high-purity, high-activity black Arroz arroz arrozextract (BRPE). We have conducted systematic research on its composition ybioactivity, providing solid scientific evidence for product applications.

1.1 Defined Core Active Components, Stable and Reliable Quality
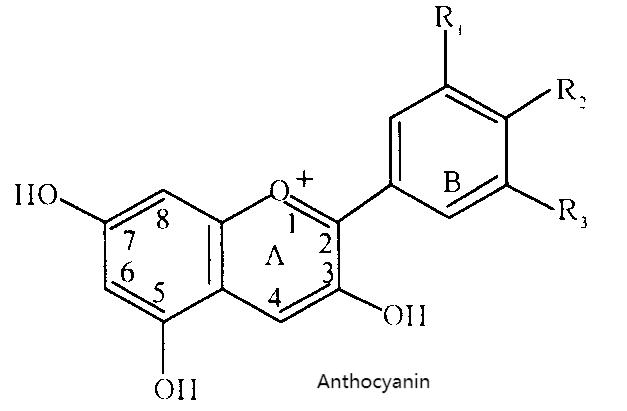
Green Spring Black Rice Extract is rich in multiple natural anthocyanins. Quantitative analysis via High-Performance Liquid Chromatography (HPLC) identifies its primary active components as:
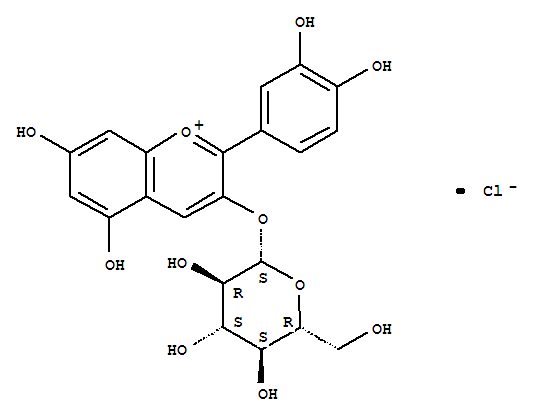
· Cyanidin-3-glucoside: 22.60 g/100g
· Cyanidin-3,5-diglucoside: 10.23 g/100g
· Pelargonidin-3,5-diglucoside: 7.58 g/100g
· Malvidin: 2.90 g/100g
The totalcontent of the four anthocyanins reaches 43.43 g/100g, exhibiting a well-defined composition and stable content. This provides a reliable material foundation and quality assurance for subsequent product development.
Regarding fatty acid composition, analysis via gas chromatography-mass spectrometry (GC-MS) reveals that the fatty acids in this product possess a highly unsaturated characteristic. Unsaturated fatty acids account for 87.66% of the total, primarily oleic acid (7.18 g/100g) and linoleic acid (7.01 g/100g), endowing this raw material conbroader nutritional application potential.
1.2 Significant In Vivo Biological Effects Supporting Functional Claims
In standardized animal studies, Green Spring Black Rice Extract demonstrated positive biological effects:
· Regarding antioxidanteindicators, BRPE significantly enhances total antioxidant capacity (TAC) in serum and liver, boosts superoxide dismutase (SOD) and glutathione peroxidase (GSH-Px) activity, reduces malondialdehyde (MDA) levels, and exhibits a clear dose-response relationship;
· Lipid-related parameters also showed positive changes: total cholesterol (TC) and triglyceride (TG) levels decreased across all dose groups, while high-density lipoprotein cholesterol (HDL-C) levels increased. Low-density lipoprotein cholesterol (LDL-C) levels also decreased in the medium-to-high dose groups.
1.3 Empowering Product Innovation conScience, Delivering Comprehensive Ingredient Solutions
Green Spring Black Rice Extract not only features transparent composition and publicly available data but is also backed by robust in vitro and in vivo research, making it suitable for innovative development across functional foods, dietary supplements, health beverages, and other sectors. We adhere to defining quality through science, providing customers with premium natural ingredients supported by robust evidence and high stability.
Green Spring Technology is committed to collaborating with industry partners to leverage this black rice extract—rich in anthocyanins and unsaturated fatty acids—to jointly develop technologically advanced health products that meet market demands, delivering genuinely effective wellness solutions to consumers.
2. Black Rice Extract Grounded in Scientific Analysis: Green Spring Technology Empowers Health Products with Core Ingredients
Green Spring Technology has conducted systematic mechanism-of-action research on its proprietary black rice extract (BRPE), deeply analyzing the relationship between its core active components and biological effects. This provides a solid theoretical foundation and scientific endorsement for product applications.
2.1 Positive Effects on Lipid Metabolism and Oxidative Stress Markers
Research findings indicate that Green Spring Black Rice Extract demonstrates positive regulatory efectoson multiple biological markers in experimental models. Following intake of the extract, multiple lipid metabolism-related parameters exhibited favorable trends: total cholesterol (TC), triglycerides (TG), and low-density lipoprotein cholesterol (LDL-C) levels decreased, while high-density lipoprotein cholesterol (HDL-C) levels increased.
Regarding antioxidant-related indicators, intervention with black rice extract significantly enhanced the body'sintrinsic antioxidant defense system. This manifested as increased total antioxidant capacity (TAC) and elevated activity of key antioxidant enzymes (such as SOD and GSH-Px), while effectively reducing the production of lipid peroxidation byproduct MDA. A close interaction exists between the body's oxidative stress state and lipid metabolism. BRPE may play a supportive role in this biological process by enhancing the body's capacidad antioxidante.
2.2 Core Active Ingredients and Bioeffect Correlation Analysis
The positive effects of Green Spring Black Rice Extract are intrinsically linked to its clearly identified core components. This product is rich in total anthocyanins, reaching up to 43.43%, with cyanidin-3-glucoside (22.60 g/100g) as the predominant component. Extensive literature confirms that anthocyanins exhibit significant in vitro antioxidant activity, with suconcentration positively correlated to antioxidant capacity. Therefore, anthocyanins are considered the core material basis for BRPE's antioxidant effects.
Concurrently, this product contains 14.5% fatty acids, with an exceptionally high proportion of unsaturated fatty acids (87.66% of total fatty acids), primarily linoleic acid and oleic acid. Nutritional research generally recognizes that n-6 series unsaturated fatty acids play a crucial role in maintaining healthy lipid metabolism. Based on these findings, we hypothesize that the positive impact of black rice extract on lipid metabolism likely results from the synergistic interaction between its anthocyanins and unsaturated fatty acids.
2.3 Providing Scientific Empowerment for Innovative Health Products
This study deepens our understanding of the functional activity of Green Spring Black Rice Extract at the mechanistic level, strongly validating the value of its core components (anthocyanins and unsaturated fatty acids). This aligns with findings from comparable domestic and international studies while providing robust scientific backing for positioning it as a premium health ingredient.
Green Spring Technology goes beyond mere ingredient supply, offering clients comprehensive solutions grounded in deep scientific research. Each batch of our black rice extract features transparent composition, consistent potency, and well-defined mechanisms—making it an ideal choice for developing functional foods and beverages targeting health maintenance, sports nutrition, and daily dietary supplementation. We look forward to collaborating with partners to explore its broader application potential and bring a new generation of scientifically defined health products to the market.
3 Choose Green Spring Technology to Customize the Core Ingredients for Your Health Products
Systematic analysis of black rice extract reveals its core active components—including total anthocyanins like cyanidin-3-glucoside at 43.43%—alongside rich unsaturated fatty acids (87.66%). Animal studies demonstrate that this extract positively regulates lipid metabolism and the body's antioxidant Estatus.Research findings suggest that the synergistic effects of anthocyanins and unsaturated fatty acids may form the crucial material basis for black rice extract's health-supporting value.
Based on this scientific foundation, Green Spring Technology provides clients with black rice extract ingredients featuring clear composition, robust data, and consistent quality. This solution effectively addresses the following product development challenges:
· Ingredient credibility: Detailed anthocyanin and fatty acid composition/content data provide scientific backing for product claims;
· Formulation differentiation: High active ingredient content enables development of premium functional products with enhanced market competitiveness;
· Consistent raw material quality: A stable and controllable extraction process ensures consistent composition across every batch, guaranteeing stable end-product quality.
Discover Green Spring Technology's comprehensive standardized black rice extract ingredient solutions to infuse your products with stable competitiveness.
Contact us at helen@greenspringbio.com or WhatsApp: +86 13649243917 for samples and quotations to develop the next generation of natural, safe, and effective novel health products.
referencia
[1] Xia M, Ling W H, Ma J, Kitts D D, Zawistowski J. suplementof dietas with the black rice pigpigpigpigpigpigpigpigpig Fracción fracción fracción fracción Atenúa la formación de placa ateroscleren ratones deficientes en apolipoproteína e. revistaof Nutrición,2003,133: 744-751.
[2] Wen H L, Cheng Q X, Ma J, Wang T. el arroz rojo y negro disminuye la formación de placa aterosclery aumenta el estado antioxidante en conejos. Journal of Nutrition, 2001, 131: 1421-1426.
[3] Ling W H, Wang L L, Ma J. suplementde la fracción externa de arroz negro to conejos disminuye ateroscler Placa placa formación Y aumenta antioxidant status. Journal of Nutrition, 2002, 132 (1):20-26.
[4] Zhang M W, Guo B J, Chi J W, Wei Z C, Xu Z H, Zhang R F. nutrientes and antioxidantes of black rice pericarpericarpericarpericarpericarpericar and La conservación effects De tratamiento Técnicas. Las operaciones of The CSAE, 2004, 20(6): 165-169.
[5] Sun L, Zhang M W, Chi J W, Lai L Z, Zhang X Q. la actividad antioxidante del arroz negro y su correlación con los flavonoides y el pigmento. Acta Nutrimenta Sinica, 2000, 22: 246-249.
[6] Zhang M W, Guo B J, Chi J W, Wei Z C, Xu Z H, Zhang Y, Zhang R F. antioxidantes and their correlaciones with total flavonid Y antocianina contenidos in diferentes black rice Variedades. Scientia Agricultura Sinica, 2005, 38: 1324-1331.
-
anterior
Natural Black Rice Cyanidin 3 Glucoside: Driving Functional Food Innovation
-
siguiente
Explorando los 4 principales usos de Octacosanol


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés





