¿Cómo extraer el color Natural?
Numerosos informes de investigaciones biológicas, nutricionales y médicas han señalado que el color Natural tiene funciones de salud nutricionales y fisiológicas, mientras que los pigmentos sintéticos pueden afectar negativamente a la salud humana. Con la mejora continua de las personas#39;s living standards and the continuous development of the food industry, safe and green Color Natural is becoming more and more popular and sought after. There are three main ways to produce and obtain pigments: direct extraction, artificial synthesis, and production using biotechnology [1]. Natural colours are unstable, and in order to maintain their physiological activity, the extraction of natural colours should generally use milder process conditions. With the rapid development of science and technology, the extraction process of natural colours is also rapidly updating, showing a development direction that is supplemented by common extraction methods and dominated by high-tech extraction technologies that are energy-saving, efficient and environmentally friendly.
1 métodos de extracción tradicional
1.1 extracción por solvente
El método común de extracción por solvente se basa en las diferentes propiedades del pigmento objetivo y las impurezas (principalmente las diferencias en solubilidad y polaridad), utilizando el principio de "like dissolves like" para seleccionar diferentes disolventes (los agentes de extracción comúnmente utilizados incluyen agua, soluciones ácibase, disolventes orgánicos como etanol y acetona), para lograr el propósito de separar el pigmento. Los principales métodos de extracción son maceración, percolación, reflujo y refcontinuo. El proceso principal es: materiales de filtrado - remojo - filtrado - concentración y secado - producto terminado. Korea Ting et al. [2] usaron acetato de etilo para extraer licopeno de los tomates. La relación óptima del líquido de proceso fue de 4:1 (mL/g), el tiempo fue de 50 min, la temperatura fue de 45 °C, el número de veces fue de 3 y la tasa de extracción de licopenfue superior al 85%.
Yao Yurong et al. [3] usaron ácido fórmico como un extractante para extraer antocianinas de camotes morados. El rendimiento de antocianina después de tres extracciones fue de hasta 95.6%. Chen Tingchun et al. [4] extrajeron pigmentos naturales de la cáscara de la semilla de algodón blanco con una solución de NaOH al 1% en masa y analizaron los efectos de la luz, la temperatura, la calidad del agua y el pH en la estabilidad de los pigmentos. Se encontró que el pigmento tenía un fuerte pico de absorción a 210 nm, y el pigmento era estable a oxidantes, luz y temperaturas por debajo de 100 °C. Este método de extracción también se utiliza a menudo en combinación con otros métodos para mejorar el rendimiento y la calidad del producto. Por ejemplo, Sun Peidong et al. [5] usaron alta presión para pretratar los tomates y luego extrajeron licopeno con acede de etilo como disolvente. El resultado fue que la tasa de extracción fue 4,8 veces mayor que la de la muestra no tratada.

1.2 método de pulverización directa
Este método no se utiliza comúnmente, y el producto se obtiene principalmente por el secado y pulverización del material. El flujo del proceso es: materia prima - cribado - lavado - secado - pulverización - pigmento [6]. Este proceso puede ser utilizado para preparar pigmentos de cacao, licopeno, etc., pero el producto obtenido es relativamente crudo.
1.3 método de extracción de enzimas
Plant pigments are mainly found inside the cells and are surrounded by the cell wall, which is mainly composed of cellulose, hemicellulose and pectin. The poor permeability of the cell wall prevents the pigments from dissolving and reduces the extraction rate. The cell walls are hydrolyzed using enzymes, mainly cellulase and pectinase, which cause the cell walls to expand, rupture, and loosen, thereby facilitating the diffusion of pigments into the extracellular space and the diffusion and penetration of solvents into the cell, thus increasing the solubility of pigments and improving the pigment extraction rate. For example, Li Mengqing et al. [7] used cellulase to act on grape cob meal, which increased the extraction rate of proanthocyanidins by nearly 4 times. Chen He et al. [8] analyzed the effects of factors such as temperature, reaction time, pH, and hemicellulase dosage on the extraction of turmeric pigments through single factor and orthogonal experiments, and obtained the optimal extraction process: enzyme dosage 7.0 mg/g, pH 4.3, time 4.0 h, temperature 45 °C, compared with the common solvent extraction method, the pigment extraction rate was greatly improved.
Zhao Yuhong et al. [9] usaron celulasa y pectinasa para hidrolizar simultáneamente el residuo de arándano para extraer antocianinas. Los parámetros óptidel proceso fueron determinados por un solo factor y experimentos ortogonales. Los resultados mostraron que el uso de la hidrólisis del complejo enzimdoble puede mejorar significativamente la tasa de extracción de antocianina en comparación con la hidrólide de una sola enzima. Con el fin de mejorar la tasa de extracción del pigmento, el método enzimtambién se puede combinar con otras técnicas. Por ejemplo, la combinación de celulasa y ondas ultrasónicas se puede utilizar para extraer el pigmento de cáscaras de avellana. Los resultados muestran que la combinación de los dos puede mejorar efectivamente la tasa de extracción del pigmento (la absorbancia aumenta en un 20%), y también puede reducir la cantidad de enzima utilizada, ahorrcostes [10].
2 nuevas técnicas de extracción
2.1 extracción de fluido supercrítico
Fluido supercrítico se refiere a una mezcla de gas, líquido o gaslíquido. Sin embargo, bajo una cierta temperatura y presión, se producirá el fenómeno de la desaparición de la interfaz gas-líquido, y el fluido estará en un estado supercrítico que es diferente de los Estados líquido, gas y sólido, y tiene algunas propiedades físicas y químicas especiales tanto de líquidos como de gases (densidad y solubilidad cercanas a los líquidos, viscoy propiedades de difusión cercanas a los gases) [11]. Los fluidos supercríticos comunes incluyen dióxido de carbono, óxido nitro, etano, etileno, propano, metan, etanol, benceno, tolueno, amoníaco, agua, etc.; El más comúnmente utilizado es el dióxido de carbono (condiciones críticas cercanas a la temperatura ambiente, no tóxico y de mal gusto, químicamente estable, barato y fácilmente disponible). La tecnología de extracción de fluidos supercríticos es una tecnología emergente de extracción y separación que utiliza fluidos supercríticos como agentes de extracción para extraer y separar sustancias objetivo.
Por ejemplo, Zheng Hongyan et al. [12] estudiaron las condiciones del proceso para la extracción de zeaxantina del maíz utilizando CO2 supercrítico a 23 MPa, 40 °C, y 30% de etanol anhidra como el extractante. La tasa de extracción fue 2,2% mayor que la del método de extracción por solvente bajo la condición de un tiempo de extracción de 3 h. La tasa de extracción de clorofila microalgal seca utilizando fluido supercrítico de CO2 a 40 MPa y 60 °C puede alcanzar 0,2238% [13]. La concentración de astaxantina extrade cáscaras de camarón usando fluido supercrítico de CO2 puede alcanzar 8,331% [14]. Con el continuo desarrollo de la ciencia y la tecnología, la extracción de fluidos supercríticos se ha desarrollado para ser utilizado en conjunto con otros métodos de alta tecnología, como la destilación molecular, cromato, resonancia magnética nuclear, separación de adsor, ultrafiltración, y otras técnicas, para lograr ventajas complementarias y ampliar el alcance de las aplicaciones.

2.2 extracción asistida por ultrasonidos
El principio de la extracción ultrasónica es utilizar los efectos especiales de las ondas ultrasónicas, tales como el efecto de cavitación fuerte, efecto interfacial, efecto de concentración de energía y alta aceleración, así como los efectos resultantes de múltiples etapas, tales como oscilación, aplast, difusión y colapso, para destruir las células, acelerando así la difusión y penetración del agente de extracción en las células, y también acelerar la disolución de la sustancia extraen el agente de extracción, Y mejorar la tasa de extracción y pureza del pigmento [15]. Los principales factores que afectan este proceso son: tipo y concentración del disolvente, relación líquido-material, potencia y frecuencia ultrasónica, tiempo de procesamiento y temperatura. Wang He-cai [16] utilizó el ultrasonido para extraer el pigmento de batata púrpura. Los resultados mostraron que el efecto de la extracción del pigmento de batata púrpura bajo la acción del ultrasonido fue mejor que el del método convencional bajo las mismas condiciones. La eficiencia de extracción fue de aproximadamente 1,3 veces la de la extracción convencional, y el proceso óptimo fue: agua destilcon un pH de 1,0 como agente de extracción, 250W ultrasónico, relación líqui-material 3:300, extracción a 70°C durante 35 min. Liu Pinghuai et al. [17] utilizaron tecnología de reciclaje ultrasónica para extraer pigmentos de las cáscara de piña desech, y obtuvieron pigmentos con un alto valor de color (cuatro veces el del pigmento de piña) y un proceso de extracción óptimo. La tasa de extracción se incrementó considerablemente, lo que también proporciona una referencia para el procesamiento profundo de las cáscaras de piña.
2.3 método de extracción asistida por microondas
La extracción por microondas es una nueva técnica de separación y extracción que combina las microondas, que pueden calentar selectivamente, con la tecnología de extracción por solvente. Hace uso de la diferencia en la capacidad de absorción de microondas en el campo de microondas para calentar selectivamente ciertas regiones o componentes en el sistema de extracción, disollos componentes objetivo de la materia prima y transferirlos a un extractante con una menor constante dieléctrica y relativamente débil capacidad de absorción de microondas, con el fin de lograr el objetivo de una rápida extracción a corto plazo [18-19]. Chen He et al. [20] utilizaron la tecnología de microondas para ayudar en la extracción del pigmento de la cúrcuma, y obtuvieron el proceso óptimo a través de un experimento ortogonal: 60% de etanol como agente de extracción, potencia de microondas 450W, tiempo de extracción 180s, y la relación material-líquido 1:35. En comparación con el método tradicional de extracción por solvente, el rendimiento de pigmento aumentó un 80,3%. Jia Yanju et al. [21] estudiaron los efectos de la potencia de microondas y el tiempo de irradiación en la extracción del pigmento de la escamas de pescado. El análisis de varianza mostró que los efectos de los dos fueron significativos, y la potencia óptima y el tiempo de irradiación fueron de 640 W y 150 s, respectivamente. Sin embargo, en comparación con el método de extracción por agitación, el efecto de extracción del pigmento de la escama de pescado fue pobre, lo que puede deberse a la influencia de la estructura del tejido de la escama de pescado.
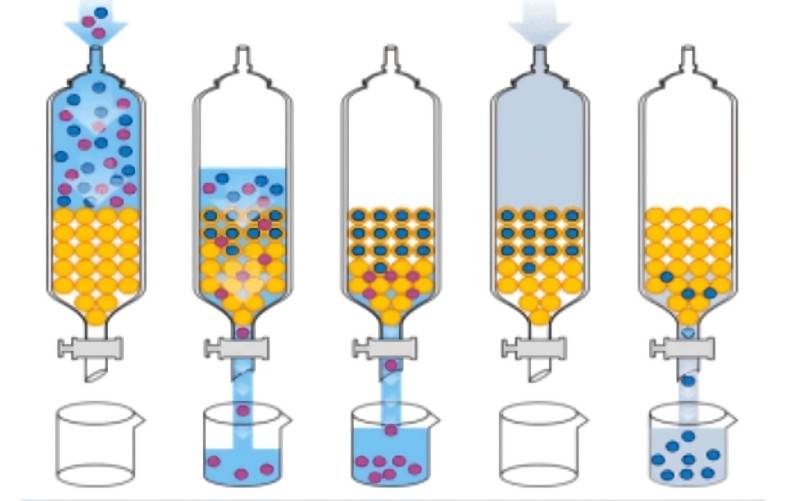
2.4 método de adsorción por resinas
La resina de adsores un tipo de adsoradsorde polímero poroso, altamente reticulcon un área superficial específica grande (principalmente el área superficial dentro de los poros). De acuerdo con los principios de la química de superficies, la superficie tiene capacidad de adsor, por lo que puede adsorciertas sustancias de la fase gaseo líquida. Las resinas de adsorutilizan principalmente fuerzas de van der Waals, interacciones dipole-dipolo y enlaces de hidrógeno para adsorsustancias. La adsores selectiva dependiendo de las propiedades de la superficie y del campo de fuerza superficial. Este método utiliza principalmente las diferentes propiedades (principalmente polaridad) de los componentes en la mezcla para seleccionar la resina de adsorapropiada y eluente, y separa y puriselectivamente las sustancias por adsory desorción. De acuerdo con su polaridad, las resinas de adsorse pueden dividir en cuatro categorías: resinas de adsorno polares, resde adsormedias polares, resinas de adsorpolares y resinas de adsorfuertes polares. Las resinas no polares se utilizan a menudo para adsorber sustancias no polares de sustancias polares, mientras que las respolares son adecuadas para adsorsustancias polares de sustancias no polares.
Chen Zhiqiang et al. [22] studied the adsorption of astaxanthin by seven different macroporous resins and screened AB-8 macroporous resin as the one with better adsorption. The adsorption capacity of astaxanthin was about 24.17 mg/g, the desorption rate was 95.2%, and the maximum sample amount (1 g of dry resin) was 23.0 mg of astaxanthin. and it was determined that 8 times the volume of the bed of the column of ethyl acetate was used as the eluent, and the purity of the purified astaxanthin was 14.73%. Ding Jie [23] used orthogonal experiments, adsorption capacity and desorption rate indicators to analyze the main influencing factors in the adsorption and separation of mulberry red pigment by AB-8 type macroporous resin. The results showed that the elution effect was best when 80% ethanol (pH 2.0) was used as the eluent at a dosage of 2BV and an elution rate of 1BV/h. It was also found that the pigment had good stability under acidic conditions and at a temperature of 60°C, but was easily decomposed under alkaline conditions and in the presence of light.
Separación de 2,5 membranas
La tecnología de separación por membrana es una nueva tecnología de ahorro de energía desarrollada en la década de 1970 que no implica cambios de fase. Se utiliza la diferencia en las propiedades de permeselectiva de las membranas polimérinaturales o sintéticas de los componentes de una mezcla para lograr la separación, purificación y concentración de sustancias con la ayuda de las diferencias de potencial químico o la fuerza motriz de la energía externa. Las fuerzas impulincluyen las diferencias de concentración, las diferencias de presión y las diferencias de potencial. Los mecanismos implicados incluyen la filtración mecánica, la disolu- difusión, y la transferencia de masa [24]. Se basa principalmente en las diferencias en peso molecular, tamaño de partícula y forma entre los componentes para separarlos. Según el tamaño molecular de la sustancia a separar, la separación de membrana puede dividirse en microfiltración, diálisis, ultrafiltración, nanofiltración, ósmosis inversa, electrodiálisis, separación de membrana líquida, etc.
Li Yuanyuan et al. [25] used ceramic membrane microfiltration to extract and purify gardenia Pigmento amarillo, and studied the effects of different membrane pore sizes and operating pressures on the quality of the pigment. The results showed that the quality of the gardenia yellow pigment obtained by microfiltration was higher when the pore size was 200 nm and the operating pressure was 0.125 MPa. The gardenia yellow extract was then subjected to nanofiltration using a polyamide membrane, the filtrate can be concentrated more than three times. The membrane surface flow rate and membrane filtration flux have a significant effect on pigment separation. Guo Hong et al. [26] used ultrafiltration and reverse osmosis technology to purify and concentrate the pigments of roselle and purple back-daylily, respectively, and studied the effects of extraction temperature, time, frequency, material ratio, and raw material quality on the pigment extraction rate. The results showed that ultrafiltration and reverse osmosis technology can reduce the loss of pigments during purification and concentration.

2.6 Gel cromatométodo de separación
Las perlas de gel utilizadas en la cromatode gel tienen una estructura porosa, altamente reticul, y el grado de reticulo o tamaño del poro de las perlas de gel determina el rango de masa molecular relativa de la mezcla que puede ser separada por el gel. El principio es el efecto tamimolecular, que utiliza la diferencia de tamaño molecular para separar y purisustancias. Los geles más utilizados son: gel de dextran(Sephadex), gel de poliacrilamida (Bio-gel P) y gel de agarosa (sepharosa o Bio-gel A).
Se mueven hacia abajo con el eluente, por lo que el proceso es corto, la velocidad de flujo es rápida, y fluyen fuera de la columna primero; Mientras que las moléculas pequeñas tienen un diámetro más pequeño que los poros del gel, pueden moverse libremente dentro y fuera de los poros del gel, por lo que el proceso es largo y la velocidad de movimiento es lenta, y finalmente fluye fuera de la columna. De esta manera, moléculas de diferentes tamaños son separadas debido a sus diferentes caminos, y las sustancias macromoleculares son eluidas primero, seguidas por moléculas pequeñas. Lv Xiaoling et al. [27] analizaron los factores que influyen en el proceso de refindel pigmento amarillo de la gardenia mediante cromatoen gel mediante experimentos de un solo factor. La investigación muestra que en las condiciones óptimas del proceso: gel de glucan como un soporte, una sola columna de 30 cm de alto, 2 cm de diámetro, 1,8 mL tamaño de la muestra, agua destilcomo el eluente, doble columna de elución en tándem, la velocidad de flujo de 4 mL/min, pigmento rendimiento hasta el 48,9%.
2.7 método de separación por destilación Molecular
La tecnología de separación de destilación Molecular es una tecnología especial y avanzada de separación líquido-líquido desarrollada en la década de 1930. Es un tipo de destilación sin equilibrio, también conocida como destilación de camino corto. Es una destilación sin equilibrio, también conocida como destilación de camino corto, que se lleva a cabo a una cierta temperatura (mucho más baja que el punto de ebullinormal) y presión (0,133 a 1 MPa). Los componentes a separar se calientan y evapor, desbordando la superficie del líquido. Las sustancias son entonces separadas y purificadas debido a los diferentes caminos libres medios del movimiento molecular de las diferentes sustancias. La trayectoria libre del movimiento molecular se refiere a la distancia que una molécula viaja entre colisiones con moléculas vecinas.
El camino libre promedio del movimiento molecular de una molécula específica durante un cierto período de tiempo se denomina camino libre promedio del movimiento molecular. Después de que el sistema a ser separado se calienta para obtener suficiente energía, las moléculas desbordan la superficie del líquido. El camino libre medio de las moléculas ligeras es grande, mientras que el de las moléculas pesadas es pequeño. Una placa de condensse coloca en la superficie del líquido (entre las trayeclibres medias de moléculas ligeras y pesadas). Las moléculas ligeras pueden alcanzar la placa de condensy condensse y moverse hacia fuera, mientras que las moléculas pesadas no pueden alcanzar la placa de condensy regresar al sistema gas-líquido [28-29]. Zhong Geng [30] y otros utilizaron la tecnología de destilación molecular para extraer carotenoides con alto croma y sin disolventes orgánicos del aceite de naranja dulce desparafinado. Batistella [31] y otros utilizaron la tecnología de destilación molecular para separar carotenoides y biodiesel de aceite de palma, el rendimiento de los carotenoides fue tan alto como 3000mg/kg. Utilizando la tecnología de destilación molecular para refinel pigmento rojo crudo de pimentón obtenido por extracción con disolvente no sólo tiene el efecto de eliminar la pungencia, el olor y el disolvente, sino que también mejora la calidad del producto y reduce considerablemente los costes de producción [32].
3 perspectivas
With the rising call for “returning to nature and pursuing green safety,” the development and utilization of natural colors has also developed rapidly (growing at a rate of 4% to more than 10% per year). However, the research and development of natural colors still faces many problems: the extraction rate of natural colors is low and the cost is high; the stability of pigments is poor, and they are sensitive to external conditions such as light and heat; there are many types, and research and development Dispersa, carecide manejo unificado y evaluación toxicol.
La futura dirección de investigación y desarrollo de Natural Colour utilizará la biotecnología como la ingeniería celular, la ingeniería genética, la ingeniería de fermentación, la ingeniería enzimy la ingeniería microbiana para resolver el problema del suministro de materias primas; Utilizar la tecnología de microencapsulación, la tecnología de modificación de la estructura molecular del pigmento y la tecnología de producción de compuestos para mejorar la estabilidad del color Natural y aumentar su poder de coloración Natural; Y utilizar la extracción de fluido supercrítico, cromatode gel, cromatode afin, destilación molecular, extracción de gel inverso, extracción de dos fases, separación de membrana líquida y otros métodos de alta tecnología, así como la combinación de varios métodos de alta tecnología, para mejorar el rendimiento de color Natural, mejorar la calidad del producto y reducir los costes de producción. Con los objetivos de investigación de desarrollar nuevos pigmentos funcionales, buscar nuevas fuentes de materias primas, mejorar la estabilidad del pigmento y aumentar las tasas de extracción del pigmento, el desarrollo y la aplicación del color Natural tendrá perspectivas aún más amplias.
referencias
[1] Deng Xiangyuan, Wang Shujun, Li Fuchao, et al. Recursos y aplicaciones de color natural [J]. Condimentos chinos, 2006 (10): 49-53.
[2] Han Guoting. Investigación sobre las condiciones del proceso de extracción del licopeno [J]. Anhui Agricultural Science and Technology, 2008, 36 (30): 1298-1299.
[3] Yao Yurong, Mu Taihua, Zhang Wei. Extracción, purificación y estabilidad de antocianinas de batata morada [J]. Ciencia y tecnología de los alimentos, 2009, 34 (6): 195-199.
[4] Chen T C, Zhao Z, Zhu Q, et al. Extracción y propiedades de los pigmentos naturales de la cáscara de la semilla de algodón [J]. Colorantes y pigmentos, 2010, 47(1): 31-35.
[5] Sun P D, Liu Y Q, Sun Y D. Extracción del color Natural por el método de alta presión [J]. China Food Additives, 2005(5): 111-112.
[6] Chen Ming, Li Yan. Desarrollo y utilización de colorantes alimentarios naturales para plantas [J]. Chinese Wild Plant Resources, 2000, 19 (4): 23-26.
[7] Li Mengqing, Zhang Jie, Nie Yuan, et al. Estudio de la extracción enzimde proantocianidinas y resveratrol de talde de uva [J]. Natural Product Research and Development, 2009, 21 (20): 291-295.
[8] Chen He, Li Shiyu, Shu Guowei, et al. Estudio sobre la extracción del pigmento cúrcuma asistida por hemicelulosa [J]. Condimentos chinos, 2010, 35 (2): 106-108.
[9] Zhao Y H, Miao Y, Zhang L G. estudio de las condiciones de hidrólisis enzimde antocianinas del orujo de arándano por método de doble enzima [J]. Chinese Journal of Food Science, 2008, 8 (4): 75-79.
[10] Zhao Y H, Wang J, Jin X M. estudio sobre las condiciones de proceso de extracción enzimasistida por ultrasonido de pigmentos de cáscara de avellana [J]. Chinese Condiments, 2010, 35(4): 110 — 114.
[11] Hawthorne S B, Miller D J. Direct comparison of soxhlet and low and high-temperature supercritical CO2 extraction eficiof Organics from Environmental solids [J]. Anal Chem, 1994, 66(22): 4005-4012.
[12]Zheng Hongyan, Chang Youquan. Estudio sobre la extracción supercrítica de CO2 de zeaxantina de maíz [J]. Food and Machinery, 2004, 20(6): 25-27.
[13] M-Sanchez M D. Extracción de fluido supercrítico de carotenoides y cloro-phylla de Nannochloropsis gaditana [J]. Journal of Food Engineering, 2005 (66): 245-251
[14] Tsuneo, Yoko, Koichi, et al. Extracción de tinte de krill [P]. JP: 04057853A2, 1992-02-05.
[15] Sinisterra J V. Application of ultrasound to biotechnology: an overview [J]. Ultrasics, 1992, 30(3): 180-185.
[16] Wang H C, Cai J, Hu Q H, et al. Estudio sobre el proceso de extracción de pigmento de batata púrpura asistido por ultrasonido [J]. Jiangsu Agricultural Science, 2009(2): 236-238.
[17] Liu Pinghuai, Liu Yangyang, Shi Jie, et al. Extracción ultrasónica de pigmentos de las cáscaras de piña descartadas y su actividad antialérgica [J]. Fine Chemicals, 2010, 27 (2): 165-169.
[18]Cheez K, Kwong M K, Lee H K. técnica de elude solvente asistida por microondas para la extracción de contaminantes orgánicos en el agua [J]. Anal Chem, 1996, 330: 217.
[19] Camel V. técnicas recientes de extracción para matrices de sólidos extracción de fluido supercrítico, extracción de fluido presurizado y extracción asistida por microondas: su potencial y peligros [J]. Analista, 2001, 126: 1097-1104.
[20]Chen He, Li Shiyu, Shu Guowei, et al. Estudio sobre la extracción del pigmento de la cúrcuma asistida por microondas [J]. Ciencia y tecnología de la industria alimentaria, 2010, 31 (3): 285-287.
[21]Jia Yanju, Zhang Can. Estudio sobre la extracción del pigmento de la escamas de pescado por el método de microondas [J]. Anhui Agricultural Science, 2010, 38 (8): 3900-3901
[22] Chen Zhiqiang, Jin Yang, Ren Lu. Separación y purificación de astaxantina mediante resina macroporosa en medios no acuosos [J]. Bioprocess Engineering, 2009, 7(3): 39-42.
[23] Ding J. separación y purificación del pigmento rojo morera por resina macroporab-8 [J]. Anhui Agricultural Science Bulletin, 2009, 15(15): 216-218.
[24] Xu Y. materiales de membrana polimérica [M]. Beijing: Chemical Industry Press, 2005.
[25] Li Yuanyuan, Gao Yanxiang. Estudio sobre la purificación del pigmento amarillo gardenia mediante tecnología de separación por membrana [J]. Food Science, 2006, 27 (6): 113-117.
[26] Guo Hong. Estudio sobre la purificación y concentración de color natural comestimediante tecnología de separación por membrana [C]. Beijing Food Science Society Youth Science and Technology Paper Collection, 1992: 45-65.
[27] Lv Xiaoling, Yao Zhongming, Jiang Pingping. Estudio sobre la purificación del pigmento amarillo gardenia mediante cromatoen gel [J]. Food and fermentación Industry, 2001, 27 (4): 39-42.
[28]Fischer W, Bethge D. Destilación de sendero corto [J]. Absorción de destilación, 1992, 128: 403-414.
[29] Batistella C B, Wolf Maciel M R. recuperación de carotenoides de aceite de palma por destilación molecular [J]. Computer Chem (en inglés). Engng, 1998 (22): 53-60.
[30] Zhong G, Wu Y X, Zeng E K. un nuevo proceso para la extracción de carotenoides naturales [J]. Sichuan Daily Chemical, 1995 (3): 6-9.
[31]Batistella C B, Morase E B, Maciel F R, et al. Proceso de destilación Molecular para la recuperación de carotenoides y aceite de palma [J]. Applied Biochemistry Biotechnology, 2002 (98): 1149-1159.
[32] Shan Fang, Tian Zhifang, Bian Junsheng, et al. Aplicación de la tecnología de destilación molecular en el proceso de refindel pimrojo [J]. Chinese Journal of Food Science, 2003 (suplemento): 144-147.
-
anterior
¿Para qué sirve el color Natural?
-
siguiente
Estudio sobre el desarrollo de pigmentos naturales y colorantes naturales


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




