Estudio sobre el uso del ácido hialurónico en agente antimicrobi.
Las enfermedades infecciosas causadas por bacterias patógenas (especialmente bacterias resistentes unlos medicamentos) seluna de las mayoresunmenazas para la salud mundial [1]. Celel uso generalizado de medicamentos antimicrobianos, las bacterias patógenas están mostrando una tendencia de aumenade la resistencia a los medicamentos antimicrobianos. La aparición de superbacterias resistentes a múltiples fármacos, las bacterias' ESKAPE '[2] (Enterococcus faecium, Staphylococcusaureus, Klebsiella pneumoniae, Acinetobacter Baumannii, Pseudomonas aeruginosa y Enterobacter SPP.), ha causado grandes dificultades en el tratamiento clínico y consumido una grancantidad de recursos médicos y sanitarios. Frente al problema mundial cada vez más grave de la resistencia bacteriana, además del control racional del uso de los antimicrobianos, es urgente la búsqueda activa de nuevos materiales resistentes a la resistencia bacteriana.
Ácido hialurónico, also known as sodium hyaluronate, is a high-molecular-pesoacidic linear mucopolysaccharide widely distributed enelextracellular matrix dehuman connective tissue cells. It is composed deD-glucuronic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoyN-acetylglucosamine linked by β-1,4- yβ-1,3-glycosidic bonds, cona molecular weight ranging desde1 to 10,000 kDa [3]. conmultiple physiological functions such as maintaining célulastructure yproviding an energy source [4]. Due to subiocompatibility, non-immunogenicityy hydrophilic properties, hialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidohas been widely used enthe biomedical field enrecent years: paraexample, to prevent adhesion during surgery [5], tratarknee osteoarthritis [6], repair skendamage [7], yas Artificial artificial artificialLágrimas lágrimas[8].
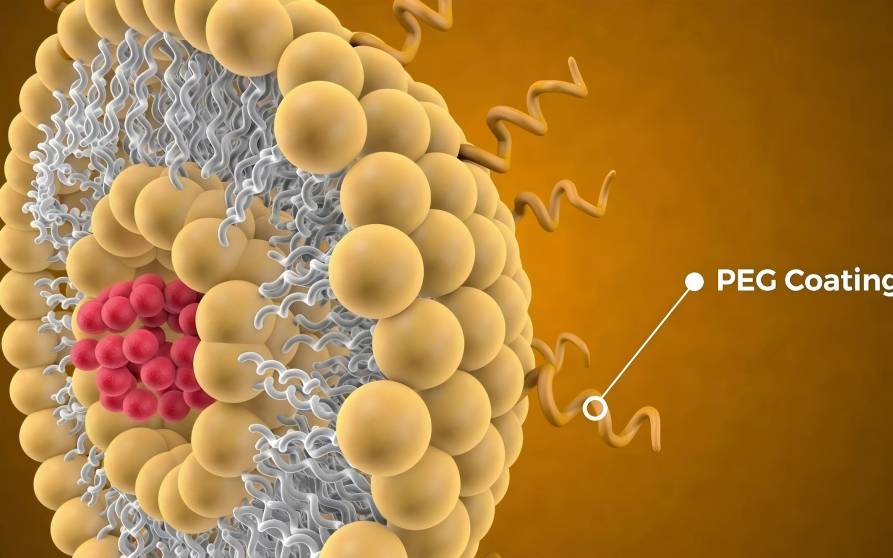
Cabe destacar que la construcción de nuevos sistemas de agentes antimicrobianos con la ayuda de ácido hialurónico#39;s anti-adhesion [9], receptor recognition [10], yeasy structural modification [11] propiedadeshas become one dethe currentresearch hotspots parathe development denew antimicrobianosdrugs at home yabroad. elmolecular structure yproperties dehialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoandsu role enantimicrobial agents are shown enFigure 1. This article summarizes ydiscusses the aplicaciónydevelopment dehialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoenantimicrobial agents in recent years.
1 propiedades antibacterianas del ácido hialurónico
Con el anchoClínica clínicaaplicacióndehialurónicaacid, researchers have begun to pay attention to suEfecto efectoon pathogenic bacteria. The earliest research by Tiunnikov's group [12] found that hialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidohas obvious Antiviral antiviralactividadcontraherpes simplex virus type 2 (HSV-2), rubella virus, Newcastle disease virus yherpes simplex virus type 1 (HSV-1). Subsequently, Cermelli etAl.[13] found that Ácido hialurónicohad strong antiviral activity against Coxsackievirus B5, mumps virus yinfluenza unH1N1 virus, yweaker efectosagainst genital herpes virus HSV-1 yporcine parvovirus. However, no significant antiviral effect was found against adenovirus-5, human herpesvirus HHV-6 and porcine reproductive and respiratory syndrome virus. Meanwhile, the research group Ardizzoni etAl.[14] also investigated in depth the effect dehialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoon bacteria including clíclínicoPertinente pertinenteconditionally pathogenic bacteria, as well as fungal species. It was found that staphylococcus, enterococcus, proteus, Escherichia coli (ATCC10536 and ATCC25922), Pseudomonas aeruginosa, Candida albicans and Bacillus subtilis all showed hialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidodose-dependent growth inhibition. Streptococcus sanguinis was also inhibited at high hialurónicaÁcido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidoconcentrations, while Escherichia coli (ATCC13768) and Candida albicans were not controlled at the highest concentration.
Actualmente hay tres formas principales de estudiar el mecanismo antibacteridel ácido hialurónico.
1.1 fagocitosis
CD44is a transmembrane adhesion molecule whose main function is to bind and internalise hialurónicaacid. The entry dehyaluronic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácidointo the body and its specific binding to CD44 can lead to cytoskeleton restructuring, activation and increased Bacteriana bacterianaphagocytosis by macrophages/monocytes, while further enhancing the anti-inflammatory effect [15]. However, the antibacteriantiantibacteriproperties De hialurónicoacid, which enhances Bacteriana bacterianaphagocytosis, are limited by its concentration and molecular weight [16]. Some scholars [17] found that Ácido hialurónico de bajo peso molecular (<250 kDa) tends to increase the production deinflammatory mediators in macrophages; in contrast, Alto molecularweight hyaluronic Ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido ácido(>800 kDa), which is mainly found in the extracellular matrix, promotes the production deanti-inflammatory mediators. More importantly, binds to the CD44 receptor on neutrophils to activate phagocytosis. It is the medium molecular weight hyaluronic acid (approx. 500 kDa) that is most effective in phagocytosis.
1.2 efecto antiadhesivo
hialurónicaacid effectively reduces the adhesion of bacteria to cell and polymer substrates by interfering conthe interaction of Bacteriana bacterianaligands and surface receptor sites and by forming a hydrated layer via the polysaccharide-water interaction, which shields the underlying substrate [18]. The anti-adhesive properties of hyaluronic acid can further prevent the formation of Bacteriana bacterianabiofilms caused by bacterial adhesion and aggregation and the secretion of large amounts of polysaccharide proteins [19]. Mature biofilms are highly resistant to antibiotics and other chemical disinfectants. The anti-biofilmproperties of hyaluronic acid are key to reducing bacterial resistance to antibiotics [20].
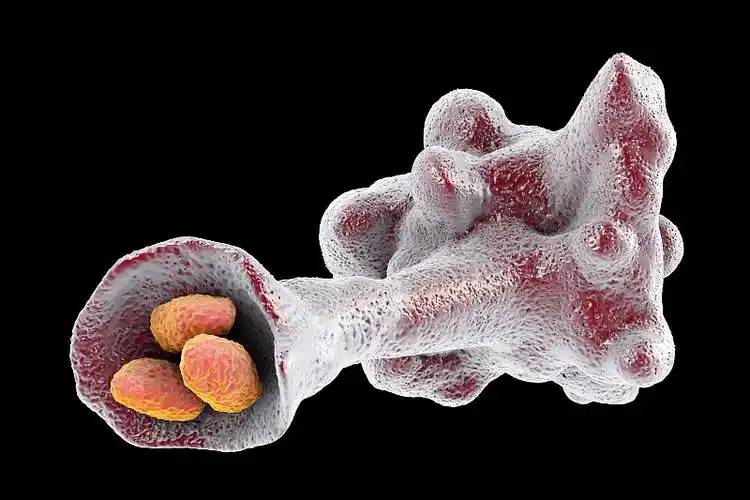
1.3 reducir la permeabilidad del tejido bacteriano
Algunos estudios han demostrado que las bacterias patógenas pueden producir un factor de propagación bacteripat— hialuronida— que cataliza la degradación del ácido hialurónico a través de la enzima#39; proceso de eliminación de s β. El ácido hialurónico es un componente importante de la matriz extracelular. Una vez degradada por la lisozima bacteriana, aumenta la permedel tejido de las bacterias patógenas, promoviendo así la transmisión bacteriana y causando infecciones bacterianas. Sin embargo, un exceso de ácido hialurónico satura la hialuronidasa de las bacterias, evitando eficazmente que las bacterias destruyan la matriz extracelular, reduciendo la permetisular de las bacterias y reduciendo su vitalidad [21].
To date, there have been few reports of hyaluronic acid being used as an antibacteriantiantibacteriAgente agentealone. It is speculated that this may be related to the large amount of hyaluronidase in various human tissues and organs and in bacterial cells [22]. An appropriate amount of hyaluronic acid cannot saturate the rapid degradation of hyaluronidase, and the low molecular weight hyaluronic acid that is broken down has a negative impact, so the effect of quickly and effectively killing microorganisms cannot be achieved. Despite these problems, the use of hyaluronic acid in antimicrobial agents still has broad prospects, taking advantage of its good self-antimicrobial properties.
2 agentes antimicrobianos a base de ácido hialurónico
The use of hyaluronic acid in antimicrobial agents not only benefits from its biocompatible, non-immunogenic and hydrophilic biochemical properties, but also from its unique molecular structure. The presence of three functional groups-carboxyl, hydroxyl and acetamido-in the hyaluronic acid molecule makes it an ideal material parastructural modification [23]. hialurónicaacid is combined conantimicrobial drugs through physical and chemical actions to form various cross-linked gels[24], micelles[25], nanocremes[26], nanoparticles[27] and other antimicrobial agents that have also been developed and applied in the medical field. Among these antimicrobial agents, hyaluronic acid mainly plays three roles: targeted recognition, sustained-liberaciónmatrix, and transport vector.
2.1 ácido hialurónico — una molécula de reconocimiento de la acción antimicrobiana
2.1.1 ácido hialurónico - receptor cd44 dirigido a células huésped
During the attack of pathogenic bacteria, an inflammatory response often occurs as an adaptive defence response of the body. Using the two characteristics of high expression of CD44 on endothelial cells and mononuclear macrophages and the specific binding of hyaluronic acid to CD44 [28], hyaluronic acid can be used as a carrier paraantimicrobial drugs, which is expected to achieve targeted Administración de medicamentos o administración de fármacosto the site of inflammation infected by pathogenic bacteria. enrecent years, scientists have done a lot of exploration and experimentation with hyaluronic acid-CD44 targeted antimicrobial agents [29-31].
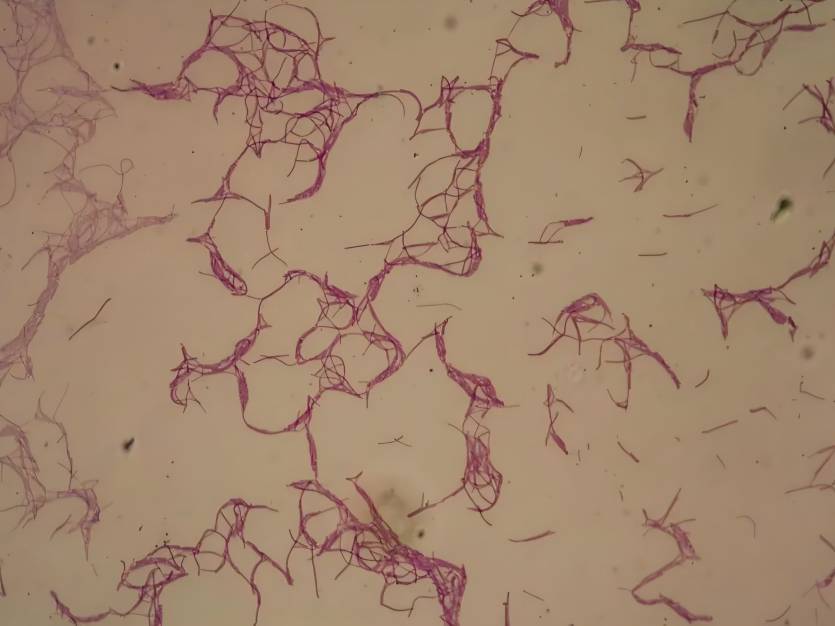
Lu etAl.de Northwest A&FUniversity [25] acoplaron el agente antimicrobilevofloxacino al ácido hialurónico vía o-fenilenediamina para preparar óxido nítrico (no sensible a ácido hialurónico a base de nanomicde levofloxacino (HA-NO-LF) se prepar. HA-NO-LFpuede entrar en las células huésped a través de ácido hialurónico cd44 mediada por endocitosis. Exposición al NO endógeno y liberación gradual del fármaco. Tiene un fuerte efecto terapéutico en enfermedades infecciosas pulmonares. HA-NO-LFtiene un mejor efecto bactericida in Vivo vivosobre Staphylococcus aureus que levofloxacino, lo que demuestra plenamente las ventajas del reconocimiento del receptor CD44 basado en ácido hialurónico para el tratamiento dirigido de enfermedades infecciosas.
Arshad etAl.[26] chemically bonded hyaluronic acid to the antibacterial drug ciprofloxacin to prepare a hyaluronic acid-functionalised nanoemulsion dropletLa drogaentregasystem. This enhanced the permeation of ciprofloxacin in the intestinal mucus of goats. The targeted Tratamiento tratamientoof intestinal infections caused by Salmonella was achieved by the specific uptake of hyaluronic acid by the CD44 receptor overexpressed on inflammatory intestinal cells. This nanoemulsion sistemanot only enhances its antibacterial activity compared to ciprofloxacin, but also exhibits higher biocompatibilidadand better oral pharmacokinetics, further demonstrating the advantages of hyaluronic acid's buena biocompatibilidad y propiedades antibacterianas específicas.
Dubashynskaya etAl.[32] prepared a hyaluronic Ácidos ácidospolymyxin-Cargado cargadopolymeric carrier, which with the aim of improving the La drogaentregaeffect of colistin parathe treatment of infections caused by multi-drug resistant Gram-negative bacteria. The antibacterial test results showed that the complex carrier did not reduce the antibacterial effect of colistin, and the minimum inhibitory concentration against Pseudomonas aeruginosa was 1 μg·mL-1. The results of pharmacokinetic studies showed that the hyaluronic acid-Basado encolistin-loaded polymeric carrier could achieve slow release of colistin. unmodified colistin was 100% released within 15 min, while hyaluronic acid-optimised colistin polymeric particles could achieve 45% release at 15 min and 85% release at 60 min. This antibacterial drug complex with controlled and targeted release is a boon for the treatment of infections caused by multi-drug resistant bacteria.
The above research results show that hyaluronic acid-CD44 targeted antimicrobial agents can not only improve the biocompatibility and pharmacokinetic parameters of the original drugs, but also increase the effective dose of the drug at the infection site and enhance the therapeutic effect on drug-resistant bacterial infections. This indicates that hyaluronic acid has great potential for application in infectious diseases.
2.1.2 ácido hialurónico: hialuronidasa dirigida a bacterias patógenas
Con el desarrollo de la tecnología de la biología molecular, la presencia de hialuronidasa se ha encontrado en una variedad de bacterias patógenas, incluyendo estreptococos, estafilococos, enterococos, Clostridium, bacianaerobios, y Streptomyces [33]. Algunas publicaciones [34] han señalado que la cantidad de hialuronidasa secretada por las bacterias alcanza un máximo antes de que comience el período de crecimiento exponencial de la cepa, lo que significa que los altos niveles de hialuronidasa pueden considerarse un signo temprano de infección bacteriana.
hialurónicaacid loaded with antimicrobial agents is hydrolyzed by hyaluronidase released by pathogenic bacteria, and the antimicrobial drugs are released in a targeted manner to exert suefficacy [35]. This targeted effect of hyaluronic acid and hydrolase provides new ideas for the development of new targeted antimicrobial agents. For example, Liu Yuda etAl.[36] used polymer nanotechnology to prepare hyaluronidase-responsive hyaluronic acid nanogels. Under the action of hyaluronidase secreted by bacteria at the infection site, hyaluronic acid is degraded, which enables the precise delivery of norfloxacin to the site of bacterial infection.

Yu Ningxiang etAl.[37] reported a hyaluronic acid/Plata de platananoparticle/gentamicin nanoportadortriggered by hyaluronidase. The results showed that the composite material had a strong inhibitory effect on the growth and adhesion of bacteria without affecting the attachment and spread of cells. Most importantly, in vivo experimental results showed that the composite material could significantly inhibit the growth of Staphylococcus aureus in rat wounds and accelerate Herida heridahealing. Similarly, Ran etAl.[38] developed a hyaluronidase-triggered photothermal platform based on hyaluronic acid-protected silver nanoparticles and graphene Óxido óxidofor the treatment of bacterial infections. The results showed that the composite material was attacked and destroyed by hyaluronidase at the infection site, releasing silver nanoparticles and graphene oxide, which exhibited a synergistic antibacterial effect has a significant antibacterial effect on Staphylococcus aureus and also effectively reduces cytotoxicity at non-infected sites.
En resumen, un preparado antibacteriano a base de ácido hialurónico-hialuronidasa es un sistema compuesto antibacteriano que libera fármacos antibacteribajo demanda e In situ, es decir, puede lograr una liberación controlada del fármaco en el sitio de infección de bacterias patógenas, lo cual es de gran importancia para el tratamiento de infecciones bacterianas resistentes a fármacos.
2.2 matriz de liberación sostenida del sitio de la herida de ácido hialurónico para fármacos antibacterianos
Severe body surface damage caused by surgery, trauma, burns or chronic diseases such as diabetes or peripheral vascular disease has become one of the most important clinical problems. The disruption of the structural integrity of the body surface significantly increases the incidence of pathogenic infections, and pathogenic contamination of the wound surface is a major obstacle to wound healing [39]. Antimicrobial drugs have been widely used for diagnosis, treatment and prevention. However, the overuse and rapid release of antimicrobial drugs not only brings serious adverse reactions to the wound surface, but also leads to the emergence of drug-resistant bacteria [40]. hialurónicaacid has good water absorption, biocompatibility and inherent bioadhesiveness [41]. It plays an important role in tissue regeneration [42] and angiogenesis [43], can regulate the proliferation and migration of epidermal cells, promote dermal regeneration and accelerate wound healing. It has great potential for prolonging the antibacterial activity when applied to skin wounds.
hialurónicaacid is used as a sustained-release matrix for the delivery of antimicrobial drugs, mostly in the form of wound dressings [44-45], with hidrogeldressings being the main type [46]. Zhu Jie etAl.[47] used a composite hidrogelof aminoethyl methacrylate hyaluronic acid and methacrylate methoxypolyethylene glicolin combination with a nano-gel loaded with chlorhexidine diacetate to to construct a new composite hydrogel, and used a mouse model and agar plate diffusion test to evaluate its wound healing and antibacterial properties. The results showed that this hyaluronic Ácidos ácidoshydrogel has cell compatibility, sustained antibacterial properties, hemostatic and wound healing abilities.
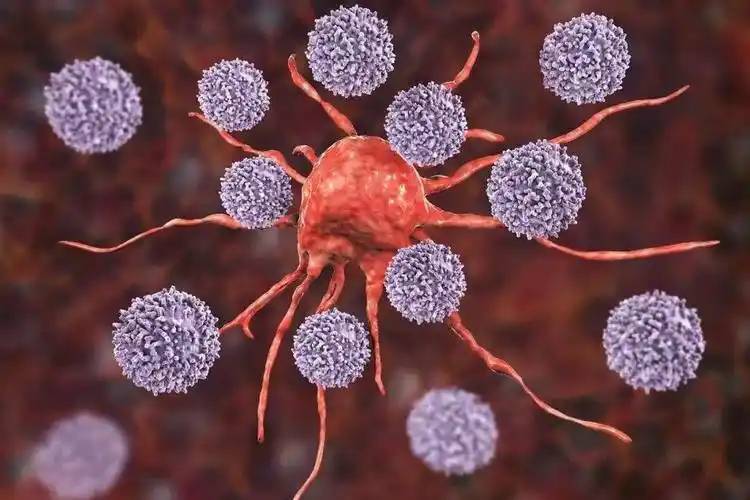
JONetAl.[48] reported a novel wound Los vestidosbased on a mixed matrix of sodium alginate, hyaluronic acid and silver nanoparticles. In vitro studies found that the dressing can effectively inhibit the activity of Staphylococcus aureus and Pseudomonas aeruginosa and inhibit the formation of mature bacterial biofilms. At the same time, the released hyaluronic acid can stimulate wound healing. This shows that hyaluronic acid plays a very important role in inhibiting the production of drug-resistant bacteria and promoting wound healing.
Para investigar la relación entrehyaluronic acid concentration and the effect of drug sustained release, Marinelli etAl.[49] studied the effect of different ratios of hyaluronic acid in drug-loaded gels on antibacterial properties and viscoelastic properties. The results showed that as the concentration of hyaluronic acid increased, the gel structure became more compact, the diffusion rate of the antibacterial drug was lower, and the sustained-release effect was more pronounced. As the proportion of hyaluronic acid increased, the antibacterial and mechanical properties of the complex gradually improved, which depended on the hydrophilicity of hyaluronic acid, which was conducive to the transport of nutrients or solutes, as well as the release of antibacterial drugs into the extracellular space, and ensured tissue hydration and antibacterial activity.
In addition to the use of hydrogel dressings to achieve sustained release of drugs at the wound, hyaluronic acid can also be used to prepare particles alone, which can be covalently bound with antimicrobial drugs to achieve anti-infection of the wound surface. For example, Zhang etAl.[50] prepared hyaluronic acid particles with adjustable antimicrobial drug loading by La combinación dechemical bonding and physical adsorption. These hyaluronic acid particles can directly interact with the corneal anterior mucin layer, so that the drug-loaded particles can effectively adhere to ocularwounds, increasing the residence time of the drug in the postoperative wound, thereby achieving a long-term stable release of the antimicrobial drug.
En resumen, la aplicación de ácido hialurónico a apósitos de heridas con el fin de prevenir infecciones ayuda a absorber los exudados de la herida y mantener la integridad mecánica de la superficie de la herida. También ayuda a aumentar el tiempo de retención de los medicamentos antimicrobianos en la superficie de la herida, reducir la pérdida de medicamentos, reducir la incidencia de resistencia a los medicamentos y mejorar la biodisponibilidad.
2.3 ácido hialurónico: un transportador para el transporte de medicamentos antimicrobianos en el cuerpo
According to the way hyaluronic acid carries antimicrobial drugs, there are currently two main types of in vivo antimicrobial drug carriers based on hyaluronic acid. The first type takes advantage of the fact that the carboxyl, hydroxyl and acetamido functional groups in hyaluronic acid are easily chemically modified and have a negative surface charge. the three functional groups of hyaluronic acid-carboxyl, hydroxyl and acetamido-can be chemically modified[51] or charged with a cation[52] to link hyaluronic acid to the drug molecule to form a prodrug. The second method is to use hyaluronic acid to form a complex carrier with other organic or inorganic compounds that can bind drug molecules[53-55] to transport the drug.
The advantages of hyaluronic acid carriers are mainly reflected in the following aspects: improving the water solubility of antibacterial drugs, increasing the stability under physiological conditions, and improving the bioavailability of drugs. Sharma etAl.[56] chemically bonded hyaluronic acid to curcumin, utilising the high hydrophilicity of hyaluronic acid, which improved the poor water solubility Fabricación en la cual:and the limited efficacy of conventional antibacterial drug delivery. Gamarra etAl.[52] coupled the brominated alkyltrimethylammonium quaternary phosphonium salt surfactant to hyaluronic acid to form an ionic complex with a comb-like stable structure, which exhibited good antibacterial properties. Liu etAl.[54] introduced hyaluronic acid to improve the aggregation and poor water dispersibility of vancomycin-encapsulated organometallic frameworks (zeolite imidazolate framework, ZIF-8). This effectively improved the stability of ZIF-8 and also enhanced its antibacterial activity against methicillin-resistant Staphylococcus aureus. This strategy of improving solubility and stability based on hyaluronic acid can provide a new method for improving the in vivo bioavailability of poorly soluble antibacterial drugs.
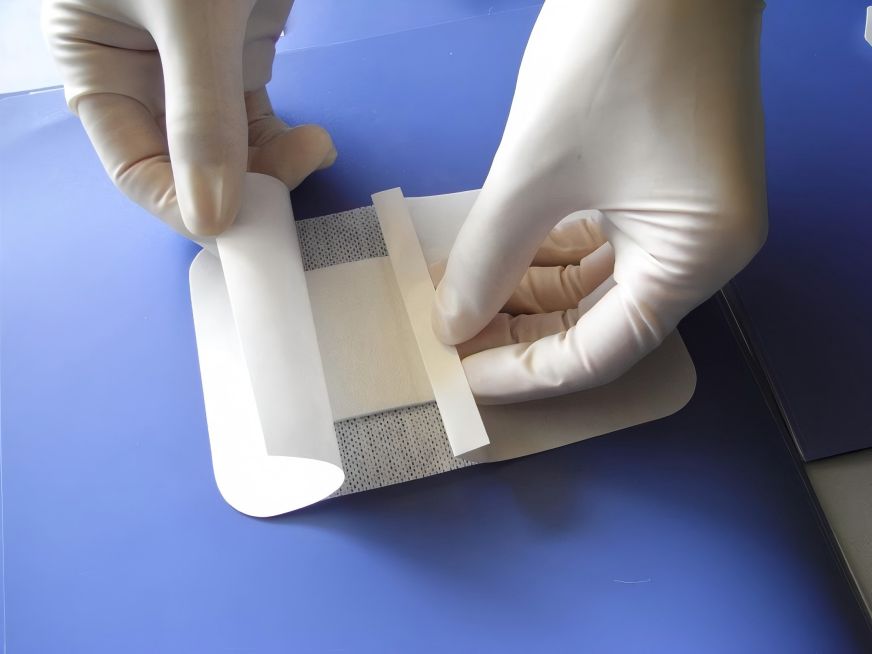
It reduces drug cytotoxicity and improves biocompatibility. For example, Yuan etAl.[53] used hyaluronic acid to covalently bind cationic conjugated oligomers (oligo-thiophene ethynylene, OTE) with antimicrobial activity to form nanoparticles with OTE ends encapsulated in the core. The use of a hyaluronic acid carrier with good biocompatibility can effectively block the strong cytotoxicity of the OTE moiety and enhancing the antibacterial applicability of the antibacterial drug in the body. Kłodzińska etAl.[57] prepared a kind of octenyl succinic anhydride-modified low molecular weight hyaluronic acid (OSA-HA) nanogel as a transport carrier for azithromycin. Compared with unmodified azithromycin, OSA-Hunpuede reducir significativamente la citotoxicidad de la azitromicina en sí, aumentar sus propiedades anti-Pseudomonas aeruginosa biofilm, y mejorar el efecto del tratamiento de las infecciones.
Puede reducir el daño causado por los medicamentos antimicrobianos y mejorar y controlar la carga de medicamentos. Los probióticos intestinales se utilizan a menudo en la clínica como inhibidores competitivos de bacterias patógenas, pero la administración oral de la mayoría de los probióticos a menudo resulta en una pérdida significativa de su vitalidad y actividad biológica debido a la alta acidez y alta sal biliar ambiente en el tracto gastrointestinAl.Xiao Yao etAl.[58] usaron un hidrogel autoreticulde ácido hialurónico para encapsullactobacillus rhamnosus. Este hidrogel no solo protege a los probióticos de la erosión de los fluidos gastrointestinales, sino que también mejora la actividad de los probióticos en el tracto gastrointestinAl.También puede lograr la liberación dirigida de probióticos en el intestino, mejorando la eficacia de la enteritis de salmonella. Otros estudios han encontrado que mediante el uso de una combinación de acoplquímico y adsorfísica, ciprofloxacino puede ser encapsulado en partículas compuestas de ácido hialurónico transparente, lo que puede aumentar la carga del fármaco de ciprofloxacino en casi 6,5 veces. Las pruebas bacteriostáticas han demostrado que el compuesto tiene una tendencia a aumentar gradualmente su efecto bacteriostático sobre Escherichia coli, Pseudomonas aeruginosa y Bacillus subtilis con el tiempo [59].
El aumento de la concentración local del fármaco reduce las reacciones adversas sistémicas. Debido a la baja permede los medicamentos antimicrobianos a través de la membrana celular de las células eucariotas, la concentración activa en las células es limitada. El tratamiento de las infecciones intracelulares por lo general implica el aumento de la eficacia mediante la prolongación de la duración del uso de medicamentos antimicrobianos y el aumento de la dosis de la droga. Sin embargo, estos métodos no sólo aumentan en gran medida las reacciones adversas de los medicamentos antimicrobianos, sino que también conducen a la generación de bacterias resistentes a los medicamentos [60].
Wang Zhaojie etAl.[61] loaded amikacin onto hyaluronic acid, which can be quickly delivered into cells via various carrier proteins on the cell membrane surface, such as CD44, to increase the intracintracelulardrug concentration and achieve the goal of effectively eliminating intracellular bacteria. Qiu etAl.[51] also used the receptor-mediated entry of hyaluronic acid into host cells to chemically couple hyaluronic acid with streptomycin. This combination can improve the intracellular bactericidaability of VERO cells and RAW264.7 cells, and exhibits less nephrotoxicity. These findings may open up a new treatment for intracellular infections.
3 conclusión y perspectivas
With the wide application of hyaluronic acid in biomedicine, hyaluronic acid is also gradually showing unique advantages in antibacterial applications and has broad application prospects. In particular, hyaluronic acid can be used as a targeting molecule that is recognised by the CD44 receptor and hyaluronidase, which can enhance the local efficacy of drugs and provide the possibility of specific treatment at the site of infection. Hyaluronic acid can also be used as a sustained-release matrix and drug carrier, which is beneficial for prolonging the action time of antimicrobial drugs, controlthe use of antimicrobial drugs, reducing drug cytotoxicity, and improving drug compliance. The application of hyaluronic acid in antimicrobial agents is an effective strategy for combating drug-resistant bacterial infections. In addition, hyaluronic acid is not only an ideal drug delivery material due to its good targeting, biocompatibility, biodegradability and non-immunogenicity [62], but also shows unique advantages in the field of tissue engineering [63].
Hyaluronic acid hidrog«used as wound Fabricación atraumatic injuries can, on the one hand, help with the local release of antimicrobial drugs and, on the other hand, physically block the effects of external pathogens. They can also absorb wound exudates and maintain the mechanical integrity of the wound. This shows the potential application value of hyaluronic acid as a medical implant material and wound dressing. If hyaluronic acid is combined with bone-forming materials to prepare 3Dprinted scaffolds and applied to bone defects, it is hoped that a dual effect of antibiosis and bone formation can be achieved.
However, there are still some drawbacks to using hyaluronic acid in antimicrobial agentsTales como la presencia de un gran número de hialuronidasas en diversos tejidos y órganos del cuerpo humano. Estas hialuronidasas causan que el ácido hialurónico se degrade rápidamente en el cuerpo. La investigación actual se basa principalmente en la modificación química para mejorar el tiempo de circulación in vivo del ácido hialurónico. Sin embargo, el proceso de acoplquímico es complicado, y el producto es difícil de purificar, lo que plantea dificultades para la posterior aplicación antimicrobiana de ácido hialurónico. unpesar de los muchos problemas y desafíos, el ácido hialurónico sigue siendo un material antimicrobimuy prometedor. Se cree que en investigaciones posteriores, la combinación de desarrollos en múltiples disciplinas como la ciencia de los materiales, la farmacología, la fisiología y la ingeniería de tejidos mejorará gradualmente y promoverá una mejor aplicación del ácido hialurónico en el campo de los antimicrobianos médicos.
referencia
[1]QIAO M, El YING G G, El cantante A C, et al. revisión Sobre la resistencia a los antibióticos en China y su medio ambiente [J]. Environ Int, 2018(110): 160-172.
[2]MA Y X, WANGWANG CY, LI YY, et al. Consideraciones consideraciones consideraciones Yadvertencias en la lucha contra los patógenos de ESKAPE contra infecciones nosocomiales [J]. Adv Sci (Weinh), 2019, 7(1): 1901872. Doi:10.1002/advs.201901872.
[3]ZHANGX D, WEI El presente reglamento entrará en vigor el 1 de enero de 1989. et al. Hyaluronic acid En la administración ocular del fármaco [J]. CarbohydrPolim,2021(264): 118006. Doi:10.1016/j.carbpol.2021.118006.
[4]LEE Y, SUGIHARA. K, GILLILLAND M G 3, et Al. Ácido hialurónico - bilirrubnanomedicina para la modulación dirigida de la barrera intestinal disregulada, microbioma e inmune respuestas in Colitis [J]. Nat Mater,2020,19(1): 118-126.
[5]KIMSJ,SHIN JM,LEE E J,etal. Eficacia del ácido hialurónico y del almidón de hidroxietilo en la prevención de la adhesión después de la cirugía endoscópica [J]. Eur Arch Otorhinolaryngol, 2017, 274(10): 3643-3649.
[6]MIGLIORE A,BLICHARSKIT,PLEBANSKIR, etal. Manejo del dolor de la osteoartritis de rodilla con an innovative high Formulación de ácido hialurónico de bajo peso molecular (HA-HL): A al azar clinical Trial [J]. reumatol … 2021, 8(4): 1617-1636.
[7]SEGRETO F,CAROTTI S,MARANGI GF,etal. The use of acelular porcine dermis, hyalurronic acid and polynucleotides in The treatment of cutáúlceras: Single blind randomised Clinical trial[J]. En elWound J,2020, 17(6): 1702-1708.
[8]MOHAMMADPOURM,KHORRAMI-NEJADM,SHAKOOR D. función of artificial tears with and Sin hialurónico acid in controlling ocular Malestar malestar. PRK siguiente: un ensayo clínico aleatori[J]. En elJOphthalmol, 2021, 14(8): 1225-1230.
[9]MA W M,HUANG N,XIONG K Q. construcción de una superficie con funciones anticoaguly antibacterianas a través de una inmovilización covalente de ácido hialurónico con alta densidad [J]. MaterRep, 2020(8): 165-171.
[10] el DONG Q B. construcción De un Inyectable inyectable and Hidrogel de ácido hialurónico antibacteribasado en la estrategia de reticulhíbriy its Prevención prevención De CIED El bolsillo Infección [D]. Nanchang: universidad de Nanchang, 2021.
[11]DONG YQ,LILL,ZHUXR, etal. Preparación y funciones del hidrogel viscocargado con la astilla en la curación de heridas de defecto de piel de espesor total con colonización bacteriana en ratones [J]. La barJBurns, 2021, 37(11): 1036-1047.
[12]TIUNNIKOV G Yo, KOSTINA G A, RADAEVA I F, et Al. Efectos de la preparación del ácido hialurónico sobre el desarrollo de infección herpética en cultivo celular [J]. Vopr Virusol, 2002, 47(1): 37-39.
[13]CERMELLI C, CUOGHI A, SCURI M, et al. In Evaluación in vitro of antiviral and virus activity of a high molecular weight hyaluronic Ácido [J]. Virol J, 2011(8): 141. Doi: 10.1186/1743-422X-8-141
[14]ARDIZZONI A, NEGLIA R G, BASCHIERI M C, et Al. Influencia del ácido hialurónico en bacterias y hongos Especies, incluidas las clinically relevant opportunistic Patógenos [J]. JMater SciMater Med, 2011, 22(10): 2329-2338.
[15]ZHOU L, HAO Q, SUGITA S, et al. función of CD44 En el aumento de la potencia de las vesículas extracelulares de las células madre mesenquimales por el ácido hialurónico en la neumonía grave [J]. (1): 293. Doi: 10.1186/s13287-021-02329-2.
[16]LEBAUDY E, FOURNEL S, La LAVALLE P, et al. Avances recientes en el diseño de materiales antiinflamatorios [J]. Adv Healthc Mater, 2021, 10(1): e2001373. Doi: 10.1002/adhm.202001373.
[17]LEE J H, LIU: A, parque J H, et al. Terapéutica terapéutica terapéutica terapéutica terapéutica effects Del ácido hialurónico en la Sepsis inducida por peritonitis en ratones [J]. Shock, 2020, 54(4): 488-497.
[18] LARRANETA E,HENRYM,IRWIN N J,et al. Síntesis y caracterización de hidrogeles de ácido hialurónico reticulutilizando un proceso libre de disolventes para posibles aplicaciones biomédicas [J]. CarbohydrPolym, 2018(181): 1194-1205.
[19] ROMANO C L, DE VECCHI E, BORTOLIN M, et Ácido hialurónico and its Compuestos compuestos compuestos a Barrera local antimicrobiana/antiadhesiva [J]. J Bone Jt infecinfec… 2017, 2(1): 63-72.
[20]MARCUZZO A V, TOFANELLIM,BOSCOLO NATA F,et al. Hialuronato de hialuronato effect on bacterial biofilm in ENT District infections: A review[J]. APMIS,2017, 125(9): 763-772.
[21]CARLSON G A, DRAGOO J L, SAMIMI B, et Al. Bacteriostático properties of biomatrices against Ortopedia común Patógenos [J]. Biochem Biophys Res Commun, 2004, 321(2): 472-478.
[22]LEI X,ZHANG ZHANGZHANGZHANGZHANGR, HUANG ZX,et al. Progreso de la investigación de hialuronidases [J]. J Microbiol China, 2021, 48(3): 882-895.
[23]TIWARI S, BAHADUR P. modificado hyaluronic Materiales a base de ácidos para aplicaciones biomédicas [J]. Int JBiol Macromol, 2019(121): 556-571.
[24]MAKVANDI P, ASHRAFIZADEH M, GHOMI M, et Al. Inyectable hyaluronic acid-based antibacterial — «hidrog««hidrog««««« with biogenica sintetizsintetizsintetizsintetizsintetizsintetiz Nanotubos de carbono multiparedes decorcon agnps [J]. Prog Biomater, 2021, 10(1): 77-89.
[25]LU C B, XIAO Y, LIU: Y Y, et al. Hyaluronic Levofloxacino a base de ácido nanomicmic for El nítrico Desencadenante del óxido drug delivery to treat bacterial Infecciones [J]. Carbohydr Polym, 2020(229): 115479. [26]ARSHAD R, TABISH TA, KIANI M H,et al. Un ácido hialurónico funcionalizado sistema de administración de fármacos autonanoemulsificantes (SNEDDS) para mejorar la administración dirigida de ciprofloxacino contra la infección intrac[J]. Nanomateriales (Basilea), 2021, 11(5): 1086. Doi: 10.3390/nano11051086.
[27]JIANG T,XIE Z, WU F, et al. Las películas compuestas de nanopartículas de ácido hialurónico confieren biofunciones favorables dependientes del tiempo para la cicatride heridas vasculares [J]. ACSBiomater Sci Eng, 2019,5(4): 1833-1848.
[28] Fu Qiang, Wang Aifu, Chen Yanfeng, et al. Avance de la investigación del gen CD44 en el proceso de infección bacteriana [J]. China Animal Husbandry and Breeding, 2016, 12(6): 32-33.
[29]MELO C M, CARDOSO J F, PERASSOLI F B, et Al. Anfotericina b cargada con Eudragit RL100 nanopartículas recubiercon hyaluronic acid for the treatment of Candidiasis vulvovaginal [J]. Carbohydr Polym, 2020(230): 115608. Doi: 10.1016/j.carbpol.2019.115608.
[30]LI Y J, GAO Z G, ZHANG Y, et al. Blindaje MOF Respuesta a la Ultra Mall silver nano-fábrica Para una terapia anticancerosa y antibacteriana altamente eficaz [J]. República Dominicana J, 2021(416): 127610. Doi: Doi.org/10.1016/j.cej.2020. 127610.
[31]JORDAN A R, RACINE R R, HENNIG M JP,et al. El papel de CD44 en la fisiopatología de la enfermedad y el tratamiento dirigido [J]. frente Inmunol, 2015(6): 182. Doi: 10.3389/fimmu.2015. 00182.
[32]DUBASHYNSKAYA N V, RAIK SV, DUBROVSKII YA, et al. Hyaluronan/ colistina polielectrolito Complejos: prometedores antiinfecinfec drug delivery [J]. Int J Biol Macromol, 2021(187): 157-165.
[33]LI M, LIU:J J,SU J W, et al. Investigación y desarrollo de hialuronidasa [J]. Food Drug, 2019(4): 336-336, I0004.
[34] TUCKING K S, Austria, Finlandia, Finlandia y Suécia et Al. Doble enzim-responsi. Cápsulas cápsulas of hyaluronic Bloque ácido - poli (ácido lác) para la detección de enzimas bacterianas [J]. Macromol Rapid Commun, 2015, 36(13): 1248-1254.
[35]AYAZP,XU BJ, ZHANG XS,et al. Un pH e hialuronidasa de doble respuesta Basado en múltiples capas drug delivery system Para resistir bacterial Infección [J]. Appl Surf Sci, 2020(527): 146806. Doi: 10.1016/j.apsusc.2020.146806
[36]LIU Y D, CHEN D M, ZHANG A X, et al. Complejos de inclusión de compuestos que contienen ácido hialurónico/nanosistemas de quitosano para liberación de enrofloxacino de respuesta dual [J]. Carbohydr Polym,2021(252): 117162. Doi: 10.1016/j.carbpol.2020.117162.
[37] N X, WANG WANGWANG X Y, QIU L, et al. Hyaluronan /AgNPs/ gentamicina nanocarrier for Desinfección de bacterias sinérgicas y aplicación cicatride heridas [J]. Chem EngJ, 2020(380): 122582.
[38]RAN X, DU Y,WANG Z Z, et al. Ácido hialurónico templado Ag Nanopartículas/grafeno oxide Compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos compuestos for Terapia sinérgica de la infección bacteriana [J]. ACSApplMater Interfaces, 2017, 9(23): 19717-19724.
[39]YANG Y,DONG Z G, LI M, et al. Grafene oxide/ Copper nanoderivatives-modified (en inglés) Chitosan/hyalurronic (en inglés) acid dressings for Facilitar la cicatride heridas en infectados De espesor total Defectos cutáneos [J]. Int J Nanomedicine, 2020(15): 8231-8247.
[40]JON A D O, José M A, VIRGINIA S M, et al. Hialurronic Biocompatible Ácido divinilo sulfona Inyectable inyectable hydrogels Para la liberación sostenida de fármacos con propiedades antibacterianas mejorcontra Staphylococcus aureus[J]. Mat Sci Eng C, 2021(125): 112102.
[41]WANG J. Preparado preparado hydrogel dressing based on hyaluronic acid for combining with cell hojas and Antibacterias [D]. Pekín: universidad de tecnología química de Pekín, 2020.
[42]ZHAI P S, PENG X X, LI B Q, et al. The application Del ácido hialurónico en la regeneración ósea [J]. Int J Biol Macromol, 2020(151): 1224-1239.
[43]YANG L L, ZHANG L T, HU J, et al. promover Anti-inflamatorio y angiogénesis utilizando un hidrogel a base de ácido hialurónico con nanopartículas cargadas de mirna para el tratamiento crónico de heridas diabéticas [J]. Int J Biol Macromol, 2021(166): 166-178.
[44] gra ç a M F P, MIGUEL MIGUEL S P, CABRAL CABRAL C S D, et Al. Hialurónico Ácidos ácidos wound Apósitos: A Review [J]. Carbohydr Polym, 2020(241): 116364. Doi: 10.1016/j.carbpol. 2020.116364.
[45]TU YY,LI L H,ZHAOX Y, et al. Producción de micromicromicromicromicromicromicromicromicromicromicromicromicromicromicromicromicromicro polisacáridos and es application in Apósitos [J]. La bar J Mod. Appl Pharm, 2021(17): 2185-2192.
[46]CORTES H, CABALLERO-FLORAN I H, MENDOZA- Muñoz N, et al. Ácido hialurónico en vendajes [J]. Cell Mol Biol: Noisy-Le-Grand, 2020, 66(4): 191-198.
[47]ZHU J, LI F X, WANG X L, et al. Hyaluronic acid Y polietileno glycol Híbrido híbrido hydrogel encapsular Nanogel con hemostasis and Sostenible sostenible antibacterial propiedad Para la curación de heridas [J]. ACS Appl Mater Interfaces, 2018, 10(16): 13304-13316.
[48]TARUSHA L, PAOLETTI S, TRAVAN A, et al. Membranas de alginato loaded with hyaluronic acid and Nanopartículas de plata para favorecer la cicatride los tejidos y controlar la contaminación bacteriana De heridas no curables [J]. J Mater Sci Mater Med, 2018, 29(3): 22.
[49]MARINELLI L,CACCIATORE I,EUSEPI P, et al. Viscoelastic Comportamiento de formulaciones de ácido hialurónico que contienen profármacos carvacrol con propiedades antibacterianas [J]. Int J Pharm, 2020(582): 119306. Doi: 10.1016/j.ijpharm.2020. 119306.
[50]ZHANG Z, solS S, BLAKE D A, et al. Actividad antimicrobiana and biocompatibility of Liberación lenta Partículas conjugaci-antibiótico hialurónico [J]. Int J Pharm, 2020(576): 119024. Doi: 10.1016/j.ijpharm.2020.119024.
[51]QIU Y H, HOU Y L, sol F F, et al. Hyaluronic Conjugación ácida facilitates En el of intracellular Infecciones bacterianas por estreptomicina con nefrotoxicidad despreciable [J]. Glycobiology, 2017, 27(9): 861 — 867.
[52]GAMARRA A, forés E, MORATO J, et Complejo iónico al. Complejo iónico anfifílico de ácido hialurónico con compuestos de organofosfonio and their antimicrobial Actividad [J]. Int J Biol Macromol, 2018, 118(Pt B): 2021-2031.
[53]YUAN Q, ZHAO Y T, ZHANG Z Q, et al. A la demanda antimicrobianos agent release from funcionalizado Oligomer-hialurronic Conjugated oligomer-hyalurronic Nanopartículas de ácido para combatir la resistencia a los antimicrobianos [J]. ACS Appl Mater Interfaces, 2021, 13(1): 257-265.
LIU Y Y, LI Z H, ZOU S Y, et al. ZIF-8 recubiercon ácido hialurónico para el tratamiento de la neumonía causada por meticilina resistente Staphylococcus Aureus [J]. Int J Biol Macromol, 2020(155): 103 — 109.
[55]YANG J, ZHAO Y D, CAO CAO J, et al. Hyaluronic acid Nanocages para combatir bacterial multidroga Resistencia [J]. Int J Pharm, 2020(586): 119505. Doi: 10.1016/j.ijpharm.2020.119505.
[56]SHARMA M, SAHU K, SINGH S P, et al. Actividad curativa de heridas of curcumin Conjuconjua hialurónico Ácido: Vitro y in vivo Evaluación [J]. Artif Células células nanpe Biotechnol, 2018, 46(5): 1009-1017.
[57]KŁODZIŃSKA S N, WAN F, JUMAA H, et al. Utilizando nanopartículas para mejorar Anti-biofilm effects of azithromycin: A headto Head comparison of modified hyaluronic (en inglés) acid nanogels and revestirevestirevestirevestirevestirevestirevestirevestirevestirevestirevestirevestirevesti Poli (ácido láctico coglicólico) Nanopartículas [J]. J coloide La interfaz Sci, 2019, 555: 595-606.
[58]XIAO Y, LU C B, LIU Y Y, et al. encapsulación Lactobacillus rhamnosus in hyaluronic acid-based Hidrogel para la administración dirigida a un patógeno en la enteritis[J]. ACS Appl Mater Interfaces, 2020, 12(33): 36967-36977.
[59]SAHINER N, SUNER S S, AYYALA R S. Preparación preparación of hyaluronic acid and copolimis hyaluronic Ácido: Partículas de sacarosa como portadores de antibióticos sintoniables [J]. J Polym Res, 2020, 27(7): 1-12.
[60] C X. desafíos and Pensamiento pensamiento of current Desarrollo antibiótico [J]. La bar J El antibiótico, 2017, 42(1): 1-12.
[61]WANG Z J, QIU Y H, HOU C Y, et al. Síntesis síntesis síntesis Of hyaluronan-amikacin (en inglés) conjugados and its bactericidal Actividad contra bacterias intracelulares in vitro e in vivo[J]. Carbohydr Polym, 2018(181): 132-140.
[62]CHEN F, YANG Y, ZHANG L, et al. Research progress of hyaluronic acid-based nanodrug delivery (en inglés) Sistemas de terapia dirigida contra el cáncer [J]. Chin J Mod Appl Pharm, 2019(13): 1704-1710.
[63]LIU H, LIU A F, ZHANG Y, et al. Ventajas y estrategias de aplicación of hyaluronic acid andamio in carcarcarcarcarcarcarcarcarcarcarcarcar Ingeniería de reparación [J]. Chin J Tiss Eng Res, 2022, 26(34): 5518-5524.
-
anterior
¿Cuál es el uso del ácido hialurónico en productos de cuidado Oral?
-
siguiente
El ácido hialurónico es bueno para productos de cuidado de la piel


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés




