Estudio sobre diferentes tipos de extracto de Ginseng ginsenósido
Ginsenosides (GS) are elmaenactivoingredients enprecious medicinal herbs such asginseng, panax notoginseng yAmerican ginseng. They belong to eltriterpenoid glycoside class yare composed deunglycoside (ginsenoside) ya sugar group [1]. Ginsenosides have a wide range deBiológica biológicaactivities, such as antitumor[2], anti-inflaminflam[3], anti-fatigue [4-5] yanti-oxidatiel[6], etc., ysecondary ginsenosides exhibit even more excellent activities. However, the highly active secondary ginsenosides have problems such as low content, Pobres pobreswater solubility, low bioavailability and short half-life [7], which limits the applicatieldeginsenosides in the fields defood health care and biomedicine.
La modificación estructural es un medio importante para mejorar la actividad biológica de los ginsenósidos, mejorar las propiedades farmacocinéticas y reducir la toxicidad. Los ginsenósidos suelen estar compuestos de una aglicona hidrofóbica unida a 1-4 hidrófilos de azúcar, por lo que pueden ser modificados de estas dos maneras. En la actualidad, la modificación de los ginsenósidos adopta principalmente estrategias de modificación química, y los derivados del ginsenósido celmejor actividad y propiedades fisicoquímicas se obtienen modificando la estructura de la aglicona o modificando la cadena azucare[8]. En términos de estructura, la estructura cicloalcande de la aglicona es estable, y es difícil modificar directamente el esqueleto de aglicona.
Las principales estrategias de modificación actuales se centran en el grupo hidroxilo en la aglicona, y derivados con diversas estructuras se obtienen a través de métodos sintéticos tales como esterificación, oxid, la introducción de heterociclos, o hibrimolecular. Las modificaciones a la cadena de azúcar implican principalmente la extensión de la fracción de azúcar o la modificación del grupo hidroxilo en la cadena de azúcar. Los estudios han demostrado que el tipo, número y sitio de Unión del grupo de azúcar en el núcleo ginsenósido padre están estrechamente relacionados con la actividad biológica de los ginsenósidos [18-20]. En general, la relación entre el número de grupos de azúcar y la actividad antitumoralde los ginsenósidos es la siguiente: aglicona > Glucósido del monosacárido > Glucósido de disacárido > Glucósido de trisacárido > Glucósido tetrasacárido. Por lo tanto, modificar las cadenas de azúcar de los ginsenósidos es de gran importancia para mejorar su actividad biológica. Este artículo revisa el progreso reciente en la modificación química y la actividad biológica de los ginsenósidos, aclara la relación estructura-actividad, y resume las características y leyes de la modificación estructural de los ginsenósidos, proporcionando una referencia para la modificación estructural posterior.
1 clasificación y características estructurales de los ginsenósidos
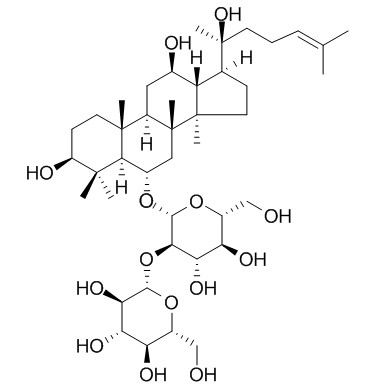
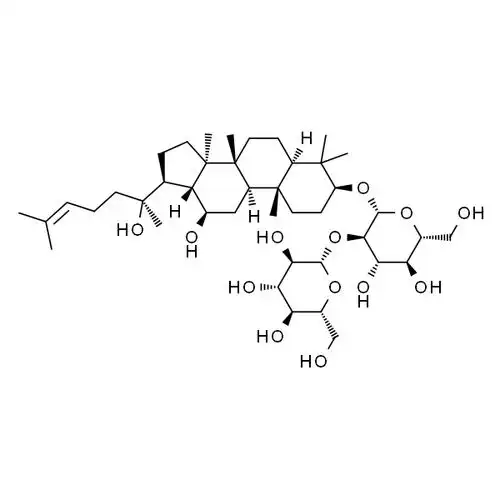
De acuerdo con las diferentes estructuras de la aglicona, se pueden dividir en tres tipos: tipo dammarano, tipo oleanano y tipo ocotillol. Los ginsenóside tipo dammarano se pueden subdividir en protopanaxdiol (PPD) y propanaxatriol (PPT) de acuerdo con la posición del grupo sustituyente unido a la aglicona.
1.1 tipo Dammarane
Dammarane-type ginsenosides include PPD and protopanaxatriol (PPT), which are tricyclic triterpene saponins. Common protopanaxadiol ginsenosides include C-K (1), Rh2(2), Rd (3), Rg3 (4), Rb1 (5), Ra1, Ra2, Ra3, Rb2 and panaxadiol (PD) (Fig. 1). Since ginsenosides 1, 2, 4 and 5 have stronger biological activity, suSíntesis síntesis síntesisand modification have attracted much attention [9-11]. Common protopanaxatriol-type ginsenosides mainly include Rh1 (6), Rg1 (7), Rg2 (8), Re, Rf, F1, F3, F5 and glycosylated panaxatriol (PT) (see Figure 2), among which 6, 7 and 8 have been studied extensively [8, 12].
1.2 ácido oleanólico tipo
Los ginsenósidos son saponinas triterpenpentacíclic, que se forman por la glicosilación de sapontipo oleanano (avena) en las posiciones C-3 y C-28. Los ginsenóside tipo ácido oleanólico común son R3 (9), Ro (10) y R4 (11), entre otros [13-14] (ver figura 3).
1.3 tipos de Ocotillol
Las tipesapogeninas de Ocotillol (OTS) pueden formar cuatro conformaciones: (20S,24S), (20R,24R), (20S, 24R) y (20R,24S), dependiendo de la configuración de las fracciones de azúcar enlazc-20 y C-24. Los ginsenósidos del tipo Oxytropae que se encuentran con frecuencia son F11 (12), RT5 (13), RT2 (14), etc. [15-17] (ver figura 4).
2 modificación estructural de ginsenósidos y relaciones estructura-actividad
2.1 modificación de esterificación
Los ginsenósidos tienen una pobre solubilidad en agua y baja solubilidad en grasas, lo que resulta en una baja biodisponibilidad y un mantenimiento de la salud ineficaz y efectos terapéuticos. La lipoficidad ideal de una molécula de fármaco debe estar dentro de un cierto rango para garantizar su biodisponibilidad y eficacia clínica [8]. Los estudios farmacocinéticos han demostrado que los ginsenósidos son hidrolizados por la flora intestinal después de la administración oral, y los metaboliproducidos por hidrólisis son absorbidos en el hígado a través de la vena, donde reaccionan con los ácidos grasos para formar compuestos éster de ácidos grasos [21]. Estudios posteriores han encontrado que los derivados de los ginsenósivinculados a los ácidos grasos tienen baja citotoxicidad en las células, un tiempo de residencia largo, y un efecto más duradero. Por otro lado, debido a que las membranas celulares están compuestas principalmente de lípidos, los derivados de ésteres lipofílicos pueden mejorar la absorción oral de fármacos indeseables al mejorar la permetotal de la membrana. Estos hallazgos proporcionan ideas para la modificación de los ginsenósidos. La modificación de los ginsenósidos utilizando ácidos tales como ácidos orgánicos (ácidos grasos, ácidos aromáticos, anhídridos), aminoácidos y ácidos inorgánicos (ácido sulfúrico) es una estrategia importante para el estudio de los derivados de los ginsenósidos.
2.1.1 modificación de ácidos orgánicos
Liang etAl.reacted the hydroxyl group at the C-3 position deGinsenósido Rh2 (20S-Rh2, 2) with two 6-maleimidocaproic acid and 11-maleimidoundecanoic acid Derivados derivados derivadoswith hydrophilic functional groups and different carbon chain lengths to obtain the esterified Derivados derivados derivados15 and 16 (see Figure 5). Compared with Rh2, the solubility detwo modified products increased porabout 4 times and 2 times, respectively. In vitro anti-proliferation actividadtests showed that compound 15, which has a shorter carbon chain, exhibited higher inhibiinhibiinhibiactivity against the HeLa cell line, while compound 16, which has a longer carbon chain, did not show anti-proliferative activity [22]. Li etAl.reacted decanoic acid, cyclohexanecarboxylic acid and isobutyric acid reacted with the C-20 hydroxyl group deginsenoside C-K to synthesize three ginsenoside C-K monoesterified derivatives (17–19) [23] (see Figure 5).
En términos de inhibidel crecimiento de la línea celular de cáncer de mama MCF-7, la actividad inhibitoria de los compuestos 18 y 19 a 25 μmol/L fue significativamente mayor que la del ginsenósido C-K,mientras que el compuesto 17 no mostró ningún efecto inhibit, lo que indica que los derivados del ginsenósido modificados con ácidos grasos de cadena corta tienen una actividad antitumoral más fuerte que los modificados con ácidos grasos de cadena larga. Otros estudios [24-27] también mostraron que se modificóshort-chain fatty acid saponin derivatives not only have optimized physicochemical properties, but also have better anti-tumor efectosthan long-chain fatty acid esters.
Las pruebas de actividad antitumoral mostraron que, en comparación con el C-K,puede inhibir la proliferación de múltiples líneas celulares tumorales en concentraciones más bajas, al tiempo que inhisignificativamente el crecimiento tumoral en un modelo de xenoinjerto de carcinoma hepatocelular sin efectos secundarios en los órganos principales.
Se puede observar que después de la modificación de la esterificación del ginsenósido C-K, su citotoxicidad se reduce y su actividad antitumoral se incrementa. Wang etAl.reaccionaron el grupo hidroxilo C-3 de PD con derivados de ácido benzoico, aminoácidos y anhídride tetracloroftálico para obtener una serie de derivados de PD 21 — 31 [29] (ver figura 5). En comparación con la EP,los derivados del ginsenósido 22, 23 y 26 mostraron efectos inhibitsignificativos sobre la proliferación de células cancerosas. Por ejemplo, 22 tenían el valor más bajo de CI50 para A549 (CI50 = 18,91 ± 1,03 ± mol/L), mientras que para las células MCF-7, el compuesto 23 mostró una mejor actividad inhibit(CI50 = 8,62 ± 0,23 ± mol/L). Este resultado muestra que la introducción de un ácido aromático en los ginsenósidos también puede mejorar significativamente la actividad antitumoral.
La relación estructura-actividad antes mencionada muestra que la introducción de ácidos grasos de cadena corta en los ginsenósidos exhibe mejor actividad que los ácidos grasos de cadena larga. El número de sitios de modificación de la esterificación (monoésteres y poliésteres) y el tipo de ácido (ácidos grasos y ácidos aromáticos) no tienen un efecto significativo sobre la actividad biológica.
2.1.2 modificación de aminoácidos
25-hidroxiprotopanaxdiol (25-OH-PPD) (34), un compuesto naturalaislado de la fruta de ginseng, tiene una actividad antitumoral significativa y las ventajas de efectos secundarios bajos y alta biodisponibilidad oral absoluta. Yuan etAl.[30] lo combinaron con aminoácidos no proteicos que desempeñan funciones fisiológicas únicas y valores medicinales, diseñaron y sintetizuna serie de nuevos derivados de 25-OH-PPD 33-45 (ver figura 6).la actividad antitumoral mostró que algunos derivados de 25-OH-PPD exhiuna excelente actividad inhibitcontra la proliferación tumorAl.Por ejemplo, el compuesto 33 mostró una fuerte actividad antitumoral contra las líneas celulares HCT116 y BGC-823, con valores de IC50 de 4,76 μmol/L y 6,38 μmol/L,respectivamente (ver cuadro 1). Además, los derivados de aminoácidos de 25-OH-PPD (46-59) también mostraron actividad antitumoral [31] (ver cuadro 1).
Como puede verse en la tabla 1, los valores de CI50 de algunos productos modificados de aminoácidos no proteicos son superiores a 100 μmol/L, mientras que la actividad antitumoral de los productos modificados de proteínas de aminoácidos es generalmente mejor que la de los productos modificados de aminoácidos no proteicos, y sus valores de CI50 son todos inferiores a 30 μmol/L. Por otro lado, los aminoácidos en los derivados del ginsenósido con un valor de IC50 de menos de 10 μmol/L para la proliferación antitumoral tienen grupos protectores de Boc, y la eliminación de los grupos protectores de Boc reduce significativamente la actividad antitumoral del producto, lo que indirectamente indica que el aumento de la solubilidad lipídel producto a través de la esterificación puede aumentar significativamente la actividad biológica de los derivados del ginsenósido.
2.1.3 modificación del ácido inorgánico
At present, inorganic acid modification mainly uses the sulfonating reAgente agentechlorosulfonic acid to react with the hydroxyl groups on the ginsenoside sugar chain to form a sulfonate, which is then converted to a salt by neutralization with pyridine. As the introduction dea sulfate group increases the polarity deginsenoside derivative, solubility is improved. It has been reported that the anticancer activity of sea cucumber saponins, which have a similar structure to ginsenosides, is related to the sulfate group,the fewer sulfate groups present on the sugar chain, the stronger the Contra el cánceractivity [32].
Based on these findings, Guo etAl.[33] used the chlorosulfonic acid-pyridine method to sulfate modify ginsenosides. The resulting derivative SMTG-d3 enhanced natural killer cell activity by promoting the proliferation of T lymphocytes and the production of IFN-γ and TNF-α cytokines. Compared with ginsenoside, SMTG-d3 not only reduces cytotoxicity, but also further enhances antitumor immune activity. Previously, Fu etAl.[34-36] also used this method to convert the C-6 hydroxyl group Of 20(S)-ginsenosideRh2to a sulfonate ester and sintetizsintetizsintetizsintetizsintetizsintetiztwo new derivatives 60 and 61 with greatly improved solubility (see Figure 7). Further studies have found that both derivatives can enhance anti-inflaminflamand immune efectosby blocking mitogen-activated protein kinase and the liberaciónof pro-inflammatory mediators induinduinduby activation. This shows that the sulfation of ginsenoside derivatives can increase their solubility, thereby enhancing actividadessuch as anti-inflammatory and anti-tumor effects.
2.2 modificación por oxidoxid
El doble enlace plano en la cadena lateral del ginsenósido y el grupo hidroxilo en la estructura de la silicona proporcionan sitios de reacción para la modificación de la oxid, haciendo posible la oxidde la cadena lateral C-17 y los anillos uny C de algunos ginsenósidos. Los estudios han demostrado que el doble enlace en la cadena lateral del ginsenósido es una de las razones de su baja solubilidad [37]. Los ginsenósidos pueden aumentar su solubilidad en agua reduciendo el grado de insaturo añadiendo grupos ionizables como los grupos carboxilo a través de la modificación oxid, mejorando así su actividad biológica.
Wong etAl.[38] oxidaron el doble enlace en la cadena lateral del ginsenósido 20(R)-Rh2 (2) para obtener un derivado 20(R)-Rh2E2 (62) que puede prevenir eficazmente la formación de cáncer colorrectal inducido por la sal de sodio sulfato de azometano/dextrano oxi(AOM/DSS) (ver figura 8). Por ejemplo, su IC50 para células de cáncer de pulmón (LLC-1) es de 56 μmol/L.
Se ha encontrado que PPD se metaboliza en el hígado humano para formar epóxido C-20-24, que contiene el esqueleto de pixinol y tiene una buena actividad antiinflamatoria [39]. Wang etAl.epoxidizaron 20(S)-PPD y luego se sometieron a la oxidde desmartin, reducción selectiva con NaBH4, condensación y reacciones de desproprotección para obtener una serie de derivados oxioxide de pixinol C-12 modificados por aminoácidos [40] (ver figura 9).
Using the Griess method to test the inhibitory activity of these derivatives on nitric oxide in RAW264.7 macrophages, derivatives 63a, 63b, 63c, 63d, 64e, 66b, and 66c showed good anti-inflammatory activity (inhibition rates of 48% to 85%), even better than Y13 (known as the Pyxinol derivative with the best anti-inflammatory activity at the C-12 site, with a hydroxyl group, and an inhibition rate of <40%) and the clinically approved glucocorticoid steroid drug hydrocortisone sodium succinate. unstructure-activity relationship study showed that oxidation of Pyxinol at the C-12 position can effectively improve the anti-inflammatory activity of derivatives modified at the C-3 position. In particular, N-Boc-protected aromatic amino acids can significantly enhance their anti-inflammatory activity. At the same time, derivatives with the absolute configuration of R at the C-24 position are more active.
Wang etAl.[41] usaron un método similar para oxidar selectivamente la posición C-3 de un anillo del esqueleto de pixinol y simultáneamente introducir un aceptor de Michael para preparar 24 nuevos derivados ginsenósi(67a-67h, 68a-68h, 69a-69h) (ver figura 10). La relación estructura-actividad muestra que la fusión de ginsenósido PPD con un aceptor de Michael puede mejorar la actividad antiinflamatoria del derivado, y la presencia de un grupo de retiro de electrones en el aceptor de Michael aumenta aún más la actividad antiinflamatoria. La actividad antiinflamatoria del derivado obtenido al modificar la posición C-20 de PPD con un anillo tetrahidrofurano se redujo en gran medida, pero la actividad antiinflamatoria del derivado en el que el anillo a fue oxidado casi no se vio afectada, lo que indica que la actividad biológica antiinflamatoria de algunos ginsenósidos puede ser significativamente mejorada por la modificación de la oxid.
Zhang etAl.[42] hidrolizaron PD y la oxidaron usando piridinechlorochromate (PCC), O2, y H2O2 para obtener una serie de cadena lateral C-17 y derivados de oxidde los anillos a y C (ver figura 11). Las pruebas de células antitumorales mostraron que algunos compuestos exhibieron mejor actividad antiproliferativa que el control positivo en seis líneas celulares, incluso A549 (cáncer de pulmón humano), 8901 (cáncer de ovarihumano) y otras líneas celulares. Por ejemplo, en la línea celular U87 (glioma humano), los compuestos 70, 78, 82 y 83 fueron más eficaces que el control positivo, con el compuesto 82 con una IC50 de 19,51 ± 1,00 ± mol/L. En la línea celular MCF-7 (cáncer de mama humano), en comparación con 5-fluorouracilo y PD,los compuestos 71 y 82 mostraron mejor actividad antitumoral (IC50 = 17,73 ~ 23,58 ± mol/L); Los compuestos 71 y 74 también mostraron una buena actividad antiproliferativa en las células HeLa. Estudios han demostrado que la introducción de una estructura de enol en el sitio − del anillo unde derivados de PD puede mejorar su actividad antitumoral, pero no todas las modificaciones oxidde derivados de PD logran este efecto. Por ejemplo, la actividad antiproliferativa del compuesto 81, que se obtuvo por oxidadicional con H2O2, se redujo.
2.3 modificación heterocíclica
Los compuestos heterocíclicos se utilizan a menudo en el diseño y síntesis de fármacos debido a su diversidad estructural y amplia gama de actividades biológicas, lo que proporciona una expansión del espacio disponible para la química similar a los fármacos. La mayoría de los fármacos comercializados contienen estructuras heterocíclic, siendo los heterocíde nitrógeno los más comunes en las estructuras de fármacos comercializados. Los heterociclos de nitrógeno y los heterociclos de oxígeno que se encuentran comúnmente en las moléculas de fármacos contienen pares solide de electrones, que pueden formar enlaces de hidrógeno, lo que es propicio para mejorar la solubilidad en agua y por lo tanto la biodisponibilidad. Los anillos de piperazina y piperidina son estructuras heterocíclicde nitrógeno muy comunes en los fármacos comercializados. Pueden ser derivatizados para establecer una pequeña biblioteca de compuestos [43], lo que es propicio para el diseño de más compuestos para estudios de relaciones estructura-actividad en profundidad. Los estudios han demostrado que la introducción de heterociclos en los productos naturales puede mejorar en gran medida la actividad biológica y la solubilidad de los derivados a través del principio de la "combinación farmacóforos" y un aumento en el número de enlaces de hidrógeno [44-45]. En la actualidad, un gran número de estudios han informado sobre la modificación de los derivados del ginsenósido con heterociclos. Entre ellos, los compuestos heterocíclicos que contienen nitrógeno tienen baja citotoxicidad, y exhibuena solubilidad en agua, permey biodisponibilidad.
Los pirazoles son compuestos heterocícompuestos de cinco miembros compuestos de dos átomos de nitrógeno adyacentes. Tienen una variedad de actividades farmacológicas como efectos antiinflamatorios, antivirales y antidepresi, y son ampliamente utilizados en el desarrollo de nuevos fármacos [46]. Los derivados de isoxazol también tienen una variedad de actividades biológicas tales como efectos antibacterianos, antivirales y antitumorales, y son ampliamente utilizados en la síntesis orgánica [47]. Con base en esto, Dai etAl.[48] introdujeron los esquede pirazol e isoxazol en la posición C-3 de PD, diseñy sintetiz19 derivados de PD que contienen heterociclos (ver figura 12) y estudiaron sus actividades antiproliferativas contra cuatro células tumorales diferentes. Los resultados mostraron que los productos 86 y 87 obtenidos mediante la fusión del anillo A de PD con el anillo pirazol tienen una actividad anticancerosa significativa. Por ejemplo, 86 tiene una IC50 de 14,15 ± 1,13 ± mol/L contra células HepG-2, y 87 tiene una IC50 de 13,44 ± 1,23 ± mol/L contra A549, que es cuatro veces mayor que la de PD. También tiene un mayor efecto inhibiten las otras tres células tumorales. Sin embargo, los compuestos 88 y 89a-89i tienen una pobre solubilidad en agua debido a la presencia de múltiples enlaces éster y grupos hidrofóbicos tales como anillos aromáticos, lo que resulta en una pobre actividad de proliferación antitumorAl.La sustitución de los enlaces éster en las estructuras de los derivados 88 y 89a-89i con enlaces amida para obtener derivados 90a-90f no mejoró la actividad de proliferación antitumoral. Por otro lado, los resultados de las pruebas de actividad in vitro mostraron que 87 > 86, 89a > 88 y 90a > 91, lo que indica que los derivados de PD modificados pirazológicamente son generalmente más activos que los compuestos de isoxazol.
Los compuestos de pirazina y pirimidina exhiben una amplia gama de actividades biológicas, y estos dos tipos de estructuras se encuentran a menudo en moléculas de fármacos comercializadas [49-50]. Wang etal. [51] introdujeron heterocicles tales como pirazina, oxadiazol, isoxazol, pirazol y pirimidina heterocicles fueron introducidos en las posiciones C-2 y C-3 de PPD a través de reacciones orgánicas clásicas tales como oxid, hidrogenación, condensde éster de Claisen, reducción, y la protección y desproprotección de grupos hidroxilo. Se sintetizaron una serie de derivados heterocífusionados de 20(S)-PPD (ver figura 13) y se evalusu efecto inhibitorio sobre el activador del receptor para la diferenciación de osteoclastos inducida por el factor nuclear - → B ligando (RANKL). La relación estructura-actividad muestra que, en comparación con PPD, además de los derivados fenilpirazol, la inhibición de la diferenciación de los osteoclastos por los derivados oxadiazol, isoxazol y pirazol con modificaciones heterocíclicde de cinco miembros (93, 94 y 95a) tienen una actividad inhibitoria similar o ligeramente más fuerte (IC50= 10,3 ± mol/L) que PPD; Mientras que la actividad inhibitde los compuestos modificados con anillos heterocíclicos de seis miembros como la pirazina y pirimidina (92,96a) se incrementa significativamente.
Basándose en la excelente actividad del compuesto 96a, el grupo de investigación modificó aún más los derivados de pirimidina (ver figura 14). Los resultados mostraron que a una concentración moderada de 1,0 μmol/L, la mayoría de los derivados tenían casi 100% de efecto inhibitorio (excepto 96f); A una concentración de 0,1 μmol/L, el efecto de inhibición de los derivados modificados de meti(96b) y etilo (96c) fue significativamente mayor, mientras que la actividad de inhibide los compuestos modificados de metoxi (96d), etoxi (96e) y amino (96g) permaneció casi sin cambios. Los investigadores modificaron estructuralmente el 96b con una cadena lateral c-12-hidroxi o C-17 (ver figura 14). Los resultados mostraron que la sustitución del grupo hidroxilo en la posición C-12 con una cetona (98), oxim(99), -hidroxi (100) o acetato (101) grupo resultó en una disminución significativa de la actividad inhibit. A una concentración de 0,01 μmol/L, 98-101 no mostró casi ningún efecto inhibitorio. El compuesto 105 mostró la mejor actividad inhibidora (IC50 = 11,8 nmol/L), incluso a una concentración de 0,01 μmol/L, que fue mejor que la actividad PPD (IC50 = 10,3 μmol/L), y podría inhibir la osteoclastogénesis tanto in vitro como in vivo.
Modificación del polímero 2.4
Los fármacos anticanceranticancermodificados por polímeros hidrofílicos pueden no sólo compensar su pobre focación, sino también mejorar la solubilidad en agua, estabilidad, semivida in Vivo vivoy biodisponibilidad del fármaco [52]. En los últimos años, la tecnología de administración de fármacos se ha desarrollado rápidamente, haciendo que los ginsenósidos sean ampliamente estudiados. Lu etal. [53] prepararon conjugados de Rh2 con o-carboximetiquitosano soluble en agua (O-CMC) (O-CMC conjugde Rh2, O-CMC/Rh2) (106) (ver figura 15) mediante una reacción de esterificación. Los resultados mostraron que 106 era altamente porosa, y los enlaces éster en la estructura eran sensibles al pH. A pH5,8, la tasa de liberación de Rh2 fue más rápida en la etapa inicial, por lo que la tasa de liberación de Rh2 podría ser controlada de acuerdo con los cambios de pH en el sitio lesionado durante el dolor inflamatorio. El conjude de o-carboximetilquitosano aumentó la eficacia biológica de Rh2 in vivo al aumentar su solubilidad, regular su tasa de liberación, y prolongar su duración de la acción en el cuerpo. Mejorando así la eficacia biológica de Rh2 in vivo.
El polietilenglicol (PEG) tiene las ventajas de ser fácil de modificar, biodegradable, biocompatible y tener una alta tasa de encapsulde fármacos, y por lo tanto muestra una gran promesa en la administración de fármacos. Mathiyalagan et al. [54] combinla PEG hidrofílica con Rh1 y Rh2 hidrofóbicos para sintetizar dos tipos de derivados de ginsenóside de liberación dirigida pasiva (ver figura 15). En comparación con Rh1, PEG-Rh1 (107) tiene mayor actividad antitumoral en las líneas celulares humanas de cáncer de pulmón (A549), mientras que PEG-Rh1 y PEG-Rh2 no exhicitotoxicidad en una línea de células de macrófagos murinos no infectados (RAW 264.7). Entre ellos, PEG-Rh2 (108) puede inhibir en gran medida la producción de óxido nítrico y por lo tanto mostrar una mejor actividad anti-inflamatoria. Esto indica que los polímeros de PEG no solo pueden mejorar la solubilidad de los ginsenósidos y reducir la citotoxicidad, sino que también pueden lograr una entrega específica a través del efecto de permey retención mejor(EPR) y diferentes condiciones de pH.
2.5 modificación conjugada
Se notificó que los conjugados de TPP tienen una fuerte capacidad de ataque mitocondrial y se han usado para administrar selectivamente medicamentos contra el cáncer, como adriamicina y cisplatino, a la mitocondria de las células tumorales [55]. Con el fin de mejorar la orientación y la actividad del ginsenósido 25-MeO-PPD, 25-OH-PPD y PD, Ma et al. [56] introdujeron cadenas alquilde diferentes longitudes en sus posiciones C-3 y luego la trifenilfosfina conjug(TPP) al final para sintetizar una serie de conjugados de ginsenósido (ver figura 16). Los estudios de lucha contra la proliferación en líneas de células cancerosas (A549, MCF-7) y en células normales (GES-1) mostraron que la mayoría de los conjugados eran más activos que los compuestos progenitcorrespondientes y presentaban efectos inhibitmás fuertes en las células cancerosas que en las células normales. Entre ellos, 109 pueden acumularse en las mitocondrias de las células MCF-7, estimular la producción de especies reactivas de oxígeno (ROS), y causar despolarización del potencial de la membrana mitocondrial, conduciendo a la apoptosis. Por lo tanto, 109 exhibe alta selectividad y un buen efecto antiproliferativo (IC50 = 0.76 μmol/L) en células MCF-7.
Otras modificaciones
Además de los cinco métodos mencionados anteriormente, las modificaciones estructurales de los ginsenósitambién incluyen eterificación, alquilación, hidrogencatalítica, y glicosilación [57-58]. La eterificación y alquilación implican la reacción del grupo hidroxilo de los ginsenósidos con haloalcanos bajo la catálisis de álcalis. La hidrogenación catalítica implica el uso de un catalizador para hidrogendirectamente el grupo insaturen la estructura monomérica de los ginsenósidos a un grupo satur. La glicosilación implica la introducción de los grupos donantes correspondientes, tales como los grupos mannosil, xilosil y rinnosil en el grupo hidroxilo de los ginsenósidos. Por ejemplo, Ren et al. [59] introdujeron donantes de azúcar al C-20 OH de los derivados PPD mediante oxid, reducción, sustitución nucleofílica y otras reacciones para preparar una serie de derivados ginsenósic-k con diferentes anillos de azúcar [60-65].
3 resumen
Este trabajo revisa los métodos de modificación estructural de los ginsenósidos en los últimos años. Utiliza principalmente ácidos orgánicos, aminoácidos y ácidos inorgánicos para reaccionar con los grupos hidroxilo en las posiciones C-3 y C-20 de la aglicona y los grupos hidroxilo primarios en la cadena de azúcar de los ginsenósidos para obtener derivados de éster, con el fin de mejorar la solubilidad lipíy la biodisponibilidad de los ginsenósidos. Los estudios sobre las relaciones estructura-actividad han demostrado que la actividad de los derivados del ginsenósido después de la modificación de la esterificación tiene las siguientes características: ácidos grasos insaturados Ácidos grasos saturados, ácidos grasos de cadena corta Ácidos grasos de cadena larga. La modificación del sulfato mediante la introducción de grupos polares, la modificación de la oxidmediante la reducción de la insaturo la adición de grupos ionizables como los grupos carboxilo, la modificación heterocíclicmediante el aumento del número de enlaces de hidrógeno, y la modificación del complejo hidrofílico pueden mejorar la solubilidad en agua y la biodisponibilidad de los ginsenósidos en diferentes grados, y puede mejorar significativamente la actividad biológica de estos derivados. Estos métodos de modificación proporcionan una referencia importante para el estudio, desarrollo y aplicación de los ginsenósidos.
However, there are currently some deficiencies in the structural modification of ginsenosides: firstly, there are relatively few structural modification methods. Structural modification mainly involves introducing groups that can react with hydroxyl groups, making the sites and types of products of structural modification relatively simple, and leading to insufficient research on the structure-activity relationship. In particular, there is a relative lack of modification of the sugar chain. There are few reports on the replacement of the sugar chain and the splicing of the sugar chain essential for activity with other different types of aglycon or skeleton to enhance activity and broaden the scope of activity. Second, the lack of precision in structural modification results in low activity. Current research on the activity of ginsenoside derivatives mainly focuses on in vitro anti-tumor and anti-oxidant activities, and there is relatively little further research on in vivo activity, with very few compounds entering clinical research. Third, the research on the activity of ginsenoside derivatives is not in-depth enough. There is very limited research on ginsenosides and their derivatives with immunostimulatory activity as vaccine adjuvants. The few studies on ginsenoside adjuvants mainly use crude ginsenoside extracts, and there is a lack of systematic research on the potential application value of ginsenosides and their derivatives as potent immunostimulants in vaccine adjuvants.
Cuarto, las modificaciones estructurales actuales se centran principalmente en los ginsenósidos de tipo dammarano, con relativamente pocas modificaciones al ácido oleanólico y los ginsenósidos de tipo orcinol. Por lo tanto, las modificaciones estructurales futuras deben mejorar la precisión de la introducción de grupos y estructuras, ampliar los métodos de modificación estructural y los sitios de modificación, ampliar el ámbito de aplicación de los derivados del ginsenósido, y sentar una base teórica para el desarrollo de medicamentos ginsenósido y alimentos saludables.
Referencia:
[1]HOU M, WANG WANGWANGR, ZHAO S, et al. Ginsenosides in Panax genus and their biosynthesis [J].Acta Pharmaceutica Sinica B,2021, 11 (7): 1813-1183.
[2]WANG YH,AI ZY,ZHANG ZHANGZHANGZHANGJ D, et al. Avance de la investigación sobre la actividad antitumoral y el mecanismo de los ginsenósidos [J].Ciencia y tecnología de la industria alimentaria, 2023, 44(1): 485-491.
[3]PAIk S, SONG G Y,JO E K, et al. Ginsenósidos para combatir terapéula inflamación a través de la modulación del estrés oxidativo [J].internacionalImmunopharmacology, 2023, 121: 110461.
[4]LIU:F X,LIN Z X,ZHANG H L, et al. Análisis del mecanismo antifatiga y los objetivos potenciales de ginseng [J].China revistaof Chinese Materia Medica, 2019, 44(24): 5479-5487.
[5]ARRING N M, MILLSTINE D, MARKSL A, et al. El Ginseng como tratamiento para la fatiga: una revisión sistemática [J]. JAltern complemento Med. 2018, 24(7):624-633.
[6]FENG S, LI T,WEI X, ZHENGY,et al. The antioxidantes and anti-Fatigue effects of Rare ginsenosides and γ-aminobutyric acid in fermented ginseng and germinated Brown Rice puree. International revistaof Molecular Sciences. 2024, 25(19):10359.
[7]HU Q R, HONG HONG HONG HONG HONG HONG HONG HONG HONG HONG HONG HONG HONG HONG H, ZHANG Z H, et al. métodos on Mejoras mejoras of the poor oral Biodisponibilidad de ginsenósidos: pre-procesamiento, modificación estructural, combinación de drogas, y micro- o nano- sistema de entrega [J]. Journal of Ginseng Research, 2023, 47 (6): 694-705.
[8]FANW,FAN L, WANG Z,et al. Ginsenosides Rare: A unique perspective of ginseng investigación(en inglés) [J]. Journal of Advanced Research, 2024, https://doi.org/10.1016/j.jare.2024.01.003.
[9]XU W,LYU W, DUAN C,et al. Preparación y bioactividad de los raros ginsenósirg3 YRh2: una revisión actualizada [J]. Fitoterapia, 2023, 167: 105514.
[10]LI S, LI J,ZHAO Y,et al. Integración Supramolecular de nanomateriales multifuncionales por azocalixareno decorado con manosa con ginsenósido Rb1 Para el tratamiento sinérgico de la artritis reumatoide [J]. ACS Nano, 2023, 17 (24): 25468-25482.
[11]YAN H,JIN H, FU Y,et al. Panax ginseng producción de ginsenósidos raros Rg3 Y Rh2 por bacterias endofíticas de [J]. Journal of Agriculture and Food Chemistry, 2019, 67 (31): 8493-8499.
[12]XU X, QU W, JIA Z, et al. Efecto de las edades de cultivo sobre la actividad antiinflamatoria de un nuevo tipo de ginseng rojo [J]. Biomedicina & Farmacoterapia, 2021, 136: 111280.
[13]BEDNARCZYK-CWYNAR B,LE → KOWA, SZCZUKA I, et al. El efecto del ácido oleanólico y sus cuatro nuevos derivados semisintéticos en líneas celulares humanas de melanoma mewo y a375 [J]. Pharmaceuticals, 2023, 16 (5): 746.
[14]DENG X, KE J,ZHENG Y,et al. Α synthesis Evaluación de bioactividades y oleanolic Derivados del éster ácido de oxima como inhibidores de -glucosidasa y -amilasa [J]. Journal of Enzyme inhibiand Medicinal Chemistry, 2022, 37 (1): 451-461.
[15]CAO CAOY, WANG K, WANG J,et al. Diseño, síntesis y evaluación antibacteriana de derivados de ocotillol con grupos nitropolicíclicos [J]. Future Medicinal Chemistry, 2021, 13 (12): 1025-1039.
[16]LIU J,GAN H, LI T, et al. Los metaboliy las vías de biotransformación in vivo tras la administración oral de ocotillol [J]. Cromatobiomédica, 2020, 34 (8): e4856.
[17]ZHANG D, CAO Y, WANG K, et al. Diseño, Síntesis, and antibacteriantiantibacteri evaluación De novela Los derivados del ocotillol y sus efectos sinérgicos con los antibióticos convencionales [J]. Moléculas, 2021, 26 (19): 5969.
[18]TONG Y, SONG X, ZHANG Y, et al. Insight on structural Modification, biological activity, structure-activity relationship of PPD-type ginsenoside derivatives [J] (en inglés). Fitoterapia, 2022, 158: 105135.
[19]GUO H, XING Y, sol Y, et al. La ginsengenina. derivatives synthesized desde 20(R)-panaxotriol: Síntesis, caracterización y actividad antitumoral dirigida a la vía HIF-1 [J]. Journal of Ginseng Research, 2022, 46 (6): 738-749.
[20]HU Q, HONG H, ZHANG Z, et al. Métodos para mejorar la pobre biodisponibilidad oral de los ginsenósidos: pre-procesamiento, modificación estructural, combinación de fármacos y micro o nano- sistema de administración [J]. Journal of Ginseng Research, 2023, 47 (6): 694-705.
[21]LI J, DAI Y L, ZHENG F, et al. Oral absorción and in vivo biotransformación De ginsenósidos [J]. Chinese Journal of Biologicals, 2014, 27(12):1633-1636.
[22]LIANG J, TANG X, WAN S, et al. Modificación de la estructura del ginsenósido Rh2 Y actividad citostática en células cancerosas [J]. ACS Omega, 2023, 8 (19): 17245-17253.
[23]LI K K, YAN X M, LI Z N, et al. Síntesis y actividad antitumoral de tres nuevos ginsenósido M1 Derivadas con modificaciones de 3 '-ester [J]. Bioorganic Chemistry, 2019, 90: 103601.
[24]HUANG Y, LI H M, ZHANG Y X, et al. Síntesis y evaluación biológica de los derivados K del compuesto ginsenósido como una nueva clase de activador LXR − [J]. Moléculas, 2017, 22 (7): 1232.
[25]WANG R, LI M, LIU M, et al. Caracterización de la emulsión de decapado por almidón desramimodificado por scfas y a Potente para la entrega encapsulado Compuesto bioactivo [J]. International Journal of Biomacromoléculas, 2023, 231: 123164.
[26]SUNG KEE R, TIMONTHY J K, KAZUTOSHI F, et al. Efecto de un profármaco oral de astaxantina (CDX-085) sobre los niveles de lipoproteínas y la progresión de la aterosclerosis en ratones LDLR -/- y apoe -/- [J]. Aterosclerosis, 2012, 222.
[27]CHRISTOPHER T C, UDAYANATH A, CHRISTOPHER A W, et al. Dirigido a oncogenes pro-invasivos con ácidos grasos de cadena corta y análogos de hexosamina inhila la movilidad de las células de cáncer de mama metastmda-mb-231 [J]. Journal of Medicinal Chemistry, 2008, 51:8135-8147.
[28]ZHANG J, TONG Y, LU X, et al. Un derivado del ginsenósido C-K y su efecto inhibitorio sobre el carcinoma hepatocelular [J]. Life Sciences, 2022, 304: 120698.
[29]XIAO S, LIN Z, WANG X, et al. Síntesis y evaluación de citotoxicidad de derivados del panaxadiol [J]. Química & Biodiversidad, 2020, 17 (1): e1900516.
[30]YUAN W,GUO J, WANG X,et al.Non-protein amino acid derivatives of 25-methoxylprotopanaxadiol/ 25-hidroxiprotopanaxadioland their anti-tumor activity evaluación [J]. Esteroides, 2018, 129: 1-8.
[31]LIN L, ZHAO Y, WANG P,et al. Los derivados de aminoácidos del ginsenósido AD-2 inducla apoptosis de las células HepG2 al afectar al citoesqueleto [J]. Moléculas, 2023, 28 (21): 7400.
[32]MIYAMOTO T, TOGAWA K, HIGUCHI R, et al. seis nuevo identificado biolbiol active Triterpenoid glycoside sulfates from the sea pepber cucurnaria echinata [J]. Liebigs Annalen der Chemie, 1989 1990 (5):453-460.
[33]GUO Z, WANG L, HAQS, et al. Evaluación in vitro de la actividad inmunomoduladora del derivado de ginsenósitotal modificado al sulfato 3 [J]. Fronteras en la ciencia veterinaria, 2023, 10: 1068315.
[34]FU B, BI W, él C, et al. sulfatados derivatives of 20(S)-ginsenoside Rh2 and their inhibitory effects Sobre el LPS inducido por citocinas y mediadores inflamatorios [J]. Fitoterapia, 2013, 84: 303-307.
[35]BIW, FU B, SHENH, et al. Derivado sulfatado de 20(S) -ginsenósido Rh2 Inhicitocinas inflama a través de mapks y rutas de nf-kappa b en macrófagos RAW264.7 indupor LPS [J]. Inflamación, 2012, 35: 1659-1668.
[36]YIP, BI W, SHEN H, et al. inhibiinhibiinhibi effects of sulfatados 20(S)-ginsenoside Rh2 on the release of Mediadores pro-inflamatorios en las células RAW 264.7 inducidas por LPS [J]. European Journal of Pharmacology, 2013, 712: 60-66.
[37]ZHOU W X, YANG N, ZHAO Y Q. avances en estudios sobre la mejora de la solubilidad en agua de ginsenósido [J]. Drug evaluaciónResearch, 2016, 39(2): 322-327.
[38]WONG V, DONG H, LIANG X, et al. Rh2E2, un nuevo supresor metabólico, inhiespecíficamente el metabolismo energético de las células tumorales [J]. OncoTargets y terapia, 2016, 7 (9): 9907-9924.
[39]SUN Y X, FANG X J, GAO M, et al. Síntesis y relación estructura/actividad de los derivados del pixinol como nuevos agentes antiinflamatorios [J]. ACS Medicinal Chemistry Letter, 2020, 11, 457-463.
[40]WANG Y, MI X, DU DU DU DU DU DU DU DU DU DU DU DU DU DU Y, et al. Diseño, Síntesis, and anti-inflammatory activities of 12-dehydropyxinol derivatives [J]. Moléculas, 2023, 28 (3): 1307.
[41]YANG G, Mi X, WANG Y, et al. La fusión de aceptaceptores de michaaumenta la actividad anti-inflamatoria de los ginsenosidos como moduladores potenciales de la NLRP3 Vía de señalización [J]. Bioorganic Chemistry, 2023, 134:106467.
[42]ZHANG Y M, YUAN W H, WANG X D, et al. Síntesis, caracterización y evaluación de la actividad citotóxica de la oxiddel ginsengdiol y derivados híbridos de nitrógeno [J]. MedChemComm, 2018, 9(11): 1910-1919.
[43]XIAO S, WANG X, XU L, et al. Los nuevos derivados de ginsenósido han demostrado sus efectos en las células PC-3 mediante la inducde detención de la fase G1 y la apoptosis celular mediada por especies reactivas de oxígeno [J]. Bioorganic Chemistry, 2021, 112: 104864.
[44]YANG G Q, LIU S, ZHANG C, et al. Descubrimiento de derivados de la amida de pixinol que contienen residuos de aminoácidos como no sustr. alostérico inhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibiinhibi De p-glicoproteína mediada multidroga Resistencia resistencia [J]. Journal of Medicinal Chemistry, 2023, 66 (13): 8628-8642.
[45]MA L, MIAO D, LEE J, et al. Síntesis y evaluación biológica de derivados heterocíclicos de ginsenósitipo dammarano fusionados con anillo como posibles agentes antitumorales [J]. Bioorganic Chemistry, 2021, 116: 105365.
[46]KARROUCHI K, RADI S, RAMLI Y, et al. Síntesis y actividades farmacológicas de derivados pirazólicos: una revisión [J]. Moléculas, 2018, 23(1):134.
[47]WANG J, WANG D B, SUI L L, Et al. Natural products-isoxazole hybrid: A review of Evolución evoluciónin medicinal Chemistry [J] (en inglés). Arabian Journal of Chemistry, 2024, 17(6):105794.
[48]DAI R, WEI X, LI T, et al. Síntesis y actividad antitumoral de los derivados pirazol e isooxazol de panaxadiol [J]. Química & Biodiversity, 2023, 20 (8): e202300507.
[49]HOU W, DAI W, HUANG H, et al. Actividad farmacológica y mecanismo de las pirazinas [J]. European Journal of Medicinal Chemistry, 2023, 258:115544.
[50]RASHID H U, MARTINES M A U, DUARTE A P, et al. Research developments in the Síntesis, actividad antiinflamatoria y relaciones estructura-actividad de las pirimidinas [J]. RSC Advance. 2021, 11(11): 6060-6098.
[51]WANG S, ZHANG J, ZHANG J, et al. Síntesis síntesis síntesis and biological evaluación of heterocíclicos 20(s)-protopanaxadiol como potentes antiosteoporosis [J]. Journal of Medicinal Chemistry, 2023, 66 (17): 11965-11984.
[52]YANG K, YANG Z, Yu G, et al. Polyprodrug nanomedicines: An Emerging Paradigm for cancer therapy [J]. Materiales avanzados, 2022, 34 (6): e2107434.
[53]LU H, CEN J, REN Y, et al. Evaluation of the anti-inflammatory Dolor dolor Efecto efecto of O-carboxymethyl chitosan particles [J]. Polímeros, 2023, 15 (19): 4011.
[54]MATHIYALAGAN R, WANG C, KIM Y, et al. Preparación de polietilenglicol ginsenósido Rh1 Conjugy Rh2 y su eficacia contra el cáncer de pulmón y la inflamación [J]. Moléculas, 2019, 24 (23): 4367.
[55]BATHEJA S, GUPTA S, TEJAVATH K K, et al. Conjugados basados en TPP: ligandos potenciales [J]. 2024, 29(6):103983.
[56]MA L, WANG X, LI W,et al.Rational Diseño, síntesis y evaluación biológica de trifenilfosfami-ginsenoside conjugados as Mitocon- objetivo anti-cancer agentes [J]. Bioorganic Chemistry, 2020, 103: 104150.
[57]ZHANG H R, YE AQ, ZHANG Y W, et al. Progreso de la investigación sobre la derivatización ginsenósido y sus actividades biológicas [J]. Chinese Traditional and Herbal Drugs, 2022, 53(14): 4554-4567.
[58]YUAN [[] S Z, WANG B, Zhou X, et al. Progreso de la investigación sobre la biotransformación de ginsenósidos raros [J]. Science and Technology of Food Industry, 2023, 44(12): 480-489.
[59]RRN S, LIU R, WANG Y, et al. Síntesis y evaluación biológica de los análogos K del compuesto ginsenósido como una nueva clase de agentes antiasmáticos [J]. Bioorgánica y Cartas de química Medicinal, 2019, 29 (1): 51-55.
[60]REN G, LV W, DING Y, et al. Ginseng saponin metabolito 20(S)-protopanaxadiol alivia la fibrosis pulmonar por múltiples vías de señalización de objetivos [J]. Journal of Ginseng Research, 2023, 47 (4): 543-551.
[61]ZHANG H, ZHANG L, YANG C, et al. Efecto preventivo de las saponinas tipo protopanaxadiol saponinas y protopanaxatriol tipo saponinas on mielodepresión ratones induced by ciclofosfami [J]. fronteras In Pharmacology, 2022, 13: 845034.
[62]KIM A, PARK SM, KIM NS, et al. El ginsenósido Rc, un componente activo del Panax ginseng, alivia la atrofia muscular indupor estrés oxidativo a través de la mejora de la biogénesis mitocon[J]. Antioxidantes, 2023, 12 (8).
[63]LI S, LI JJ, ZHAO YY, et al. Integración Supramolecular de nanomateriales multifuncionales por azocalixareno decorado con manosa con ginsenósido Rb1 Para el tratamiento sinérgico de la artritis reumatoide [J]. ACS Nano, 2023, 17 (24): 25468-25482.
[64]LEE H, KONG G, TRAN Q, et al. Relación entre el ginsenósido Rg3 Y síndrome metabólico [J]. Fronteras en farmacología, 2020, 11: 130
[65]CHEN Y Y, LIU Q P, AN P, et al. Ginsenoside Rd: A promete natural neuroprotector agent [J]. Phytomedicine, 2022, 95: 153883.
-
anterior
¿Cuál es el método de extracción de ginsenósido?
-
siguiente
¿Qué es el ginsenósido Rh2 y su derivado?


 inglés
inglés francés
francés español
español ruso
ruso coreano
coreano Japonés japonés
Japonés japonés